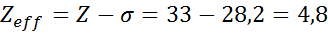Effektiv kärnkraftsbelastning
- 1073
- 283
- PhD. Emil Svensson
Vad är effektiv kärnkraftsbelastning?
De Effektiv kärnkraftsbelastning (representerad som zAvgränsning Och i vissa fall som Z*) Det är kärnbelastningen netto som en elektron upplever när den är i en polyhelektronisk atom (det vill säga den har mer än en elektron).
På ett mer exakt sätt är det den elektriska laddningen som skulle ha kärnan i en hypotetisk atom som kan locka sin enda elektron med samma kraft som kärnan i den verkliga atomen lockar samma elektron i närvaro av alla andra elektroner.
Det är en korrigerad kärnbelastning som tar hänsyn till effekten av närvaron av andra elektroner på en polylektronisk atom. Denna reducerade belastning förklarar varför de yttersta elektronerna i en polyhelektronisk atom är svagare kopplade till kärnan än interna elektroner.
Effektiv kärnbelastning är ett begrepp av stor betydelse i kemi, eftersom det gör att vi kan förstå den periodiska tendensen för många egenskaper som atomradie, jonradie, elektronegativitet, joniseringsenergier och mer.
Varför finns den effektiva kärnbelastningen?
Den effektiva kärnbelastningen uppstår från två fenomen:
- Den skärmande effekten av elektroner på polyhelektroniska atomer.
- Elektrostatisk avstötning bland elektroner eftersom alla har samma elektriska laddning.
han skärmeffekt Den består av en slags sköld som bildas av de inre elektronerna i en atom som täcker kärnan. Detta gör att de yttersta elektronerna "känner" en lägre attraktion från kärnan än de skulle känna om de andra elektronerna inte var närvarande.
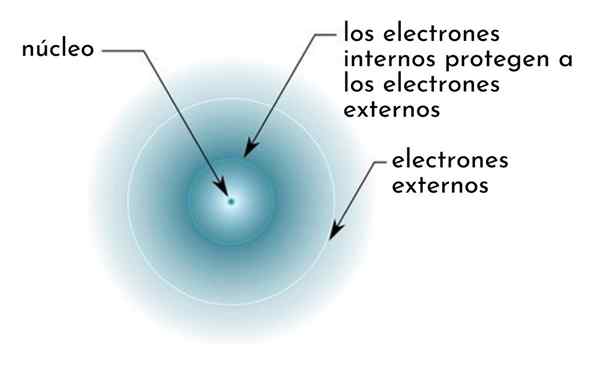 Figur schematiskt visar interna elektroner som fungerar som en skärm som skyddar de yttre elektronerna i attraktionen i kärnan
Figur schematiskt visar interna elektroner som fungerar som en skärm som skyddar de yttre elektronerna i attraktionen i kärnan Till exempel är natriumatomens kärnbelastning +11 (dess atomantal är z = 11), men den enda elektronen i Valencia som den har, känner faktiskt attraktionskraften för en belastning på endast +2,2.
Kan tjäna dig: natriumbensoat: struktur, egenskaper, användningar och riskerMed andra ord, skärmen av de andra 10 inre elektronerna orsakar natrium för Valencia -elektron att känna en kraft av kärnkraftsattraktion av bara den femte av vad som borde vara.
Förutom den skärmande effekten, repulsion mellan elektroner (som har samma elektriska laddning) bidrar också till att motverka kärnans kapacitet för att locka externa elektroner. Det vill säga denna avstötning hjälper också till att minska effektiv kärnbelastning.
Viktiga egenskaper hos effektiv kärnbelastning
Det bör noteras att den skärmningseffekt som är ansvarig för att minska effektiv kärnbelastning endast påverkar elektroner som är i samma energinivå eller i de övre skikten, men inte de mest inre elektronerna. Dessutom är effekten inte densamma för elektroner som finns i atomiska orbitaler och P än de som finns i orbitalerna D och F.
Av denna anledning känner varje elektronuppsättning av varje lager eller energinivå en annan effektiv kärnbelastning. Detta har viktiga konsekvenser för de olika elementens kemiska egenskaper.
Periodisk trend med effektiv kärnbelastning
Över en tid
Elektroner belägna på samma energinivå är mindre skärmning än de som finns i lägre energinivåer.
På grund av detta ökar den skärmningseffekten inte avsevärt när vi rör oss under en period, men den verkliga kärnbelastningen gör det. Av denna anledning är den effektiva kärnkraftsbelastningen Ökar från vänster till höger i det periodiska bordet.
Genom en grupp
Å andra sidan, när du passerar från en period till en annan i samma grupp (det vill säga när vi flyttar ner längs en grupp), läggs hela lager av mycket skyddande inre elektroner. Detta gör att den effektiva kärnbelastningen minskar från topp till botten eller, vad är detsamma, öka från botten uppåt.
Kan tjäna dig: ayaroínaEffektiv kärnbelastningsformel
Effektiv kärnbelastning kan beräknas med hjälp av en mycket enkel halvtidsekvation som tar hänsyn till det verkliga värdet på kärnbelastningen (ges av atomantalet, z) och en term som kallas konstant skärmning. Det senare omfattar effekterna av närvaron av andra elektroner i en.
Ekvationen ges av:
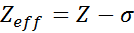
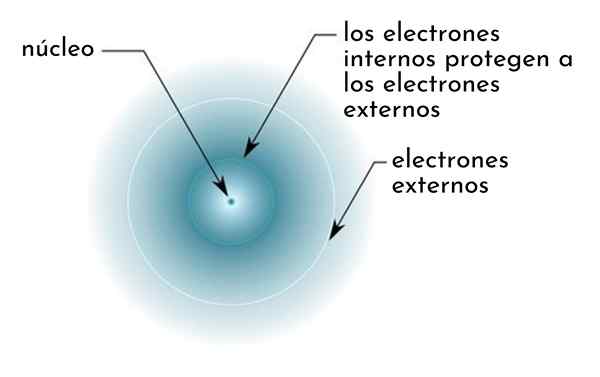
Där Z är atomnumret och σ (grekisk bokstav Sigma) representerar skärmningskonstanten, som beror på den elektroniska konfigurationen.
SLATER -regler
Skyddskonstanten kan uppskattas från ett system som kallas Slater -reglerna. Dessa regler tillåter beräkning av sköldkonstanten för en elektron genom att lägga till bidrag från de andra elektronerna till nämnda skärmkonstant. Dessa regler kan sammanfattas enligt följande:
- Alla elektron som är på samma energinivå (nivå n0) Tillhandahåller ett belopp på 0,35 till skärmkonstanten, såvida inte båda är på nivå 1, i vilket fall det ger 0,30.
- Varje elektron som är på omedelbart föregående nivå (på nivå n0-1) I en orbital S eller P ger den 0,85; Å andra sidan, om det är i en orbital d eller f det bidrar 1.
- Alla andra elektroner som är på lägre energinivåer (n0-2, n0-3, etc.), bidra 1 till skärmkonstanten.
Exempel på effektiv kärnbelastningsberäkning
Valencia elektron av natriumatomen
Den elektroniska konfigurationen av natriumatomen är 1s22s22 p63s1. Det vill säga att om vi vill beräkna den effektiva kärnbelastningen som Valencia Electron känner (Electron 3S1), vi måste lägga till bidrag från de andra 10 elektronerna efter reglerna för Slater.
Kan tjäna dig: järnoxid (ii): struktur, nomenklatur, egenskaper, användningarHur beräknar vi 3S Electron Shield Constant1 (n0= 3) Och detta är ensamt i Valencia -lagret, det finns inga andra elektroner på samma energinivå.
Den omedelbart tidigare nivån är n0-1 = 2, där det finns 8 elektroner i orbital S eller P som bidrar med 0,85 vardera, och det finns inga elektroner i orbitaler D eller F.
Slutligen är den enda nivån lägre än 2 n = 1, där det bara finns 2 elektroner. Allt detta sammanfattas i följande tabell:
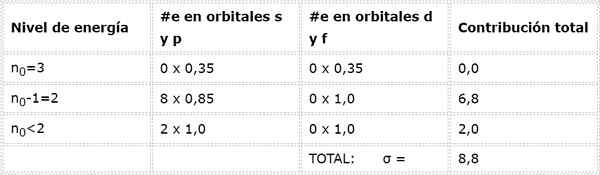
Som framgår ger de inre elektronerna i natrium en sköldkonstant på 8,8, så den effektiva kärnbelastningen som elektronen känner 3s1 är:
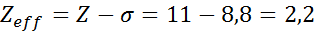
Arsenikvalencia elektroner
Den arseniska elektroniska konfigurationen är 1s22s22 p63s23p63D104S24p3. Valencia -skiktet är skikt 4 (n0= 4) som har 5 elektroner: (4s24p3). I detta fall kommer var och en av dessa 5 elektroner att känna effekten av de andra 4 som är i samma skikt och det för de andra 28 interna elektronerna som visas i tabellen:
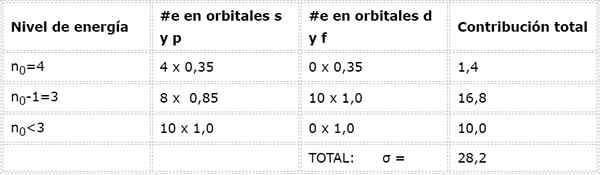
Därför är den effektiva kärnbelastningen som Arsenic Valencia -elektronerna känner: