Cykling
- 1438
- 341
- Erik Eriksson
 Cucloalquinos
Cucloalquinos Vilka är cykloalquinosna?
De Cykling De är organiska föreningar, som har en eller flera trippellänkar och en cyklisk enhet. Dess kondenserade molekylformler följer formel cnH2n-4. Således, om n är lika med 3, kommer formeln för nämnda cykloalquino att vara c3H2.
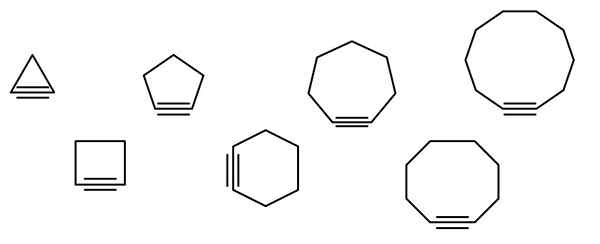
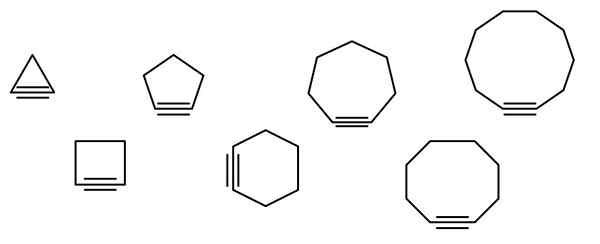
I den överlägsna bilden illustreras en serie geometriska figurer, men den i verkligheten består av exempel på cykloalquins. Var och en av dem kan betraktas som en mer oxiderad version av respektive cykloalcanos (utan dubbla eller tredubbla länkar). När de saknar en heteroátomo (o, n, s, f, etc.), är bara "enkla" kolväten.
Kemi kring cykloalquinos är mycket komplex, och det finns ännu fler mekanismer bakom deras reaktioner. De representerar en utgångspunkt för syntesen av många organiska föreningar, som i sin tur är föremål för möjliga applikationer.
I allmänna termer är de mycket reaktiva om de inte är "förvrängda" eller bildar komplexa med övergångsmetaller. Dessutom kan deras trippelbindningar kombineras med dubbelbindningar, vilket skapar cykliska enheter inuti molekylerna.
Att inte vara fallet, i sina enklaste strukturer kan de lägga till små molekyler till sina trippelbindningar.
Egenskaper hos cykloalquins
Apolaritet och trippellänk
Cyklesser kännetecknas av att vara apolära molekyler, och därför hydrofoba. Detta kan förändras om de i sina strukturer har någon heteroátomo eller funktionell grupp som ger ett betydande dipolmoment; Som i heterocykler med tredubbla länkar.
Men vad är en trippellänk? Det är inget annat än tre samtidiga interaktioner mellan två kolatomer med SP -hybridisering. En länk är enkel (σ), och de andra två π, vinkelrätt mot varandra. Båda kolatomerna har en fri SP-orbital för att koppla andra atomer (R-C≡C-R).
Det kan tjäna dig: radikal att hyra: hur de bildas, nomenklatur, exempelDessa hybrid orbitaler har 50% av S och 50% av karaktären P. Eftersom S -omloppet är mer penetrerande än P, gör detta faktum de två kolhydrarna i trippelbindningen fler syror (elektronacceptorer) än kolhydrarna i alkanerna eller alkenerna.
Av denna anledning representerar Triple Bond (≡) en specifik punkt för elektrondonatorarter som ska läggas till den som bildar enkla länkar.
Detta resulterar i brottet i en av π -länkarna och blir en dubbel länk (C = C). Tillägget fortsätter tills r4C-cr4, det vill säga helt mättade kol.
Ovanstående kan också förklaras på detta sätt: Triple Link är en dubbel omättnad.
Intermolekylära krafter
Cykloalcinmolekyler interagerar genom spridningskrafter eller krafter i London och efter interaktioner av typ π-x-typ. Dessa interaktioner är svaga, men när storleken på cyklerna ökar (som de sista tre på höger sida av bilden) lyckas de bilda fasta ämnen vid temperatur och omgivningstryck.
Vinkelspänning
Triple Link -länkar finns på samma plan och en linje. Därför har -C≡C- en linjär geometri, med orbitalerna på cirka 180 °.
Detta har ett allvarligt engagemang i cykloalquins stereokemiska stabilitet. Mycket energi krävs för att "fälla" orbitalerna SP, eftersom de inte är flexibla.
Ju mindre cykloalquino, desto mer måste orbital SP: er vikas för att tillåta den fysiska existensen av samma. Att analysera bilden kan det, från vänster till höger, att i triangeln är vinkeln på länkarna till sidorna på trippellänken mycket uttalad; Medan de är i decagon är de mindre plötsliga.
Kan tjäna dig: metylenblå: egenskaper, förberedelser, användningarEftersom cykloalquino är större är vinkeln på länkarna till orbital sp till idealen 180º närmare. Det motsatta händer när de är mindre och tvingar dem att böja och skapa en vinkelspänning I dem, installera cykloalquino.
Således har de största cykloalquinerna lägre vinkelspänning, vilket möjliggör deras syntes och lagring. Med detta är triangeln den mest instabila cykeln, och decagon den mest stabila av alla.
Egentligen är cyklooctin (Octagon) den med den minsta kända mer stabila; Andra finns endast som tillfälliga mellanhänder i kemiska reaktioner.
Cykelnomenklatur
Att utse cyklerna. Den enda skillnaden ligger i suffixet -ico i slutet av namnet på den organiska föreningen.
Huvudkedjan är en som har trippellänken och börjar räknas upp från det närmaste slutet på detta. Om du till exempel har cyklopropan. Om en metylgrupp är länkad på det övre toppunktet, kommer det att vara: 2-metylciclopropino.
R-C≡C-R-kolhydraterna har redan sina fyra bindningar, så det saknar hydrogener (som med alla cykloalquins av bilden). Detta händer inte bara om trippellänken är i terminalposition, det vill säga i slutet av en kedja (R-C≡C-H).
Cykloalquine -applikationer
Cykloalcans är inte särskilt vanliga föreningar, så inte heller deras tillämpningar. De kan tjäna som bindemedel (grupper som samordnar) till övergångsmetaller och därmed skapa en oändlighet av organometalliska föreningar som kan vara avsedda för mycket rigorösa och specifika användningar.
Kan tjäna dig: natriumbisulfit (nahso3): struktur, egenskaper, användningar, erhållaDe är vanligtvis lösningsmedel i sina mest mättade och stabila former. När de består av heterocykler, förutom att de har cykliska enheter C≡C-C = C-C≡C interna, finner de intressanta och lovande användningsområden som anticancerläkemedel; Sådant är fallet med diemicin för att. Andra föreningar med strukturella analogier har syntetiserats från den.
Exempel på cyklokinos
Bilden visar sju enkla cykloalquins, där det knappast finns någon trippellänk. Från vänster till höger, med sina respektive namn har de: Cyclopropino, triangeln; Ciclobutino, torget; Cycopentine, Pentagon; Cyclohexino, hexagon; Cycloheptino, hepagon; Cyclooctino, Octagon; och Cyclodecino, Decagon.
Baserat på dessa strukturer och ersätter väteatomerna hos mättade kol, kan andra föreningar härstammar från dem erhållas. De kan också genomgå oxidativa förhållanden för att generera dubbla länkar på andra sidor av cyklerna.
Dessa geometriska enheter kan vara en del av en större struktur, vilket ökar chansen att funktionalisera hela uppsättningen. Det finns inte många tillgängliga exempel på cykloalcino, åtminstone inte utan att fördjupa landen med organisk syntes och farmakologi.
Referenser
- Francis A. Sköldpaddsskal. Organisk kemi. (Sjätte upplagan., Sida 372, 375). MC Graw Hill.
- Wikipedia. (2018). Cykloalkyne. Taget från: i.Wikipedia.org
- William Reusch. (5 maj 2013). Namnge organiska föreningar. Taget från: 2.Kemi.Msu.Edu
- Oorganisk kemi. Cykling. Taget från: fullquimica.com
- Patrizia Diana & Girolamo Cirrincione. (2015). Biosyntes av heterocykler från isolering till genkluster. Wiley, sidan 181.
- Intressant organisk kemi och naturliga produkter. (17 april 2015). Cykloalkynes. Taget från: Quintus.Mickel.ch

