Nickelhydroxid (iii) struktur, egenskaper, användningar, risker
- 2926
- 766
- Anders Larsson
han Nickelhydroxid (III) Det är en oorganisk förening där nickelmetallen har ett oxidationsnummer på 3+. Dess kemiska formel är Ni (OH)3. Enligt de konsulterade källorna har det hittills inte varit möjligt att verifiera förekomsten av nickelhydroxid (III) eller (OH)3, Men nickeloxo-hydroxid (III), barn (OH) har erhållits.
Nickel (iii) NIO (OH) oxohydroxid är ett svart kristallint fast ämne som kristalliseras på två sätt: beta -formen och gammas. Den vanligaste kristallina formen (OH) är beta.
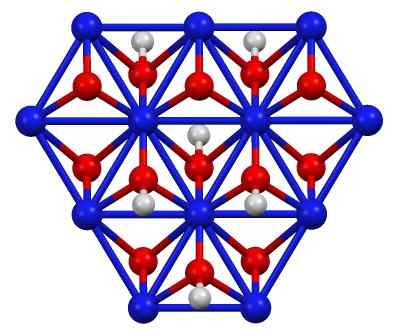
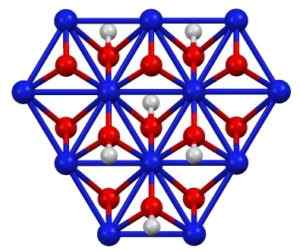 Nickeloxohydroxidstruktur (III), barn (OH). Blå = nickel, röd = syre, vit = väte. Författare: Smokefoot. Källa: eget arbete. Källa: Wikipedia Commons
Nickeloxohydroxidstruktur (III), barn (OH). Blå = nickel, röd = syre, vit = väte. Författare: Smokefoot. Källa: eget arbete. Källa: Wikipedia Commons Barnet (OH) kan erhållas genom oxiderande nickelnitratlösningar (ii) (eller (nej3)2) med klor (CL2) eller brom (Br2) I närvaro av kaliumhydroxid (KOH). Nickel (iii) oxohydroxid är mycket löslig i syror. Den har applikation i nickelbatterier, i Superca.
Nickel (iii) NIO (OH) och nickelhydroxid (II) eller (OH) (OH)2 De är förenade i driften av de flesta av sina applikationer, eftersom båda är en del av samma oxidreduktionsekvation.
Som en nickelförening utgör barnet (OH) samma risker för andra nickelsalter, det vill säga hudirritation eller dermatit och cancer.
[TOC]
Kristallstruktur
Nickeloxohydroxid (iii) kristalliseras på två sätt: Beta och Gamma. Beta-ß-nio (OH) -formen har en struktur som är mycket lik ß-Ni (OH)2, vilket verkar logiskt eftersom den första kommer från oxidationen av den senare.
Γ-nio (OH) -gammaformen är oxidationsprodukten från nickelhydroxid (ii) i sin alfa, a-Ni (OH) -form2. Liksom den senare har Gamma en skiktstruktur med alkaliska metalljoner, anjoner och vatten isär mellan lagren.
Elektronisk konfiguration
Hos barnet (OH) finns nickeln i oxidationstillståndet 3+, vilket innebär att 3 elektroner saknas på dess yttersta lager, det vill säga två elektroner i skikt 4 saknass och en elektron från lager 3d. NI: s elektroniska konfiguration3+ Hos barnet (OH) är: [ar] 3d7, Där [ar] är den elektroniska konfigurationen av ädla argongas.
Det kan tjäna dig: pi -länkNomenklatur
- NIO (OH): Nickel Oxohydroxide (III)
- Nickel svart
Egenskaper
Fysiskt tillstånd
Svart kristallint fast.
Löslighet
Nio (OH) oxohydroxid är mycket löslig i syror. Gammafasen upplöses i svavelsyra med syreutveckling.
Andra egenskaper
I varmt vatten blir det en oxohydroxid av nickel (ii) och (iii), eller3ANTINGEN2(ÅH)4.
Det sönderdelas till 140 ºC i nickel (ii) (barn och syreoxid.
Gammafasen (y-nio (OH)) kan erhållas på flera sätt, till exempel behandla nickel med en smält blandning av natriumperoxid (NA2ANTINGEN2) och natriumhydroxid (NaOH) vid 600 ºC och kylning i isvatten.
Gamma -fasen bryts ned när den värms upp till 138 ºC.
Ansökningar
I nickelbatterier
Edisons nickelhydrumbatteri, där KOH används som elektrolyt, är baserat på nickeloxohydroxidreaktionen (iii) med järn:
Ladda ner:
Fe + 2nio (OH) + H2Eller ⇔ Faith (OH)2 + 2ni (OH)2
Börda:
Det är en reversibel oxidreduktionsreaktion.
I anoden av dessa batterier inträffar en serie kemiska och elektrokemiska processer. Nedan är ett allmänt schema:
Ladda ner
P-NI (OH)2 ⇔ ß-nio (OH) + H+ + och-
Börda
Åldrande ↑ ↓ överbelastning
Ladda ner
α-Ni (OH)2 ⇔ γ-nio (OH) + H+ + och-
Börda
Kan tjäna dig: arsenik: historia, struktur, egenskaper, användningarI nickelbatteri -teknik kallas nickeloxohydroxid (III) NIO (OH) "Nickel Active Mass".
 Uppladdningsbara batterier. Författare: Superuerergeneric. Källa: eget arbete. Källa: Wikipedia Commons.
Uppladdningsbara batterier. Författare: Superuerergeneric. Källa: eget arbete. Källa: Wikipedia Commons. I elektrokatalys som en regenererbar katalysator
Barnet (OH) har använts framgångsrikt i elektrosyntesen av azopirazoler genom den elektrokatalitiska oxidationen av aminopyrazoler. Dess användbarhet i syntesen av karboxylsyror som börjar från alkoholer eller karbonylföreningar har också bevisats.
 Erhålla en karboxylsyra genom att oxidera en alkohol katalyserad av barnet (OH). Källa: Ursprungligen från In.Wikipedia. Originalförfattare uppladdare var v8rik på i.Wikipedia. Källa: Wikipedia Commons
Erhålla en karboxylsyra genom att oxidera en alkohol katalyserad av barnet (OH). Källa: Ursprungligen från In.Wikipedia. Originalförfattare uppladdare var v8rik på i.Wikipedia. Källa: Wikipedia Commons Ett annat exempel är den kvantitativa omvandlingen av hydroximetypyridin till en pyridokarboxylsyra. I detta fall är stål- eller nickelektroden motsvarande anoden täckt med ett lager av barn (OH). Mediet där elektrolys utförs är alkaliskt.
I dessa reaktioner fungerar barnet (OH) som en reduktion-utomhusförmedlare eller "redox" -mediator.
Elektrolys utförs i en cell med nickelanod och titankatod, i alkaliskt medium. Under processen bildas den eller (OH)2 På ytan av nickelanoden, som snabbt oxideras till barn (OH):
Ni (OH)2 + Åh- - och- ⇔ nio (oh) + h2ANTINGEN
Barnet (OH) reagerar med det organiska underlaget och den önskade organiska produkten erhålls, vilket regenererar Ni (OH)2:
NIO (OH) + organisk förening → Ni (OH)2 + produkt
När Ni (OH) regenereras2, Katalysreaktionen fortsätter.
Användningen av barnet (OH) som elektrokatiserare gör det möjligt att få organiska föreningar med låga kostnader och på ett miljövänligt sätt.
I Super CardPisors
Barnet (OH) tillsammans med Ni (OH)2 De utgör utmärkta material för supercaidingelektroder (engelska Superkapacitos).
Ni (OH)2 + Åh- ⇔ nio (oh) + h2Eller + e-
De har hög kapacitans, låg kostnad och enligt vissa referenser under miljöpåverkan.
 Kondensatorer i en elektronisk krets. Författare: pdphotos. Källa: Pixabay.
Kondensatorer i en elektronisk krets. Författare: pdphotos. Källa: Pixabay. De har dock låg konduktivitet. Detta löses med användning av nanopartiklar av nämnda föreningar, eftersom således ökar ytan och minskar det avstånd som krävs för diffusion, vilket säkerställer hög hastighet för överföring av elektroner och/eller joner.
Kan tjäna dig: elastiska materialVid oxidation av metalljoner
En av de kommersiella tillämpningarna av nickeloxohydroxid (III) är baserad på dess förmåga att oxidera koboltjoner (ii) i lösning på koboltjoner (III).
Risker
I lösningen är nickeln mer stabil som en jon eller2+, Därför är det inte vanligt att komma i kontakt med NI3+. Emellertid är försiktighetsåtgärderna desamma, eftersom nickeln, vare sig metallisk, i lösning eller i form av dess fasta salter, kan orsaka hudsensibilisering.
Det är tillrådligt att använda skyddsutrustning och kläder, till exempel ansiktssköld, handskar och säkerhetsskor. Allt detta måste användas varje gång det finns möjlighet att komma i kontakt med nickelösningar.
Om dermatit inträffar, bör den behandlas med en läkare för att utesluta att det orsakas av nickel.
När det gäller möjligheten till inandning är det god praxis.
Alla nickelföreningar klassificeras av International Cancer Research Agency, eller IARC (akronym för engelska Internationell byrå för cancerforskning), i kategorin cancerframkallande ämnen för människan.
Detta är baserat på epidemiologiska och experimentella data.
Referenser
- Bomull, f. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Lyalin, b.V. et al. Elektrosyntes av azopyrazoler via oxidationen av N-alkylaminopyrazoler på ett barn (OH) -anod i vattenhaltig alkali-A-grön metod för N-N-homocouplel. Tetrahedronbrev. 59 (2018) 2741-2744. Återhämtat sig från Scientedirect.com.
- Liuyang, Zhang, et al. (2018). Nickelbaserade material för superkapacitos. Material idag. Återhämtat sig från Scientedirect.com
- Ettel, v.TILL. och Mosolu, m. TILL. (1977). Förberedelse av nickel svart. ELLER.S. Patentnr. 4,006,216. 1 februari 1977.
- Scharbert, f. (1993). Process för oxidation av hydroximetylpyridinderivat till pyridinekarboxylsyrorivat vid nickeloxidhydroxidanoder. ELLER.S. Patentnr. 5 259 933. 9 november 1993.
- Kirk-THERMER (1994). Encyclopedia of Chemical Technology. Volym 17. Fjärde upplagan. John Wiley & Sons.
- Ullmanns Encyclopedia of Industrial Chemistry. (1990). Femte upplagan. Volym vid 17. VCH Verlagsgellschaft MBH.
- McBreen, James. (1997). Nickelhydroxider. I handbok med batterimaterial. VCH -utgivare. Återhämtat sig från Osti.Gov.
- « Makrocomputers historia, egenskaper, användningar, exempel
- Presenterade analoga datorer, komponenter, typer »

