Vattenens fysiska och kemiska egenskaper

- 815
- 165
- Johan Gustafsson
De Vattenens fysiska och kemiska egenskaper De är alla de manifestationer av vattnet som vi kan mäta tack vare interaktioner mellan deras molekyler med sig själva eller deras miljöer. Men vad är vatten? Vatten är en kemisk substans eller molekyl som bildas av föreningen av en syreatom (O) med två väteatomer (H).
Dessa tre atomer förblir förenade genom bildandet av kovalenta bindningar, mycket starka och stabila länkar. Vattenmolekylen är för formel h2Eller att kunna skriva som H-O-H. Det är denna molekyl, dess länkar och dess interaktioner är ansvariga för att vara en färglös och smaklös flytande substans.

Vatten är i en stor distribuerad andel över hela jorden, mellan färskt och saltat vatten. Vatten är nödvändigt att livet finns på vår planet, eftersom det är en mycket värdefull naturresurs. Det är mellan 60 och 70% i levande organismer, vilket är en hög andel som gör att de kan uppfylla otaliga funktioner.
Bland några av dessa vitala funktioner är strukturella, tillsynsmyndigheter såsom underhåll av kroppstemperatur och pH -reglering (surhet eller alkalinitet) inom normala gränser. På samma sätt utför vatten transport av näringsämnen och avfall i levande varelser.
Det används också i många områden inom människans produktiva, tekniska, vetenskapliga och dagliga rutinmässiga arbete; Från toalett, matlagning, bland andra användningsområden.
[TOC]
Fysiska vattenegenskaper
De fysiska egenskaperna hos vatten är relaterade till de egenskaper eller storlekar som kan mätas eller bestämmas när man överväger materia, såsom dess massa, energi, bland andra.
Bland de fysiska storleken på vatten är dess färg, lukt, hur den kan hittas och alla de som vi kan bestämma utan reaktioner eller förändra dess kemiska sammansättning.
Smak
Genom att smaka lite rent vatten till vår smak visar det sig att det är Insabor eller smaklöst. Det är lika luktlöst eller lukt. För reningsprocessen kan en liten lukt uppfattas som beror på klorrester. Det är mineralerna som ger vattnets vatten olika bokstäver.
Aspekt

Vatten i allmänhet är färglöst och transparent när det observeras i ett glasglas. Det verkar dock som om det hade en ljusblå färg när den ackumuleras i stora mängder i stora behållare, eller när de observeras i glaciärer, floder eller hav.
Kan tjäna dig: vad är forskningskällor?Och i själva verket uppvisar vattnet en viss blek blåaktig färg, vars uppfattning är koncentrerad, desto högre är mängden vatten.
Vattenstater
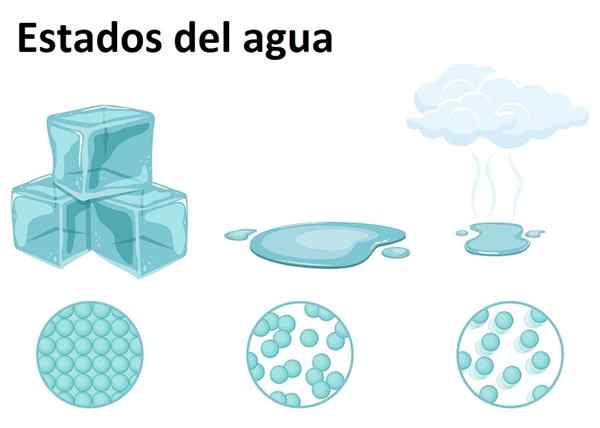 Fast, flytande och gasformigt tillstånd
Fast, flytande och gasformigt tillstånd Vatten är mycket rik på jorden och kan hittas i något av de tre materien: fast, flytande eller gasformigt. Vatten vid rumstemperatur är en flytande substans, vilket motsvarar dess vanligaste form.
Så fast, vatten kallas is eller snö, beroende på storleken på dess kristaller och processen för dess bildning. Samtidigt bildas det gasformiga tillståndet när vattnet passerar från flytande tillstånd till gasformigt och bildar den berömda vattenånga, lätt igenkännande i köket och ovanför maten.
Densitet
Ren vattentäthet sträcker sig runt 1 g/cm3. Under tiden är havsvattens densitet lite högre på grund av det salt det innehåller.
Frys punkt
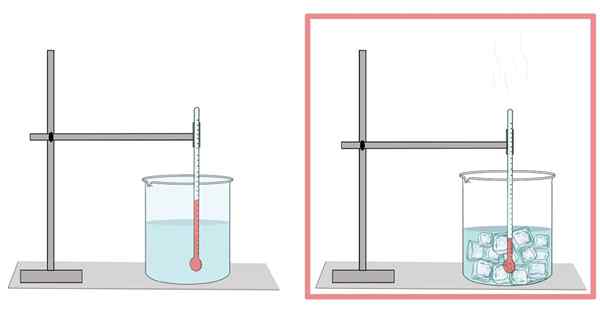
Vatten fryser vid 0 ° C. Vid denna temperatur passerar från sin flytande fas till det fasta ämnet. När vattnet är fruset expanderar det. Det är därför den i sin fasta form har mindre densitet än i dess flytande tillstånd, vilket gör det lättare för is att flyta på flytande vatten.
På samma sätt är detta anledningen till att vattenkylning i en flaska inte ska fyllas mycket, eftersom isen expanderar och slutar bryta flaskan.
Kokpunkt
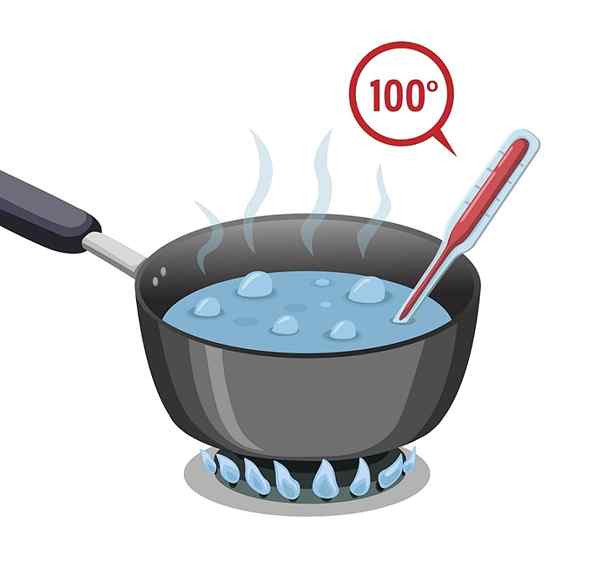
Vattnet har en hög kokpunkt som är 100 ° C. Det måste underkastas varmt så att det kan värma och koka eller nå sin kokpunkt.
Vattnet har sedan en hög specifik värme, eller kallas också värmekapacitet, vilket gör att det försenar uppvärmningen; Men också för att svalna, det vill säga att processen som krävs för att förlora den förvärvade värmen är långsam.
Den här egenskapen gör det mycket användbart i kylsystem, i kroppstemperaturregleringssystem, bland andra relaterade.
Elektrisk konduktivitet
Vatten är en bra elektricitetsledare. Men rent vattnet kommer alltid att ha en viss mängd joner, vilket ger det egenskapen att ha en av de högsta dielektriska konstanterna bland icke -metalliska vätskor.
Sammanhållning
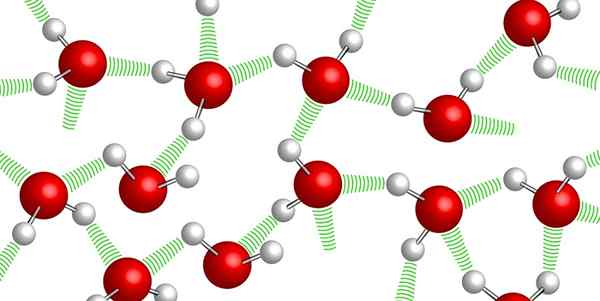 Vätebroar mellan vattenmolekyler
Vätebroar mellan vattenmolekyler Vattenmolekyler förblir tillsammans med varandra tack vare de så kallade vätebroarna: svaga bindningar som är etablerade mellan en och en annan vattenmolekyl. På grund av denna höga sammanhållningsnivå är det mycket svårt att komprimera vatten.
Kan tjäna dig: 7 dokumentära forskningsinstrumentAnslutning

Det är lätt för vatten att fästa, till exempel, till den väl rena ytan på ett glas, bilda en film, som vi kallar fukt eller "våt". Vatten följer också snabbt vår hud, så vi blir våta så snart vi kommer in i en pool. Annars skulle vi torka på några sekunder.
Ytspänning
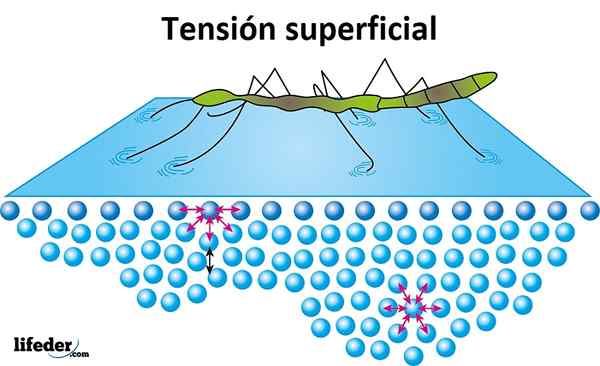
Ytspänningen är motståndet som vätskans motstånd erbjuder på ytan som ska penetreras. Vatten har en hög ytspänning, produkten av sammanhållningen som finns mellan dess molekyler, vilket gör att det lätt bildas, istället för att fritt sprida en slät yta.
Ytspänningen bevisas när insekter verkar röra sig eller gå på vattnet utan att sjunka, och det är anledningen till att vissa blad eller andra ljusa föremål kan flyta över vattnet.
Kapillaritet

Den enkelhet som vattnet stiger upp eller lågt genom ett kapillärrör beskriver vattenkapillären egenskapen. Denna egenskap beror också på de höga egenskaperna för sammanhållning och vidhäftning som vatten har.
Kapillariteten utnyttjas av växtens natur för att leverera vatten till bladen på de högsta grenarna av ett träd, samt underlättar dess absorption av växternas rötter.
På samma sätt gör egenskaperna för ytspänning och kapillaritet vattnet till en strukturell del av cellerna, som är en del av blodet, och som rinner eller flyter lätt genom de olika blodkärlen.
Lösningsmedel

Vatten kan lösa upp många ämnen, vilket är viktigt för levande organismer, eftersom alla kemiska reaktioner från levande varelser förekommer i en vattenhaltig miljö. I levande organismer fungerar det som en transport av näringsämnen, joner och många andra ämnen.
Det tjänar också för transport av avfall, till exempel urea, som elimineras i urinvatten. När ett ämne upplöses och blandas väl med vatten sägs det att det är hydrofil eller hydrosoluble. Om du inte blandar eller löser sig väl, sägs det att ämnet är hydrofobt eller olösligt i vatten.
Kemiska vattenegenskaper
Kemiska egenskaper eller egenskaper är de som inträffar när förändringar i den kemiska strukturen för vatten produceras. Det är då viktigt att ta en kort titt på dess molekylstruktur.
Kemisk natur
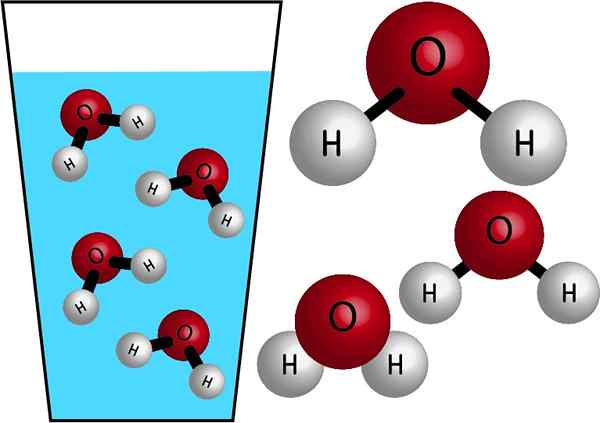
Vatten är en oorganisk molekyl, eftersom den inte innehåller c (kol), och dess kemiska formel är h2ANTINGEN. Deras atomer förenas genom att dela elektroner som bildar kovalenta bindningar, starka och mycket stabila länkar. Dess molmassa är 18 g/mol, det vill säga en mol vatten har en massa på 18 gram.
Kan tjäna dig: vetenskaplig forskningPolaritet
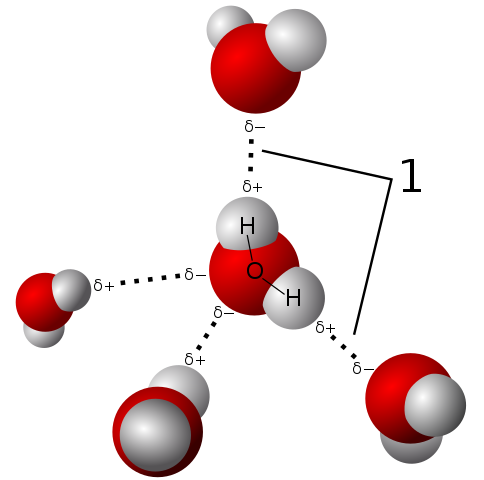 Vattenpolaritet tillåter sin molekyl att etablera mycket starka vätebroar
Vattenpolaritet tillåter sin molekyl att etablera mycket starka vätebroar Vattenmolekylen är neutral, men den presenterar en viss polaritet, eftersom delningen av dess elektroner inte är så rättvis.
När syre lockar sig starkare de delade elektronerna till sig själv, är vattenmolekylen med denna sida där syre är med en tendens att ha en viss negativ belastning; Och därför kvarstår det med en positiv partiell belastning där hydrogener är (observera den överlägsna bilden).
Denna polaritet underlättar facket med varandra av vattenmolekylerna och vattenföreningen med andra molekyler som också har belastningsskillnader i deras struktur, vilket främjar de fysiska egenskaperna som beskrivs i föregående avsnitt.
Jonisering
Spontant i flytande vatten finns det en liten jonisering eller självdissociation. Det betyder att några av dess molekyler omorganiseras genom att ändra dess normala molekylstruktur som genererar nya elektriskt laddade molekyler, såsom hydroniumjoner (h3ANTINGEN+) och hydroxyl (OH-).
Reaktiv kapacitet
Vatten reagerar med många ämnen och bildar en stor mångfald av kemiska föreningar. Genom elektrolys kan vatten brytas genom att separera syre från dess två hydrogener. Denna process inträffar när en elektrisk ström passerar genom vatten. Även vatten i sin fasta form kan också vara en del av vissa kemiska reaktioner.
pH
 pH nära 7
pH nära 7 Rent vatten har ett neutralt pH (lika med 7), medan havsvatten är något alkaliskt (större än 7). Regnvatten surgörs (pH mindre än 7) något när de blandas med de komponenter som finns i atmosfären, såsom koldioxid eller CO2, Till exempel.
Anoterism
Vatten är amfotat, det vill säga det kan bete sig som en syra eller som bas beroende på lösningens pH. Denna kemiska egenskap stöder sin roll som pH -regulator.
Referenser
- Shiver & Atkins. (2008). Oorganisk kemi. (Fjärde upplagan). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Castillero m. ANTINGEN. (2020). Psykologi och sinne. De 15 fysiska och kemiska egenskaperna hos vatten. Återhämtat sig från: psykologi och.com
- Wikipedia (2020). Vattenegenskaper. Hämtad från: i.Wikipedia.org
- Skarp k. TILL. (s.F.). Vatten: Struktur och egenskaper. Återhämtad från: Crystal.Med.Utbrett.Edu
- Byju. (s.F.). Vattenens fysiska och kemiska egenskaper. Återhämtat sig från: byju.com
- Skolenergi och miljö. (s.F.). Vatten var en resurs. Återhämtat sig från: eariscuola.netto

