Estrar
- 1135
- 65
- Anders Svensson
 Esteres är organiska föreningar som har en del av karboxylsyra och en annan alkohol
Esteres är organiska föreningar som har en del av karboxylsyra och en annan alkohol Vad är estrar?
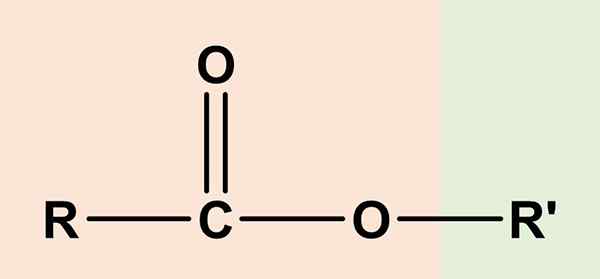
De estrar De är organiska föreningar som har en karboxylsyrakomponent och en annan alkohol. Dess allmänna kemiska formel är RCO2R' eller rcoor'. Den högra sidan, RCOO, motsvarar karboxylgruppen, medan höger eller' Det är alkohol. De två delar en syreatom och delar en viss likhet med etrarna (ROR ').
Av denna anledning är acetatet av etyl, CH3Cooch2Ch3, Det enklaste av estrar, betraktades som Ättiksyra- eller vinägerät, Och därifrån det etymologiska ursprunget till namnet 'ester'. Så att en ester består i ersättningen av det sura väte i COOH -gruppen, med en alkoholhyrning från en alkohol.
Var är estrarna?
Från jordens jordar finns det många naturliga källor. Den trevliga lukten av frukt, som bananer, päron och äpplen, är produkten av interaktion mellan estrar med många andra komponenter. De finns också i form av triglycerider i oljor eller fetter.
Vår kropp tillverkar triglycerider från fettsyror, som har långa kolsyrade kedjor och glycerolalkohol. Vad som skiljer vissa estrar från andra ligger både i r, kedjan för syrakomponenten, som i r ', den för alkoholhaltiga komponent.
En ester med låg molekylvikt måste ha få kol i r och r ', medan andra, såsom vaxer, har många kol, särskilt i r', alkoholhaltiga komponent och därför höga molekylvikter.
Men inte alla estrar är strikt organiska. Om Carbonhel -gruppatomen i karbonylgruppen ersätts av en av fosfor, kommer Rpoor att ha '. Detta är känt som en fosfatester och är avgörande betydelse i DNA: s struktur.
Således, när en atom kan kopplas till kol eller syre, såsom svavel (rsoor '), kan den följaktligen bilda en oorganisk ester.
Estres egenskaper
Estrar är inte syror eller alkoholer, så de uppför sig inte som sådana. Dess smält- och kokpunkter, till exempel, är lägre än de med liknande molekylvikter, men närmare värdena till aldehyder och ketoner.
Butanoic syra, cho3Ch2Ch2COOH, har en kokpunkt på 164 ° C, medan etylacetat, CH3Cooch2Ch3, av 77.1: a c.
Bortsett från det senaste exemplet, kokningspunkterna på 2-metylbutan3Ch (ch3) Ch2Ch3, Metylacetat, CHO3Cooch3, och 2-butanol, cho3,Ch (oh) ch2Ch3, De är följande: 28, 57 och 99º C. De tre föreningarna har molekylvikter på 72 och 74 g/mol.
Låga molekylära pesosestrar tenderar att vara flyktiga och har behagliga luktar, varför deras innehåll i frukt ger dem deras familjedoar. Å andra sidan, när deras molekylvikter är höga, är de färglösa och luktlösa kristallina fasta ämnen, eller beroende på deras struktur, kan de uppvisa feta egenskaper.
Vattenlöslighet
Karboxylsyror och alkoholer är vanligtvis lösliga i vatten, såvida de inte har en hög hydrofob karaktär i sina molekylstrukturer. Detsamma gäller för estrar. När r eller r 'är korta kedjor kan estern interagera med vattenmolekyler genom dipol-dipolo och styrkor från London Forces.
Kan tjäna dig: kemisk föreningDetta beror på att estrar är vätebryggacceptorer. Som? För sina två rcoor syreatomer '. Vattenmolekyler kan bilda vätebroar med något av dessa syre. Men när R- eller R -kedjorna är väldigt långa, avvisar de vattnet i sin omgivning, vilket gör det omöjligt för deras upplösning.
Ett uppenbart exempel på detta inträffar med triglyceridestrar. Deras sidokedjor är långa och gör oljor och fett olösliga i vattnet, såvida de inte är i kontakt med ett mindre polärt lösningsmedel, mer relaterade till dessa kedjor.
Hydrolysreaktion
Ester kan också reagera med vattenmolekyler i det som kallas hydrolysreaktion. De kräver emellertid en syra eller grundläggande miljö för att främja mekanismen för nämnda reaktion:
Rcoor ' + H2ANTINGEN RcoÅh + R'oH
(Sur hälft)
Vattenmolekylen tillsätts till karbonylgruppen, C = O. Syrahydrolys sammanfattas vid ersättningen av varje r 'av alkoholhaltig komponent med en OH från vatten. Observera också hur estern "bryts" i sina två komponenter: karboxylsyra, rcooh och r'oh alkohol.
Rcoor ' + Åh- => RcoANTINGEN- + R'oH
(Grundläggande medium)
När hydrolys utförs i ett basmedium inträffar en irreversibel reaktion känd som förtvålning. Detta är mycket anställd och är hörnstenen i utarbetandet av hantverk eller industriella tvålar.
Rcoo- Det är karboxylatanjonen, stabil, som är associerad elektrostatiskt med den dominerande katjonen i mitten.
Om den använda basen är NaOH bildas saltet. När estern är en triglycerid, som per definition har tre R -sidokedjor, bildas tre fettsyrasalter, rcoone och glycerolalkohol.
Reduktionsreaktion
Estrar är mycket oxiderade föreningar. Det betyder att det har flera kovalenta bindningar med syre. Genom att eliminera C-O-bindningar inträffar en paus som slutar separera syran och alkoholhaltiga komponenter; Och ännu mer reduceras syra till ett mindre oxiderat sätt till en alkohol:
Rcoor '=> rch2Oh + r'oh
Detta är reduktionsreaktionen. Ett starkt reducerande medel behövs, såsom litium och aluminiumhydrid, lialh4, och av ett surt medium som främjar elektronmigration. Alkoholer är de minsta formerna, det vill säga de som har mindre kovalenta bindningar med syre (endast en: C-OH).
De två alkoholerna, RCH2OH + R'OH, kom från de två respektive kedjorna i den ursprungliga esterna rcoor '. Detta är en metod för syntes av värde -tillägg alkoholer från dess estrar.
Om du till exempel ville tillverka en alkohol av en exotisk estrar skulle detta vara en bra väg för det ändamålet.
Transsterifieringsreaktion
Estrar kan förvandlas till andra om de reagerar på sura eller grundläggande medier med alkoholer:
Rcoor ' + R "oh RcoEller " + R'oH
Esterstruktur
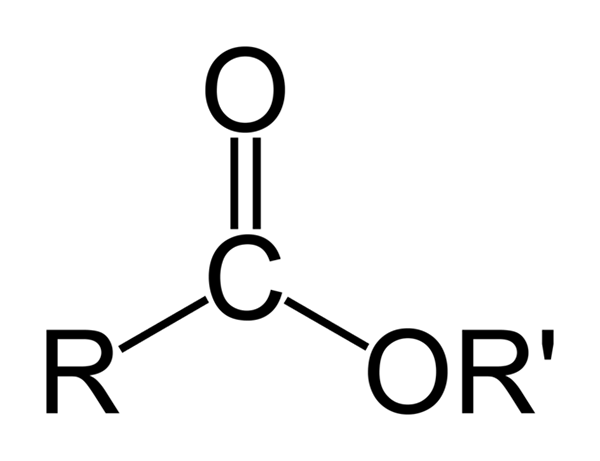 Allmän kemisk struktur för organiska estrar. Källa: Ben Mills via Wikipedia
Allmän kemisk struktur för organiska estrar. Källa: Ben Mills via Wikipedia Den överlägsna bilden representerar den allmänna strukturen för alla organiska estrar. Observera att R, karbonylgruppen C = O, och eller ', bildar en platt triangel, produkt av SP -hybridisering2 av den centrala kolatomen. Men andra atomer kan anta andra geometrier, och deras strukturer beror på den inre naturen hos R eller R '.
Kan tjäna dig: nitrater: egenskaper, struktur, nomenklatur, träningOm r eller r 'är enkla alqulicas -kedjor, till exempel av typen (välj2)nCh3, Du kommer att se sickzagueada ut i rymden. Detta är fallet med Pentilo Butanoat3Ch2Ch2Cooch2Ch2Ch2Ch2Ch3.
Men i någon av kolhydraterna i dessa kedjor kunde en gren eller omättning hittas (C = C, C≡C), vilket skulle modifiera esterns globala struktur. Och av denna anledning varierar dess fysiska egenskaper, såsom löslighet och dess kokning och fusionspunkter, med varje förening.
Till exempel har omättade fetter dubbla länkar i sina R -kedjor, vilket negativt påverkar intermolekylära interaktioner. Som ett resultat sjunker deras smältpunkter, tills de är flytande eller oljor vid rumstemperatur.
Vätebryggas acceptor
Även om bilden av estrar -skelettet sticker ut mer, är det R- och R -kedjorna som är ansvariga för mångfald i deras strukturer.
Emellertid förtjänas en strukturell egenskap hos estrarna till triangeln: de är vätebro acceptorer. Som? Av syre av karbonyl- och alkoxidgrupper (-Or ').
Dessa har fria elektronpar, som kan locka delvis positiva väteatomer av vattenmolekyler.
Därför är det en speciell typ av dipol-dipolinteraktioner. Vattenmolekylerna närmar sig estern (om r o r 'kedjorna inte förhindrar och broarna bildas c = o-h2Eller eller åh2-O-r '.
Esters nomenklatur
För att på lämpligt sätt namnge en ester är det nödvändigt. Också möjlig gren, substituent eller omättnad.
När detta är gjort läggs namnet på r 'för alkoxidgruppen -eller' suffixet läggs till -ilo, Medan karboxilo -coor -gruppkedjan r, suffixet -Ato. Först nämns avsnitt R, följt av ordet 'och sedan namnet på R' avsnitt ''.
Till exempel Cho3Ch2Ch2Cooch2Ch2Ch2Ch2Ch3 Den har fem kol på höger sida, det vill säga de är de som motsvarar r '. Och på vänster sida finns det fyra kolatomer (inklusive karbonylgruppen C = O).
Därför är r 'en pentilgrupp, och R A Butane (för att inkludera karbonyl och överväga huvudkedjan). Sedan, för att ge namnet till föreningen räcker det att lägga till motsvarande suffix och namnge dem i rätt ordning: ButaneAto pentilo.
Hur man namnger följande förening: CH3Ch2Cooc (ch3)3? Kedjan -c (cho3)3 motsvarar den rekto-butylalquilical substituent. Eftersom vänster sida har tre kol är det en "propan". Han heter då: propanAto av tert-menilo.
Hur bildas estrar?
Förestring
Det finns många rutter för att syntetisera ester, av vilka till och med kan vara nya. Men de konvergerar alla i det faktum att triangeln i bilden av strukturen måste bildas, det vill säga co-o-länken. För det måste det starta från en förening som tidigare har karbonylgruppen: som en karboxylsyra.
Och vad ska karboxylsyran kopplas? Till en alkohol, annars skulle det inte ha den alkoholhaltiga komponenten som kännetecknar estrarna. Karboxylsyror kräver emellertid värme och surhet för att reaktionsmekanismen ska fortsätta. Följande kemisk ekvation representerar ovanstående:
Kan tjäna dig: aluminiumhydrid (Alh3): struktur, egenskaper, användningarRCOOH + R'OH RCOOR ' + H2ANTINGEN
(Sur hälft)
Detta är känt som förestring.
Till exempel kan fettsyror förestras med metanol, CHO3Åh, för att ersätta sina syror med metylgrupper, så denna reaktion kan också betraktas som metylering. Detta är ett viktigt steg när man bestämmer fettsyraprofilen för vissa oljor eller fetter.
Esters från syraklorider
Ett annat sätt att syntetisera estrar är från acylklorider, RCOCL. I dem, istället för att ersätta en OH -hydroxylgrupp, ersätts CL -atomen:
RCOCL + R'OH => RCOOR ' + HCL
Och till skillnad från sterifieringen av en karboxylsyra frisätts inte vatten utan saltsyra.
Andra metoder finns tillgängliga inom världen av organisk kemi, såsom oxidation av Baeyer-Villiger, som använder peroxysyror (RCOOOH).
Estresanvändningar
 Esteres används för olika saker, till exempel ljus
Esteres används för olika saker, till exempel ljus Bland de viktigaste användningarna av estrar är:
- I utarbetande ljus eller ljus, till exempel den överlägsna bilden. För detta ändamål används mycket långa sidokedjeestrar.
- Som medicinsk konserveringsmedel eller mat. Detta beror på verkan av parabenerna, som inte är annat än esters av para-hydroxibensoesyra. Även om de behåller produktens kvalitet finns det studier som ifrågasätter dess positiva effekt på kroppen.
- De tjänar för tillverkning av konstgjorda dofter som imiterar lukten och smaken hos många frukter eller blommor. Så att estrar finns i godis, glass, parfymer, kosmetika, tvålar, schampon, bland andra kommersiella produkter som förtjänar aromer eller attraktiva smaker.
- Estrar kan också ge en positiv farmakologisk effekt. Av denna anledning har läkemedelsindustrin ägnat sig åt att syntetisera estrar härrörande från syror som finns i kroppen för att utvärdera eventuell förbättring av behandlingen av sjukdomar. Aspirin är ett av de enklaste exemplen på dessa estrar.
- Flytande estrar, såsom etylacetat, är tillräckliga lösningsmedel för vissa typer av polymerer, såsom nitrocellulosa och ett brett spektrum av hartser.
Exempel på estrar
Några ytterligare estrar -exempel är följande:
- Butanato de pentilo, ch3Ch2Ch2Cooch2Ch2Ch2Ch2Ch3, som luktar albicoque och päron.
- Vinylacetat, CHO3Cooch2= Ch2, från vilken polyvinylacetatpolymeren inträffar.
- Isopentilo pentanoato, ch3Ch2Ch2Ch2Cooch2Ch2Ch (ch3)2, som efterliknar smaken av äpplen.
- Etylpropanoat, ch3Ch2Cooch2Ch3.
- Propylmetanoat, hcooch2Ch2Ch3.
Referenser
- T.W. Graham Solomons, Craight B. Fryhle. Organisk kemi. (Tionde upplagan, s 797-802, 820) Wiley Plus.
- Carey, f. TILL. Organic Chemistry (2006) Sjätte upplagan. MC Graw Hill -redaktion-
- Kemi librettexts. Esers nomenklatur. Återhämtad från: kem.Librettexts.org
- Administration. (19 september 2015). Estrar: dess kemiska natur, egenskaper och användningar. Taget från: ren-kemisk.com
- Organisk kemi i vårt dagliga liv. (9 mars 2014). Vad är användningen av estrar? Hämtad från: Gen2ChemistAssignment.Liten.com
- Kemiker.Net (2018). Exempel på estrar. Återhämtat sig från: kemiker.netto
- Paz María de Lourdes Cornejo Arteaga. Estrar. Taget från: uaeh.Edu.mx
- Jim clark. (Januari 2016). Introduktionsestrar. Taget från: Chemguide.co.Storbritannien

