Isoamilo -struktur, egenskaper, syntes och använder acetat

- 2752
- 137
- Johan Olsson
han Isoamilocetat Det är en ester vars molekylformel är Cho3Coo (ch2)2Ch (ch3)2. Vid rumstemperatur består den av en oljig, klar, färglös, brandfarlig och flyktig vätska. I själva verket är det en för flyktig och doftande ester.
Dess huvudsakliga egenskap är att säga adjö till en lukt som bidrar till aromen av många frukter, särskilt bananer eller banan. Dessutom utgör denna sista frukt en av dess naturliga källor par excellence.
 Bananer, vars karakteristiska arom beror på isoamiloacetat. Källa: Pixabay.
Bananer, vars karakteristiska arom beror på isoamiloacetat. Källa: Pixabay. Därifrån namnet på bananolja som ges till en isoamiliska acetatlösning eller en blandning av isomylacetat med nitrocellulosa. Föreningen används allmänt som en smak av mat, glass och godis.
Dessutom används det vid utarbetande av dofter med olika jobb. Det är också ett lösningsmedel som används vid extraktion av metaller och organiska föreningar såsom ättiksyra.
Isoamiloacetat är resultatet av sterifiering av isoamylalkohol med ättiksyra. I organisk kemi undervisningslaboratorier representerar denna syntes en intressant upplevelse för att implementera förestringarna, samtidigt som laboratoriet översvämmar med banan doft.
[TOC]
Isoamiloacetatstruktur
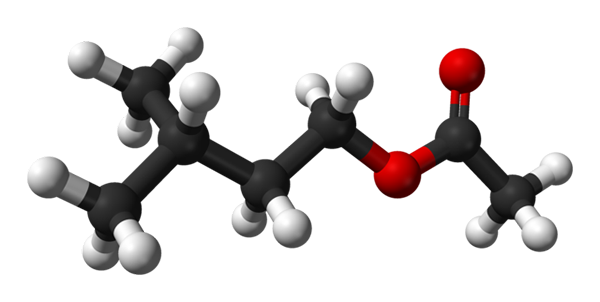 Isoamiloacetatstruktur. Källa: Ben Mills [Public Domain]
Isoamiloacetatstruktur. Källa: Ben Mills [Public Domain] I den övre bilden har du molekylstrukturen i isoamiliska acetatet med hjälp av en sfär- och staplarmodell. De röda sfärerna motsvarar syreatomer, särskilt de som identifierar denna förening som en ester; Dess del av eter, R-O-R och karbonylgruppen, C = O, sedan har den strukturella formeln R'Koor.
Till vänster, r', Du har den isopentila alkygliska radikalen, (Cho3)2Chch2Ch2; Och till höger, r, till metylgruppen, till vilken "acetatet" av namnet på denna ester är skyldig. Det är en relativt liten ester som kan interagera med de kemiska receptorerna för lukten av våra näsor och orsakar signaler som hjärnan tolkar som en doft.
Kan tjäna dig: grenade alkanerIntermolekylär interaktioner
Isoamiliska acetatmolekylen är flexibel; Men den isopentilradikalen gynnar inte intermolekylära interaktioner eftersom den är grenad, och steriskt förhindrar att syreatomer interagerar effektivt av dipol-dipolo-krafter.
Dessa två syre kan inte heller acceptera vätebroar; strukturellt har molekylen inte hur man donerar dem. Inför de avbrutna dipolerna kan isoamilacetat interagera intermolekylärt genom London -spridningskrafter; som är direkt proportionella mot deras molekylmassa.
Således är det molekylmassan hos estern som är ansvarig för dess molekyler för att bilda en vätska med en hög kokpunkt (141 ° C). På samma sätt är det ansvarigt för dess fasta täckning till en temperatur av -78 ° C.
Banan doft
Dess intermolekylära krafter är så svaga att vätskan är tillräckligt flyktig för att genomsyra omgivningen med bananer lukt. Intressant nog kan den söta lukten av denna ester förändras om antalet kol är minskade eller ökade.
Det vill säga, om han istället för att ha sex alifatiska kolhydrater hade fem (med den radikala isobutilen) skulle hans lukt likna hallon; Om radikalen var sekbutilen, skulle lukten laddas med spår av organiska lösningsmedel; Och om jag hade mer än sex kol, skulle lukten börja bli tvål och metallisk.
Egenskaper
Kemiska namn
-Isoamilocetat
-Isopentil etanoat
-3-metylbutiloacetat
-Isopentiloacetat
-Bananolja eller banan.
Molekylär formel
C7H14ANTINGEN2 eller ch3Coo (ch2)2Ch (ch3)2
Molekylvikt
130,187 g/mol.
Fysisk beskrivning
Det är en oljig, klar och färglös vätska.
Lukt
Vid rumstemperatur har den en intensiv och trevlig lukt av banan.
Smak
Den har en smak som liknar den som presenteras av päron och äpple.
Kokpunkt
124,5 ºC.
Smältpunkt
-78,5 ºC.
antändningspunkt
92 ºF Stängd kopp (33 ºC); Kopp öppen 100 ºF (38 ºC).
Kan tjäna dig: kristallina fasta ämnen: struktur, egenskaper, typer, exempelVattenlöslighet
2.000 mg/l a 25 ºC.
Löslighet i organiska lösningsmedel
Belopp med alkohol, eter, etylacetat och amylalkohol.
Densitet
0,876 g/cm3.
Ång-densitet
4.49 (i luftförhållande = 1).
Ångtryck
5,6 mmHg vid 25 ºC.
Självtemperatur
680 ºF (360 ºC).
Gegga
-1,03 CPOISE vid 8,97 ºC
-0,872 CPOISE vid 19,91 ºC.
Förbränningsvärme
8.000 kalk/g.
Lukttröskel
Luft = 0,025 | il/L
Vatten = 0,017 mg/L.
Brytningsindex
1 400 till 20 ° C.
Relativ förångningshastighet
0,42 (i förhållande till butylacetat = 1).
Dialektrisk
4,72 till 20 ºC.
Lagring
Isoamiloacetat är en brandfarlig och flyktig förening. Därför måste det vara kallt i helt hermetiska behållare, långt ifrån brännbara ämnen.
Syntes
Det produceras genom förestring av isoamylalkohol med glacialsyra, i en process som kallas Fishers estterifiering. Svavelsyra används vanligtvis som en katalysator, men också p-toluenosulfonsyra katalyserar reaktionen:
(Ch3)2Ch-ch2-Ch2Ch2Oh + ch3COOH => CH3Cooch2-Ch2-Ch2-Ch (ch3)2
Ansökningar
Mat och dryck smak
Det används för att ge en päronsmak i vatten och sirap. Det används i Kina för att förbereda fruktsmaker, som jordgubbar, björnbär, ananas, päron, äpple, druva och banan. De använda doserna är: 190 mg/kg i konfekt; 120 mg/kg i bakverk; 56 mg/kg i glass; och 28 mg/kg i läskedrycker.
Lösningsmedel och utspädningsmedel
Det är ett lösningsmedel för:
-Nitrocellulosa och celluloid
-Vattentät lack
-Estergummi
-Vinylharts
-Cummarona harts och ricinolja.
Det används som lösningsmedel för krombestämning och används som ett järn-, kobolt- och nickelekstraktionsmedel. Det används också som ett lösningsmedel av oljemålningar och gamla lacker. Dessutom används det vid utarbetandet av nagellack.
Denna ester används som ett utspädningsmedel i ättiksyraproduktion. Olja används som råmaterial i en oxidationsprocess som producerar en vattenhaltig lösning av ättiksyra och andra föreningar, såsom myrsyra och propionsyra.
Kan tjäna dig: etylenglykol: egenskaper, kemisk struktur, användningarSom lösningsmedel och bärare av andra ämnen användes det i början av flygindustrin för att skydda tygerna från luftvingarna.
Doft
-Det används som en atmosfär för att täcka de dåliga luktarna.
-Det används som en parfym i skor.
-För att bevisa effektiviteten hos antigasmasker, eftersom isoamiliska acetat har en mycket låg lukttröskel och är inte särskilt giftig.
-Det används i dofter som chipre; den mjuka aromen Osmanthus; Jacinto; och den starka orientaliska smaken, som används i låga doser, lägre än 1%.
Andra
Det används i utarbetandet av siden och konstgjorda pärlor, fotografiska filmer, vattentäta och bronsande lacker. Det används också inom textilindustrin i färgning och efterbehandling. Det används vid torr tvätt av klädartiklar och tygmöbler.
Dessutom används isoamiloacetat i rayonutarbetning, ett syntetiskt tyg; I penicillin -extraktion och som standardkromatografi substans.
Risker
Isoamiloacetat kan irritera huden och ögonen genom fysisk kontakt. Inandning kan orsaka irritation, hals och lungor. Samtidigt kan exponering för höga koncentrationer orsaka huvudvärk, dåsighet, svindel, yrsel, trötthet och svimning.
Långvarig kontakt med huden kan orsaka torrhet och sprickor.
Referenser
- Bilbrey jenna. (30 juli 2014). Isoamylacetat. Chemistry World av Royal Society of Chemistry. Återhämtat sig från: Chemistryworld.com
- Nationellt centrum för bioteknikinformation. (2019). Isoamylacetat. Pubchemdatabas. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- Wikipedia. (2019). Isoamylacetat. Hämtad från: i.Wikipedia.org
- Royal Society of Chemistry. (2015). Isoamylacetat. Tanka. Återhämtat sig från: chemspider.com
- New Jersey Department of Health and Senior Services. (2005). Isoamylacetat. [Pdf]. Återhämtat sig från: nj.Gov
- Kemisk bok. (2017). Isoamylacetat. Återhämtat sig från: Chemicalbook.com
- « 4 perioder med kemi från förhistorien fram till idag
- Politiska talegenskaper, typer, frågor och exempel »

