Slutna
- 5062
- 793
- Johan Eriksson
Vi förklarar vad som är alkaner, deras egenskaper, nomenklatur, typer och ger flera exempel
Vad är alkanerna?
De Slutna är de enklaste organiska föreningarna som finns. De är mättade alifatiska kolväten, bildade uteslutande av kol och väte, där kol förenas endast med enkla enkla kovalenta bindningar.
De kan vara öppen kedja, i vilket fall har de den allmänna formeln cnH2n+2. De kan också bilda en eller flera cykler, i vilket fall den allmänna formeln förlorar två väten för varje cykel som bildas (CnH2n Om de har en enda cykel, cnH2n-2 Om de har 2, etc.).
Många vanliga organiska föreningar som vi använder varje dag uppnås. Till exempel bildas köksgas och naturgas av en eller flera gasformiga alkaner. Bränslet för bilar (bensin, bensin eller bränsle, beroende på land) består av komplexa blandningar av flytande alkaner, bland vilka de viktigaste är isomererna i oktanen.
Alcean fastigheter
De är väldigt lite reaktiva
Den huvudsakliga kemiska egenskapen eller egenskapen hos alkaner är att de är ganska stabila molekyler som inte deltar i kemiska reaktioner, såvida det inte är i mycket energiska förhållanden som mycket höga temperaturer eller i närvaro av ultravioletta ljus eller fria radikaler.
De är apolära föreningar
Enkla C-C- och C-länkar är apolära kovalenta bindningar, så alkanerna molekyler kan inte ha ett netto dipolmoment. På grund av detta är de apolära molekyler.
De har låga kokning och fusionspunkter
På grund av samma faktum att vara apolär, är de enda krafterna för intermolekylär attraktion som de närvarande alkaos är spridningskrafter som krafterna från van der Waals. Eftersom dessa krafter är mycket svaga är de enkla att bryta för att göra fasta ämnen till vätskor och dessa låga temperaturgaser.
De är mindre täta än vatten
Alkanerna är de minst täta av organiska föreningar, och de är alltid mindre täta än vatten. Av denna anledning flyter de alltid på ytan av vattnet när de två är blandade.
I allmänhet är de färglösa
Gasformiga och flytande alkaner är färglösa och genomskinliga. Men när de stelnade bildar de vita ogenomskinliga amorfa fasta ämnen, som i fallet med vissa paraffiner och vissa plast.
De är inte vattenlösliga
Den gyllene regeln för löslighet är att liknande upplöses till sådana. Vatten är ett polärt lösningsmedel medan alla alkaner är helt apolära, så de är inte lösliga i vatten.
Kan tjäna dig: diasteromererDe är lösliga i apolära organiska lösningsmedel
Med samma tidigare argument är alkanerna lösliga i apolära lösningsmedel som bensen eller cyklohexan. Faktum är att flytande alkaner är en del av apolära organiska lösningsmedel.
De kan inte drabbas av tilläggsreaktioner
Att vara mättade kolväten kan alkaner inte drabbas av tilläggsreaktioner. Det enda undantaget är cyklopropanen som har en ring på endast tre medlemmar som är mycket spännande och lätt kan brytas.
De är bränslen
En av de få kemiska reaktionerna där alkanerna deltar är i förbränning, och det är just den huvudsakliga användningen som ges till dem.
Typer av alkaner
Beroende på anslutningen mellan kolatomer kan alkaner vara:
- Linjär
- Grenad
- Cykliska (cykloalcanos)
- Bicyl- eller polycykliska toces
- Spiranos
Linjära alkaner
De är de enklaste alkanerna och därför av alla organiska föreningar. Alla har molekylformel cnH2n+2 Och de kännetecknas av att ha en enda kedja av kolatomer kopplade till varandra efter den andra.
Förvirrade alkaner
De har också allmän formel cnH2n+2 Men till skillnad från linjära alkaner är kedjan av kolatomer grenad åtminstone vid en punkt. De grenade alkanerna är kedjeisomerer av linjära alkaner, eftersom de bara skiljer sig åt i den ordning som kolatomer är kopplade.
Cykloalkaner
I cykloalcanos förenas ändarna på kedjan av linjära alkaner för att bilda en cyklisk kedja. För att bilda denna ytterligare C-C-bindning är det nödvändigt att eliminera ett väte från varje terminal kol, så den allmänna formeln för dessa föreningar är CnH2n. Den minsta möjliga cykeln är den av tre kolatomer som kallas cyklopropan (c3H6).
Liksom de öppna kedjan alkaner som kan ha förgreningar kan cykloalcan också presentera substituentgrupper i form av öppna kedjor.
Bicyl- och polycykliska till
Det finns många cykliska Toum där två eller flera cykler delar två eller flera kolatomer. Dessa föreningar kallas polis. Polisens molekylformel beror på hur många cykler strukturen.
I det enklaste fallet, cyklar, är formeln cnH2n-2 Eftersom ett par hydrogener måste gå förlorade för att stänga varje cykel. För polis med mer än två sammanslagna cykler kommer formeln att vara lika med alkaner mindre ett par hydrogener för varje bildad cykel.
Kan tjäna dig: hydraceSpiranos
Spiranials är en speciell klass av cyklar där de två cyklerna bara delar en kolatom. I dessa fall är de två cyklerna i vinkelräta plan med varandra, så strukturen ses som om en av cyklerna roterades med avseende på den andra.
Alkaners nomenklatur
Nomenklatur av linjära alkaner
Nomenklaturen hos alkaner och i själva verket den av alla organiska föreningar är baserad på nomenklaturen hos linjära alkaner. Dessa heter helt enkelt enligt antalet kolatomer i kedjan.
De första fyra får vanliga namn som är metan, Ethan.) Till slutet av Alcano.
Antal kol | Molekylär formel | Halvutvecklad formel | namn |
1 | Ch4 | Ch4 | Metan |
2 | C2h6 | Ch3ch3 | Etano |
3 | C3H8 | CH3CH2CH3 | Propan |
4 | C4h10 | CH3 (CH2) 2CH3 | Butan |
5 | C5H12 | CH3 (CH2) 3CH3 | Pentano |
6 | C6H14 | CH3 (CH2) 4CH3 | Hexan |
7 | C7H16 | CH3 (CH2) 5CH3 | Heptano |
8 | C8H18 | CH3 (CH2) 6CH3 | Oktan |
9 | C9H20 | CH3 (CH2) 7CH3 | Nonano |
10 | C10H22 | CH3 (CH2) 8CH3 | Dekanus |
Nomenklatur av grenade alkal
De grenade alkanerna heter på namnet på linjära alkaner. Processen innebär att du väljer en av de möjliga kolkedjorna som huvudkedjan och resten av konsekvenserna kvarstår som substituentgrupper.
Processen består av följande steg:
Steg 1: Identifiera huvudkedjan.
Valet görs enligt följande kriterier i prioriteringsordning:
- Den längsta kedjan väljs.
- Om det finns mer än en, väljs de flesta konsekvenserna från dem.
- Vid mer än en som har samma längd och samma antal förgreningar, det som, när du numrerar den, ger den minsta möjliga lokaliseringskombinationen väljs.
- Om två eller flera kedjor har samma längd, har samma antal förgreningar och alla samma lokaliseringar, de som tilldelar minderåriga lokaler till de förgreningar som visas först i alfabetisk ordning.
- Om allt ovan är detsamma, kan vem som helst väljas.
Huvudkedjan ger huvudnamnet till alkanen, som om det var en linjär alkan.
Det kan tjäna dig: kaliumnitrit (KNO2): Struktur, egenskaper och användningarSteg 2: Numrera huvudkedjan.
Kolatomer i huvudkedjan i följd från ena änden till en annan måste listas efter dessa regler:
- Den numrering som tilldelats av den lägsta kombinationen av lokaler till konsekvenserna väljs.
- Om de två siffrorna ger samma kombination av lokaler, väljs det som tilldelas av minderåriga lokaler till de konsekvenser som visas först i den alfabetiska ordningen.
- I händelse av att båda är desamma, spelar det ingen roll vilken som är vald.
Steg 3: Namnge förgreningarna och beställa dem alfabetiskt.
Förgreningarna kallas radikaler och ersätter _ano för motsvarande linjär alkan vid _ilo -änden.
Antal kol | Radikal alkyl | namn |
1 | -Ch3 | Radikal metyl |
2 | -Ch2ch3 | "Etyl |
3 | -CH2CH2CH3 | "Propy |
4 | -CH2 (CH2) 2CH3 | "Butyl |
5 | -CH2 (CH2) 3CH3 | "Pentilo |
6 | -CH2 (CH2) 4CH3 | "Hexilo |
7 | -CH2 (CH2) 5CH3 | "Heptyl |
8 | -CH2 (CH2) 6CH3 | "Octilo |
9 | -CH2 (CH2) 7CH3 | "Nonilo |
10 | -CH2 (CH2) 8CH3 | "Decil |
Steg 4: Namnet på föreningen är byggd.
Namnet är byggt genom att namnge alla konsekvenser i alfabetisk ordning (undertrycker den slutliga "O" -brevet), föregått av dess lokalisering, följt av namnet på huvudkedjan.
Om någon gren upprepas placeras lokaler för var och en, åtskilda av komma, och lägg prefixet som indikerar hur det upprepas för 2, TRI för 3, och så vidare) föregås av grenen, och så vidare).
Exempel:
Namnge följande grenade alkan:

Steg 1: Val av huvudkedjan.
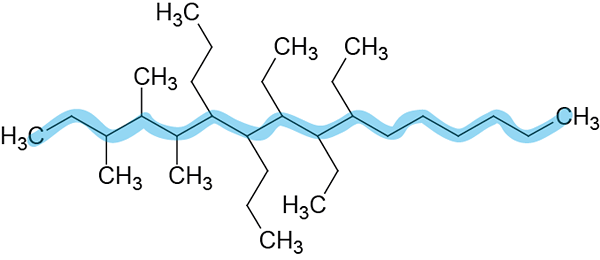
Denna kedja har 16 kol, så huvudkedjan kommer att kallas Hexadecano.
Steg 2: Numrering av huvudkedjan.
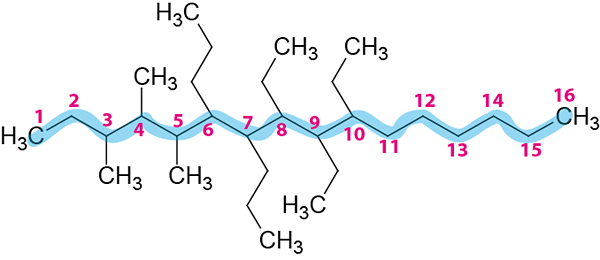
Det är numrerat från vänster till höger eftersom de ger de mindre lokaliseringarna.
Steg 3: Namnge alla förgreningar.
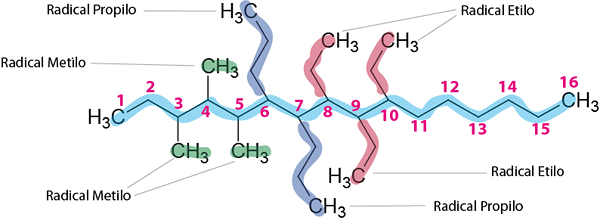
Det finns tre etylradikaler, tre metylradikaler och två propylradikaler.
Steg 4: Bygg namnet
Namnet på föreningen kommer att vara:
8,9,10-trietil-3,4,5-trimetyl-6,7-dipropilhexadecano
Exempel på alkaner
I följande tabell presenteras några ytterligare exempel på alkaner.
namn | Molekylformel eller struktur | Radikal | Antal kol |
Metan | Ch4 | Metyl | 1 |
Etano | C2h6 | Etyl | 2 |
Propan | C3H8 | N-propil | 3 |
N-butan | C4h10 | N Blight | 4 |
Isobutan | C4h10 | Isobutil | 4 |
Nopan | C5H12 | Nepentil | 5 |
Isopentano | C5H12 | Isopentil | 5 |
Neopentano | C5H12 | Neopentilo | 5 |
N-hexan | C6H14 | N-hexyl | 6 |
Polyetylen | CH3 (CH2) NCH3 | ---- | > 100 |
Cyklopentano | C5h10 | Cyklopentil | 5 |
Cyklohexan | C6H12 | Cyklohexil | 5 |

