Alkyn
- 1199
- 276
- Lars Eriksson
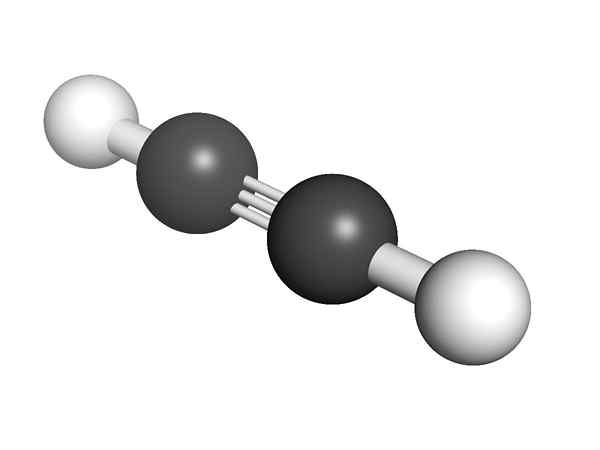
 Alvento -strukturen, med en trippellänk
Alvento -strukturen, med en trippellänk Vad är alkines?
De Alkyn De är kolväten eller organiska föreningar som i sina strukturer finns i en trippellänk mellan två kolhydrater. Denna trippellänk (≡) anses vara en funktionell grupp när man representerar en aktiv plats för molekylen och är därför ansvarig för deras reaktivitet.
Även om alkynar inte skiljer sig mycket från alko eller alkener, uppvisar de större surhet och polaritet på grund av deras länkar. Den exakta termen för att beskriva denna lilla skillnad är vad som kallas omöjlighet.
Alkanerna är mättade kolväten, medan alkinerna är de mest omättade med avseende på den ursprungliga strukturen. Vad betyder det här? Att en alkan h3C-ch3 (etan) kan vara dehydrogen till h2C = ch2 (eten) och därefter HC≡CH (Etino, eller bättre känd som acetylen).
Observera hur ytterligare länkar bildas bland kolen minskar antalet hydrogener som är kopplade till dem. Kol, på grund av dess elektroniska egenskaper, försöker bilda fyra enkla länkar, så desto större tendens att reagera (med undantag för aromatiska föreningar).
Å andra sidan är trippellänken mycket starkare än den dubbla (=) eller den enkla (-) bindningen, men till en hög energikostnad. Därför kan de flesta kolväten (alkaner och alkener) bilda trippelbindningar vid höga temperaturer.
Som en följd av dessa höga energier, när de bryter släpper de mycket heta. Ett exempel på detta fenomen kan ses när acetylenförbränningar med syre och den intensiva värmen från flamman för att svetsa eller smälta metaller används.
Acetylen är den enklaste och mest lilla alkynen av alla. Andra kolväten kan uttryckas från deras kemiska formel genom att ersätta H med alquiliska grupper (RC≡CR '). Detsamma händer i världen av organisk syntes genom ett stort antal reaktioner.
Denna alkyn uppstår från reaktionen av kalciumoxid hos kalksten och koque, råmaterial som tillhandahåller de nödvändiga kolen inuti en elektrisk ugn:
Cao + 3c => cac2 + Co
CAC2 Det är kalciumkarbid, en oorganisk förening som äntligen reagerar med vatten för att bilda acetylen:
Cac2 + 2h2O => ca (OH)2 + Hc≡Ch
Alkines fysiska och kemiska egenskaper
Polaritet
Triple Link skiljer alkiner från alkaner och alkener. De tre typerna av kolväten är apolära, olösliga i vatten och mycket svaga syror. Emellertid är elektronegativiteten hos de dubbla och trippelbindningskolorna större än för enkla kolhydrater.
Enligt detta. Av denna anledning, var är C≡C eller C = C -länkarna kommer att finnas större elektronisk densitet än i resten av det kolsyrade skelettet. Som en följd av detta finns det ett litet dipolmoment där molekylerna interagerar med dipol-dipolo-krafter.
Dessa interaktioner är mycket svaga om deras dipolmoment jämförs med vattenmolekylens eller någon alkohol. Detta återspeglas i deras fysiska egenskaper: Alkines har i allmänhet högre fusions- och kokpunkter jämfört med deras mindre omättade kolväten.
Kan tjäna dig: de sju viktigaste biokemi -applikationernaPå samma sätt, på grund av deras låga polaritet, är de mindre olösliga i vatten, men lösliga i apolära organiska lösningsmedel, såsom bensen.
Aciditet
Denna elektronegativitet orsakar också väte Hc≡CR är surare än någon som finns i andra kolväten. Därför är alkiner arter mer sura än alkener och mycket mer än alkaner. Emellertid förblir dess surhet föraktlig om den jämförs med karboxylsyror.
Eftersom alkiner är mycket svaga syror reagerar de bara med mycket starka baser, till exempel natrium amiduro:
HC≡CR + NANH2 => HC≡CNA + NH3
Från denna reaktion erhålls en lösning av natriumacetyl, råmaterial för syntes av andra alkyner.
Alquinos reaktivitet
Alkynes reaktivitet förklaras genom tillsats av små molekyler till deras trippellänk, vilket minskar dess omättnad. Dessa kan vara vätemolekyler, vätehallogenider, vatten eller halogener.
Hydrering
Den lilla H -molekylen2 Det är mycket svårfångat och snabbt, så att öka chansen att läggas till trippellänken till alkinerna.
Dessa är vanligtvis metaller (Pd, Pt, RH eller Ni) fint uppdelade för att öka ytan; Och på detta sätt, kontakten mellan väte och Alquino:
RC≡CR ' + 2H2 => Rch2Ch2R '
Resultatet är att väte är "ankare" till kol som bryter en bindning, och så vidare tills motsvarande alkan producerar, RCH2Ch2R '. Detta mättar inte bara det initiala kolvätet, utan modifierar också dess molekylstruktur.
Tillsats av vätehalogenuros
Här tillsätts den oorganiska molekylen HX, där X kan vara någon av halogenerna (F, CL, BR eller I):
Rc≡Cr ' + hx => rch = cxr'
Hydrering
Hydrering av alkiner är när de lägger till en vattenmolekyl för att bilda en aldehyd eller en keton:
RC≡CR ' + H2O => rch2Cor '
Om r 'är en h, är det en aldehyd; Om det är en hyra är det en Cetona. I reaktionen bildas en förening som kallas enol (rch = c (OH) r ') som en mellanhand.
Detta lider av en omvandling av den enoliska formen (C-OH) till keton (C = O) i en balans som kallas tautomerisering.
Tillsats av halogener
Och med avseende på tillägg kan de diatomiska molekylerna av halogener också förankras till kol (x x2= F2, Kli2, Bras2 Jag hörde2):
RC≡CR ' + 2x2 => Rcx2-Cx2R '
Acetylenalkylering
Från natriumacetylyrlösningen kan andra alkiner framställas genom att använda en hyreshalogenid:
HC≡CNA + RX => HC≡CR + NAX
Till exempel, om det var metyljodiden, skulle den resulterande alkynen vara:
HC≡CNA + CH3I => hc≡CCH3 + Nax
HC≡CCH3 är rätt, även känd som Metylacetylen.
Alkines kemisk struktur
 Alquino kemisk struktur
Alquino kemisk struktur Vad är strukturen på alkynen? I den övre bilden visas en acetylenmolekyl. Den linjära geometrien för C≡C -länken kan vara tydlig från den.
Därför, där det finns en trippelbindning, måste molekylens struktur vara linjär. Detta är en annan av de anmärkningsvärda skillnaderna mellan dem och resten av kolväten.
Det kan tjäna dig: Cycopropane (C3H6)Alkanerna representeras vanligtvis som sicksackar, eftersom de har SP -hybridisering3 och deras länkar är separerade 109º. De är faktiskt en kovalent förenad tetrahedra -kedja. Medan alkener är platta genom SP -hybridisering2 av dess kol, bildar mer specifikt ett trigonalt plan med separerade länkar med 120º.
I alkyner är orbital hybridisering SP, det vill säga de har 50% av A och 50% av en P. Det finns två SP -hybridorbitaler som är kopplade till H -atomer i acetylen- eller alkyngrupper i alkinerna.
Avståndet både H eller R är 180º, utöver det faktum att de rena kolbanor inte på detta sätt kan bilda trippelbindningen. Av denna anledning är länken -c≡C- linjär. Ser strukturen för alla molekyler -c≡C -höjdpunkterna i de regioner där skelettet är mycket linjärt.
Avstånd från länkar och terminalalms
Kolbindningar i trippelbindningen är på ett mindre avstånd än i dubbel eller den enkla länken. Med andra ord är C≡C kortare än C = C och det C-C. Som ett resultat är länken starkare eftersom de två π -länkarna bidrar till att stabilisera den enkla länken σ.
Om trippelbindningen är i slutet av en kedja, är det en terminal alkyne. Därför måste formeln för nämnda förening vara HC≡CR, där H kommenterar slutet eller starten av kedjan.
Om det tvärtom är en trippel intern länk är formeln rc≡Cr ', där r och r' är höger och vänster sida av kedjan.
Alquinos nomenklatur
Hur utses alkiner enligt reglerna som dikteras av IUPAC? På samma sätt som Alquenos och Alkenes har utsetts. För att göra detta ändras suffixet -ano eller -eno för suffixet -ino.
Till exempel: HC≡CCH3 Det utses tips, eftersom det har tre kol, till exempel propan (Cho3Ch2Ch3). HC≡CCH2Ch3 Det är 1-butino, som är en terminal alkyne. Men i fallet med Cho3Conom3 Detta är 2-butino, och i detta är trippellänken inte terminal utan intern.
Ch3Conom2Ch2(Ch3)2 Det är 5-metyl-2-hexin. Kolbockar börjar från sidan närmast trippellänken.
En annan typ av alkiner är cykloalquinerna. För dem räcker det för att ersätta suffixet -ano av -ino av motsvarande cykloalcan. Således kallas cyklopropanen som har en trippelbindning som cyklopropin (som inte finns).
När det finns två trippellänkar läggs prefixet DI till namnet-. Det har som exempel till HC≡C-C≡H, diacetylen eller propadin; Och till HC≡C-C-C≡H, Butadiino.
Alquinos användning
Acetylen eller etino
Den minsta av alkynerna förtjockar det möjliga antalet användningsområden för dessa kolväten. Från det genom alk kan andra organiska föreningar syntetiseras. Det genomgår också oxidativa reaktioner för att erhålla etanol, ättiksyra, akrylsyra, bland andra.
Kan tjäna dig: litiumhydrid: struktur, egenskaper, erhållning, användningAndra av dess användningsområden består i att tillhandahålla värmekällan för att locka elektronerna av atomer; mer specifik, E av metallkatjoner i bestämningar genom atomabsorptionsemission, allmänt använt spektroskopisk teknik.
Naturalkines
De enda befintliga metoderna för att förbereda alkyner är inte bara syntetiska eller med värmeapplikation i frånvaro av syre, utan också biologiska.
I dessa enzymer som kallas acetylisk, som kan förneka en dubbelbindning. Tack vare detta uppnås många naturliga källor till alkyner.
Efter detta kan dessa källor extraheras gifter, motgift, läkemedel eller någon annan förening som ger någon fördel; särskilt när det gäller hälsa. Alternativen är många när de modifierar sina ursprungliga strukturer och har dem som stöd för nya alkiner.
Exempel på alkyner
Hittills har många exempel på alkiner nämnts. Vissa kommer emellertid från mycket specifika källor eller har särskilda molekylstrukturer: de är polyacetyle.
Detta innebär att det kan finnas mer än en trippellänk som är en del av en mycket stor struktur, och inte bara av en enkel kolsyrad kedja.
Taririnsyra
 Garnstruktur
Garnstruktur Taririnsyra kommer från en växt belägen i Guatemala som heter Picramnia Tariri. Det är specifikt extraherat från oljan från dess frön.
I sin molekylstruktur kan en enda trippellänk observeras som skiljer en apolär svans från ett polärt huvud; Därför kan det betraktas som en amfipatisk molekyl.
Histrionikotoxin
 Histrionicotoxinstruktur
Histrionicotoxinstruktur Histrionicotoxin är ett gift segregerat av huden på invånare i Colombia, Brasilien och andra latinamerikanska länder. Den har två trippelkonjugerade länkar med en dubbelbindning. Båda är terminaler och separeras med en sexkolring och en cyklisk amin.
Cicutoxin
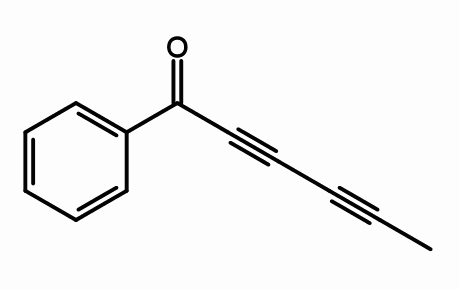 Cicutoxinstruktur. Av Giorgiogp2 [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0) eller GFDL (http: // www.gnu.Org/copyleft/fdl.html)], från Wikimedia Commons
Cicutoxinstruktur. Av Giorgiogp2 [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0) eller GFDL (http: // www.gnu.Org/copyleft/fdl.html)], från Wikimedia Commons Från molekylstrukturen i cicutoxin, var är trippelförbindelserna? Om dubbelbindningarna är platta, som de ses rätt, och de enkla bindningarna är tetraedraler, som i ändarna, är tripplarna linjära och är i sluttningen (\).
Denna förening består av ett neurotoxin som huvudsakligen finns i den vattenlevande läkningsanläggningen.
Kapill
 Capillina struktur. Av Klever [CC0], från Wikimedia Commons
Capillina struktur. Av Klever [CC0], från Wikimedia Commons Det är en alkyn som finns i den eteriska oljan från Artemis -växter som används som ett svampdödande medel. Två trippel på varandra följande länkar kan observeras, mer korrekt konjugerade.
Vad betyder det? Att trippelbindningarna resonerar längs hela kolkedjan och innebär att dubbelbindningen C = O öppnas för C-O-.
Pargilin
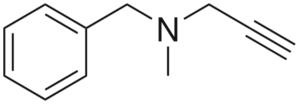 Pargilin
Pargilin Det är en Alty med antihypertensiv aktivitet. Att analysera dess struktur i delar är: en Benchilo -grupp till vänster, en tertiär amin i mitten och en höger -wing; det vill säga en terminalfastighetsgrupp.
Referenser
- Francis A. Sköldpaddsskal. Organisk kemi. Karboxylsyror. (sjätte upplagan., Sida 368-397). MC Graw Hill.
- Brennan, John. (10 mars 2018). Exempel på alkyner. Forskning. Taget från: forskning.com
- Byju. (2018). Trippelbindning i alkyner. Taget från: byjuus.com
- Encyclopedia of Exempel (2017). Alkyn. Återhämtat sig från: exempel.co
- Kevin a. Baudreaux. Alkyn. Taget från: Angelo.Edu
- Robert C. Neuman, jr. Alkener och alkyner. [Pdf]. Taget från: Chem.Ucr.Edu

