Berylliumhistoria, struktur, egenskaper, användningar

- 1612
- 433
- Johan Eriksson
han beryllium Det är ett metalliskt element som tillhör grupp 2 eller IIA i det periodiska tabellen. Det är den mest ljusa alkaliska metallen i gruppen och representeras av BE -symbolen. Dess atom och katjon är också mindre än de av deras kamrater (Mg, CA, MR ...).
På grund av dess ovanliga belastningstäthet förekommer denna metall vanligtvis inte isolerat. De vet cirka 30 mineraler som innehåller det, bland vilka är: berylen (3beo · al2ANTINGEN3· 62· 2h2O), Bertrandita (4beo.2se2.2h2O), El Chrisoberilo (Beal2ANTINGEN4) och Fenaquita (vara2Ja4).
 Metallisk beryllpipitas. Källa: W. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]
Metallisk beryllpipitas. Källa: W. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)] La Esmeralda, en ädelsten, är en variant av berylen. Pure Beryllium är emellertid inte så slående; Det ser blek gråaktig ljusstyrka (överlägsen bild) och har uppnåtts i form av pepitas eller dragees.
Beryllium har en uppsättning karakteristiska fysiska egenskaper. Den har låg densitet; högt termiskt och elektriskt beteende, såväl som dess termiska kapacitet och värmeavledning; Det är inte en magnetisk metall; och har också en lämplig kombination av styvhet och elasticitet.
Alla dessa egenskaper har lett till att beryllium är en metall med många applikationer, allt från dess användning i kopparlegeringar för utarbetande av verktyg, till dess användning i raketer, flygplan, bilar, kärnreaktorer, röntgenutrustning, resonans kärnmagnet, etc. .
Beryllium har 10 kända isotoper, allt från 5Vara en 14Vara, vara 9Vara den enda stallen. Det är också en mycket giftig metall, som särskilt påverkar andningssystemet, så det finns en begränsning i dess användning.
[TOC]
Historik om din upptäckt
Beryllium upptäcktes av Louis-Nicolas Vauguelin 1798 som ett sammansättningselement i Berilo Mineral, och ett aluminium- och berylliumsilikat.
Därefter lyckades den tyska kemisten Frederic Wöhler 1828 isolera beryllium genom att reagera kalium med berylliumklorid i en platina potten.
Samtidigt, och självständigt, uppnådde den franska kemisten Antoine Bussy också isoleringen av Beryllium. Wöhler var den första som föreslog namnet Beryllium för metall.
Han fick sitt nuvarande namn under året 1957, eftersom han tidigare var känd som glucinium, på grund av den söta smaken av vissa salter. Men för att undvika förvirring med andra söta smakföreningar, och med en växt som heter Glucina beslutades det att ändra namnet på Beryllium.
Berily struktur
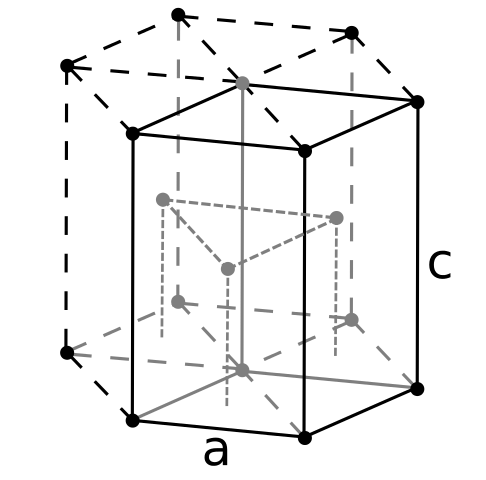 Berily cign struktur. Källa: Användare: Dornelf [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]
Berily cign struktur. Källa: Användare: Dornelf [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)] Som beryl den lättaste av alkalinoteriska metaller, bör det förväntas att volymen på dess atomer kommer att vara den minsta av alla. Berylil -atomer interagerar med varandra genom den metalliska bindningen, så att deras "hav av elektroner" och avvisningar mellan kärnmodellen den resulterande glasstrukturen.
Det kan tjäna dig: Periódic Acid (HIO4): Vad är, struktur, egenskaper, användningarDe svarta kristallerna i beryllium bildas sedan. Dessa kristaller har en hexagonal struktur (överlägsen bild), där var och en har sex sidogrannar, och tre andra i topp- och ner -planen.
Att vara svarta kristaller är det användbart. Detta är en av de mest kompakta strukturerna som en metall kan anta; Och det är meningsfullt att de så små atomerna av "Squeeze" båda för att undvika den minsta mängden tomhet eller antal hål mellan dem.
Elektronisk konfiguration
1s22s2
Vad är lika med 4 elektroner, varav 2 är från Valencia. Om en elektron till 2p -omloppet främjas kommer två SP HBíbridos -orbitaler att ha. Således kan det i berylliumföreningar finnas linjära geometrier, x-be-x; Till exempel den isolerade BECL -molekylen2, Cl-cl.
Egenskaper
Fysisk beskrivning
Fast grå, ljus och spröd färg.
Smältpunkt
1287 ºC.
Kokpunkt
2471 ºC.
Densitet
- 1 848 g/cm3 vid rumstemperatur.
- 1,69 g/cm3 till smältpunkten (flytande tillstånd).
Atomradio
232.
Radiokovalent
21.00.
Atomvolym
5 cm3/mol.
Specifik värme
1,824 J/g · mol vid 20 ºC.
Fusionsvärme
12,21 kJ/mol.
Förångningsvärme
309 kJ/mol.
Elektronnegativitet
1.57 på Pauling -skalan.
Standardpotential
1,70 V.
Ljudhastighet
12.890 m/s.
Termisk expansion
11,3 um/m · K vid 25 ° C.
Värmeledningsförmåga
200 W/m · K.
Kemiska egenskaper
Beryllium är täckt med ett lager beryloxid (Beeo) som fungerar som luftskydd vid rumstemperatur. Oxidationen av beryllium förekommer vid temperaturer större än 1000 ° C, som härstammar som berylliumoxid och beryllium nitridprodukter.
Det är också resistent mot verkan av salpetersyra 15 m. Men det löses i saltsyra och alkalier, såsom natriumhydroxid.
Ansökningar
Förberedelse av verktyg
Beryllium bildar legeringar med koppar, nickel och alumino. I synnerhet producerar legeringen med kopparverktyg med stor hårdhet och motstånd och utgör endast 2% av legeringens vikt.
Dessa verktyg producerar inte gnistor när man träffar järnet, vilket gör det möjligt för dem att användas i miljöer med ett högt innehåll av brännbara gaser.
Kan tjäna dig: termisk: struktur, egenskaper, bildning, exempelPå grund av sin låga densitet har den en lätt vikt, som tillsammans med sin styvhet tillåter dess användning i rymdflygplan, raketer, missiler och flygplan. Legeringen med beryllium har använts vid utarbetandet av bildelar. Det har också använts i Springs -utarbetande.
På grund av den stora hårdheten som beryllium tilldelas till dess legeringar har dessa använts i bromsarna av militära flygplan.
Speglar utarbetande
Beryllium har använts vid produktion av speglar på grund av dess dimensionella stabilitet och dess förmåga att ha en hög pulter. Dessa speglar används i satelliter och brandkontrollsystem. Dessutom används rymdteleskop.
I joniserande strålning
Beryllium är ett element med låg densitet, så det kan anses vara transparent till x -strålar. Denna funktion tillåter dess användning i konstruktionen av fönstren i rören som producerar röntgen, industriell applikation och medicinsk diagnos.
På samma sätt används Beryllium i fönstren för radioaktiva utsläppsdetektorer.
I magnetismgenererande lag
Bland egenskaperna hos beryllium är inte ett magnetiskt element. Detta gör det möjligt att användas vid konstruktion av artiklar med magnetisk resonansutrustning, där magnetfält med stor intensitet genereras, vilket minimerar alla störningar.
Kärnreaktorer
På grund av sin höga fusionspunkt har den hittat tillämpning i kärnreaktorer och keramik. Beryllium används som en kärnreaktioner moderator och som neutronproducent:
9Vara + 4Han (α) => 12C +n (neutron)
Det uppskattas att för en miljon berylatomer som bombas med a -partiklar förekommer upp till 30 miljoner neutroner. Precis denna kärnreaktion tillät upptäckten av neutronen.
James Chadwick bombarderade berylliumatomer med a -partiklar (HE). Forskaren observerade frisläppandet av subátomiska partiklar, utan elektrisk laddning, vilket ledde till upptäckten av neutroner.
Metallskydd
Lägg till en mängd beryllium på ytan av metaller som kan oxideras, ger ett visst skydd. Till exempel reduceras brandfarligheten hos magnesium och ljusstyrkan hos silverlegeringar förlängs.
Var ligger det?
Berylen finns i pegmatiten, associerad med glimmer, fältspat och kvarts. Genom användning av en flotationsteknik är det möjligt att separera en blandning av beryl och fältspat. Därefter koncentreras fältspat och beryl och utsätts för en behandling med kalciumhypoklorit.
Det kan tjäna dig: Skillnader mellan organiska och oorganiska föreningarFöljt av en behandling med svavelsyra och kaliumsulfonat, genom utspädning, uppnås berylflotationen och skiljer den från fältspat.
Berylen behandlas med natriumfluorosylikat och soda vid 770 ° C för att bilda natriumfluoroberilat, aluminiumoxid och kiseldioxid. Därefter utfälls berylliumhydroxiden i natriumhydroxidhydroxidfluorroberillösningen.
Berylliumfluorid bildas genom att reagera berylhydroxid med ammoniacal vätefluorid, vilket producerar ammonium ammonium. Detta värms upp för att bilda berylliumfluorid, som behandlas med varmt magnesium för att isolera beryllium.
Risker
Beryllium som fint uppdelad metall, i form av lösningar, torrt damm eller rök, är mycket giftigt och kan producera dermatit. Den största toxiciteten produceras dock genom inandning.
Ursprungligen kan beryllium inducera överkänslighet eller allergi, som kan bli bellios eller kronisk sjukdom i beryllium (CBD). Detta är en allvarlig sjukdom, kännetecknad av en minskning av lungkapaciteten.
Akut sjukdom är sällsynt. Vid kronisk sjukdom finns det farulombildning i hela kroppen, särskilt i lungorna. Kronisk bellios orsakar progressiv dyspné, hosta och allmän svaghet (asteni).
Akut bellios kan vara dödlig. I bellios inträffar den progressiva förlusten av andningsfunktion, eftersom det finns hinder i flödet av luftvägar i luftvägarna och minskad syresättning av blodtrycket.
Referenser
- Royal Society of Chemistry. (2019). Beryllium. Återhämtat sig från: rsc.org
- Nationellt centrum för bioteknikinformation. (2019). Beryllium. Pubchemdatabas. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- Helmestine, Anne Marie, PH.D. (15 mars 2019). Beryllium fakta. Återhämtat sig från: tankco.com
- Wikipedia. (2019). Beryllium. Hämtad från: i.Wikipedia.org
- Lentech B. V. (2019). Beryllium-be. Återhämtat sig från: Lentech.com
- Bolagsmaterial. (2019). Lär dig mer om elementet Beryllium återhämtat sig från: Beryllium.com
- D. Michaud. (12 april 2016). Berylliumbehandling och extraktionsproblem. 911 Metallurgist. Återhämtat sig från: 911Metallurgist.com
- Timothy P. Hanusa. (5 januari 2016). Beryllium. Encyclopædia Britannica. Återhämtat sig från: Britannica.com
- Läs S. Ny man. (2014). Berylliumsjukdom. MSD -manual. Återhämtat sig från: msdmanuals.com
- « Idrottspsykologi historia, mål och profiler
- Social globalisering Social dimension, fördelar och exempel »

