Kaliumnatriumpumpstruktur, funktion, mekanism, betydelse
- 5007
- 247
- Lars Eriksson
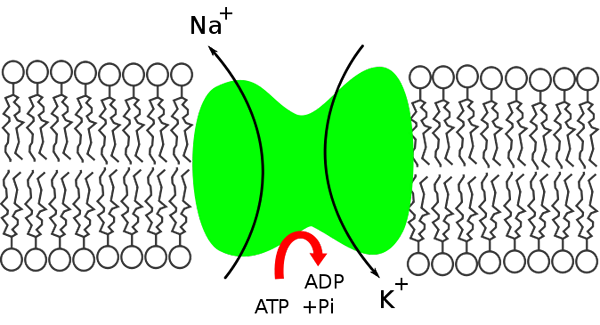
De Kaliumnatriumbombe Det är en proteinstruktur som ingår i en bredare uppsättning molekyler som finns i många cellmembran, och som är ansvariga för aktiv transport av joner eller andra små molekyler mot dess koncentrationsgradienter. De använder den energi som frigörs genom ATP -hydrolys och det är därför de kallas generiskt.
Kalium -natriumpumpen är en Na+/K+ATPAY eftersom den frigör energin i ATP -molekylen för att flytta natrium inuti cellen och introducerar samtidigt kaliumkalium.
 Kalium natriumbombsystem. Yttre och inre av cellen. (Källa: Miguelferig, via Wikimedia Commons)
Kalium natriumbombsystem. Yttre och inre av cellen. (Källa: Miguelferig, via Wikimedia Commons) Inuti cellen är natrium mindre koncentrerad (12 mEq/L) än utanför (142 mEq/L), medan kalium är mer koncentrerad utanför (4 mEq/L) än inuti (140 mEq/L).
Atasas -bomber klassificeras i tre stora grupper:
- Joniska pumpar av typ F och V: De är ganska komplexa strukturer, de kan bestå av 3 olika typer av transmarketunderenheter och upp till 5 associerade polypeptider i cytosol. De fungerar som protontransportörer.
- ABC Superfamily (av engelska TILLTp-BIndikering CAssette = ATP Union Cassette): Integrerad av mer än 100 proteiner som kan fungera som jontransportörer, monosackarider, polysackarider, polypeptider och till och med andra proteiner.
- Joniska pumpar i klass P: bildas av minst en transmembraal alpha katalytisk underenhet som har en facklig plats för ATP och en mindre ß -underenhet. Under transportprocessen är α -underenheten fosforyila och därmed namnet "P".
Kalium -natrium (Na+/K+Atpasa) -bomben tillhör den joniska pumpgruppen av klass P och upptäcktes 1957 av Jens Skou, en dansk forskare, när han studerade mekanismen för anestesi i nerverna i en krabba (Carcinus maenas); arbete som Nobelpriset i kemi tilldelades 1997.
 Kaliumnatriumbombe. Nakpompe2.JPG: Phi-Gastrein på Cold.Wikipedierarivativ arbete: Sonia/CC BY-S (http: // Creativecommons.Org/licenser/BY-SA/3.0/)
Kaliumnatriumbombe. Nakpompe2.JPG: Phi-Gastrein på Cold.Wikipedierarivativ arbete: Sonia/CC BY-S (http: // Creativecommons.Org/licenser/BY-SA/3.0/) [TOC]
Kaliumnatriumpumpstruktur
Kalium -natriumpumpen är ett enzym som från dess kvartära struktur bildas av 2 ALFA (α) proteinsubenheter och två betatyp (ß).
Det är därför en tetramer av a2p2, vars underenheter är omfattande membranproteiner, det vill säga de korsar lipid -tvåskiktet och har både intra och extra cytosoliska domäner.
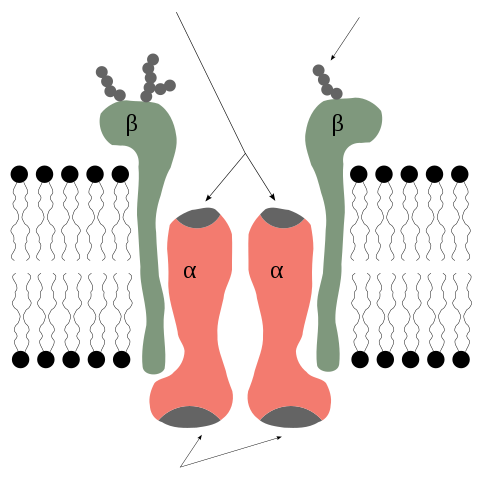 Alfa- och betasubenheter på kaliumpumpen. Rob Cowie/CC BY-SA (http: // Creativecommons.Org/licenser/BY-SA/3.0/)
Alfa- och betasubenheter på kaliumpumpen. Rob Cowie/CC BY-SA (http: // Creativecommons.Org/licenser/BY-SA/3.0/) Alfa -subunities
A -underenheterna är de som innehåller unionsplatserna för ATP och för Na+ och K+ -jonerna och representerar den katalytiska komponenten i enzymet och den som utövar själva bombens funktion.
A-underenheterna är polypeptider i stor storlek, med en molekylvikt av 120 kDa, 10 transmembranala segment och med deras N-och C-terminala ändar belägna på cytosoliska sidan.
De har på de intracellulära sidoföreningsplatserna för ATP och för Na+, såväl som en aspartatrest i position 376 som representerar platsen som lidit av fosforyleringsprocessen under aktiveringen av pumpen.
Bindningsstället för K+ är tydligen på den extracellulära sidan.
Beta -underenheter
Ss -underenheterna verkar inte ha ett direkt deltagande i pumpfunktionen, men i deras frånvaro nämns inte funktion.
P -subenheterna har en molekylvikt på cirka 55 kDa vardera och är glykoproteiner med en enda transmarknadsdomän vars glukidavfall sätts in i det extracellulära regionen.
Kan tjäna dig: Basalblad: Egenskaper, histologi och funktionerDe verkar vara nödvändiga i endoplasmatisk retikulum, där de skulle bidra till korrekt vikning av a -underenheterna, och sedan, på membranets nivå, för att stabilisera komplexet.
Båda typerna av underenheter är heterogena och har beskrivits hittills a1, a2 och a3 -isoformer för UNA och ß1, β2 och ß3 för den andra. A1 finns i membranen i de flesta celler, medan a2 är närvarande i muskler, hjärta, fettvävnad och hjärna och a3 i hjärta och hjärna.
P1 -isoformen är den mest diffusa fördelningen, även om den är frånvarande i vissa vävnader såsom vestibulära celler i det inre örat och de snabba svarglykolytiska muskelcellerna. Den senare innehåller endast β2.
De olika strukturerna i underenheterna som utgör Na+/K+ -pumpen i de olika vävnaderna kan följa specialiseringar av en funktionell typ men ändå klargjorda.
Kaliumpumpfunktion
Under när som helst beaktas plasmamembranet en separationsgräns mellan motsvarande fack till det inre av en cell och den som representerar den extracellulära vätskan i vilken den är nedsänkt.
Båda facken har en sammansättning som kan vara kvalitativt annorlunda, eftersom inuti cellerna finns ämnen som inte är ute av dem och den extracellulära vätskan innehåller ämnen som inte finns intracellulärt.
Ämnen som finns i båda facken finns i olika koncentrationer, och dessa skillnader kan ha en fysiologisk betydelse. Så är fallet med många joner.
Homeostasunderhåll
Na+/K+ -pumpen uppfyller en grundläggande funktion i upprätthållandet av intracellulär homeostas genom att kontrollera natrium- och kaliumjonkoncentrationer. Detta underhåll av homeostas uppnår det tack vare:
- Jontransport: introducerar natriumjoner och utvisar kaliumjoner, process genom vilka den också främjar rörelse av andra molekyler genom andra transportörer som beror antingen på den elektriska laddningen eller den inre koncentrationen av dessa joner.
- Cellvolymkontroll: Introduktionen eller utgången från joner innebär också att denentre vattenrörelser i cellen, så pumpen deltar i cellvolymkontroll.
- Membranpotentialgenerering: Utvisning av 3 natriumjoner för varje 2 kaliumjoner som introduceras orsakar membranet. Denna skillnad kallas vilopotential.
Na+ har en extracellulär koncentration på cirka 142 mekv/l, medan dess intracellulära koncentration endast är 12 mekv/l; K+, å andra sidan, är mer koncentrerad i cellen (140 mEq/L) än utanför den (4 meq/l).
Även om den elektriska laddningen för dessa joner inte tillåter deras passage genom membranet, finns det jonkanaler som tillåter den (selektivt), som gynnar rörelsen om de krafter som vanligtvis rör sig dessa joner också finns närvarande.
Kan tjäna dig: membranreceptorer: funktioner, typer, hur de fungerarNu har dessa koncentrationsskillnader stor betydelse i bevarande av homeostas av organismen och måste upprätthållas i en slags balans som skulle gå förlorad.
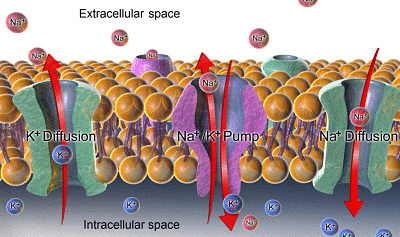 Spridning och kaliumnatrium (källa: Bruceblaus. När du använder den här bilden i externa källor kan det citeras som: Blausen.Com Staff (2014). "Medical Gallery of Blausen Medical 2014". Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.010. ISSN 2002-4436.Derivat av Mikael Hägström/CC av (https: // Creativecommons.Org/licenser/av/3.0) via Wikimedia Commons)
Spridning och kaliumnatrium (källa: Bruceblaus. När du använder den här bilden i externa källor kan det citeras som: Blausen.Com Staff (2014). "Medical Gallery of Blausen Medical 2014". Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.010. ISSN 2002-4436.Derivat av Mikael Hägström/CC av (https: // Creativecommons.Org/licenser/av/3.0) via Wikimedia Commons) - Koncentrationsskillnaden för Na+ mellan interiören och utanför cellen skapar en kemisk lutning som skjuter natriumet inåt och gör att denna jon ständigt kommer in och behandlar för att sprida den skillnaden, det vill säga för att matcha koncentrationerna i båda sidor.
- Kaliumgradienten upprätthålls i motsatt riktning, det vill säga inifrån och ut, vilket tillåter jonens konstant utgång och dess inre reduktion och externa ökning.
Funktionen för Na+/K+ -pumpen tillåter extraktion av natrium som har angetts genom diffusion genom kanaler eller med andra transportvägar och återinförande av kalium som har spridits utåt, vilket möjliggör bevarande av intra och extracellulära koncentrationer av dessa joner.
Mekanism (process)
Verkningsmekanismen för ATPase Na+/K+ består av en katalytisk cykel som innebär överföring av reaktioner från en fosforylgrupp (PI) och konformationella förändringar av enzymet som går från ett tillstånd E1 till ett E2 -tillstånd och vice versa.
Operationen kräver närvaro av ATP och Na+ inuti cellen och K+ i den extracellulära vätskan.
Förening av natriumjoner till transportören
Cykeln börjar i tillståndet för konformation E1 i enzymet, i vilket det finns 3 cytosoliska platser för Na+ -förening och hög affinitet (km på 0,6 mM) som är helt ockuperade eftersom intakoncentrationen av jonen (12 mM) tillåter den.
ATP -hydrolys
I detta tillstånd (E1) och med Na+ fixat på sina unionsplatser är ATP fixerad till dess ställe i den cytosoliska sektorn av molekylen, en fosfatgrupp till 376 Aspartat överförs och överförs, och bildar en högenergicilfosfat som inducerar En konformationell förändring till staten E2.
Utvisning av 3 natriumjoner och introduktion av 2 kaliumjoner
Den konformationella förändringen till E2 -tillståndet innebär att Na+ -föreningsplatserna passerar till utomlands, deras affinitet för jonen minskar mycket och frigörs i den extracellulära vätskan, medan samtidigt affiniteten för unionsplatserna till K+ ökar Och dessa joner binder till pumpen.
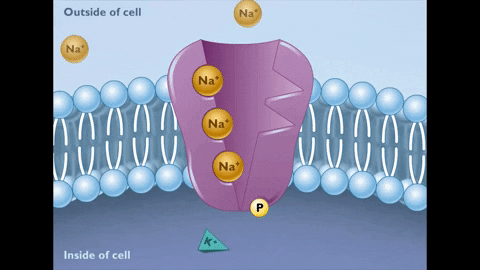 Under tillståndet E2 släpps jonerna av Na+ på andra sidan membranet.
Under tillståndet E2 släpps jonerna av Na+ på andra sidan membranet. 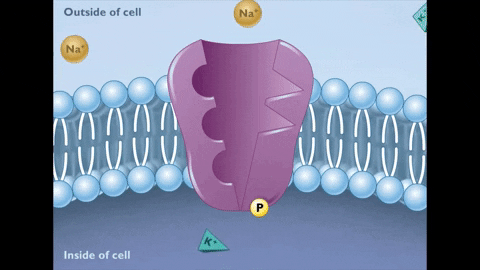 I sin tur genererar detta nya tillstånd av pumpen affinitet för föreningen av kjoner+
I sin tur genererar detta nya tillstånd av pumpen affinitet för föreningen av kjoner+ Reversering från E2 till E1
När Na+ har frisatts och K+ är förenad, produceras hydrolysen av aspartylfosfatet och konformationell förändring av E2 -tillståndet till tillståndet E1 vänds, med återinförandet av unionsplatserna för den tomma Na+ och de för K+ ockuperade till staten.
När denna förändring inträffar förlorar platserna för Na+ sin affinitet och de av K+ förlorar den, med vilken K+ släpps inuti cellen.
Betydelse
Vid underhåll av cell osmolaritet
Na+/K+ -bomben har varit närvarande i de flesta, om inte i alla, däggdjursceller, där det är av allmän betydelse genom att bidra till att upprätthålla dess osmolaritet och därför dess volym.
Kan tjäna dig: peroxidaser: struktur, funktioner och typerDen kontinuerliga inledningen av natriumjoner i cellen är att konditionera en ökning av det intracellulära antalet osmotiskt aktiva partiklar, vilket inducerar vatteninmatning och ökningen i volym som skulle hamna orsakar brottet i membranet och cellkollapset.
Vid bildandet av membranpotentialen
Eftersom dessa pumpar bara introducerar 2 K+ för varje 3 Na+ de tar ut, uppför de sig elektrogeniskt, vilket innebär att de "dekompenserar" interna elektriska laddningar, vilket gynnar produktionen av den karakteristiska membranpotentialen hos kroppsceller.
Dess betydelse är också tydlig i relation till cellerna som utgör de exciterbara vävnaderna, där handlingspotentialerna kännetecknas av inträde av Na+-jonen, som depolariserar cellen, och utgången från K+, som ompolariserar den.
Dessa joniska rörelser är möjliga tack vare driften av Na+/K+-pumpar, vilket bidrar till produktionen av kemiska gradienter som flyttar de involverade jonerna.
Utan dessa pumpar, som fungerar i motsatt riktning, skulle koncentrationsgradienterna för dessa joner spridas och den exciterande aktiviteten skulle försvinna.
I njurfunktion
En annan aspekt som belyser den extrema betydelsen av natriumpotassiumbomber är i förhållande till njurfunktion, vilket inte skulle vara omöjligt.
Njurfunktionen innebär den dagliga filtreringen av mer eller mindre 180 liter plasma och stora mängder ämnen, av vilka några måste utsöndras, men många måste reabsorberas så att de inte går förlorade i urinen.
Resorptionen av natrium, vatten och många av de filtrerade ämnena beror på dessa pumpar, som är belägna i det basolaterala membranet i cellerna som utgör epitelet för de olika rörformiga segmenten av njurnefronerna.
Epitelcellerna som upprättar njurrören har ett ansikte som är i kontakt med tubulens ljus och som kallas det apikala ansiktet och en annan som är i kontakt med interstitium runt tubuli och kallas basolateral.
Vattnet och de ämnen som är reabsorb måste först passera in i cellens inre genom apikalen och sedan till mellanstödet av basolateralt.
Reabsorptionen av Na+ är nyckeln både i förhållande till honom och i förhållande till vatten och den för andra ämnen som beror på hans. Den apikala inträdet av Na+ cellen kräver att det finns en lutning som rör den och som innebär en mycket låg koncentration av jonen inuti cellen.
Denna låga intracellulära koncentration av Na+ produceras av natriumpumpar från det basolaterala membranet som fungerar intensivt för att ta bort jonen från cellerna till interstitium.
Referenser
- Ganong WF: Den allmänna och cellulära grunden för medicinsk fysiologi, i: Granskning av medicinsk fysiologi, 25: e upplagan. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JI: Ämnetransport över cellmembranet, i: Lärobok för medicinsk fysiologi, 13: e upplagan, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J: Transport över cellerna membran, i: Molecular and Cell Biology, 4th ed.
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger principer för biokemi. Macmillan.
- Alberts, b., Bray, D., Hopkin, K., Johnson, A. D., Lewis, J., Raff, m.,... & Walter, s. (2013). Essential Cell Biology. Kransvetenskap.
- « Soma -egenskaper delar och funktioner
- Mayates (cotinis mutabilis) egenskaper, livsmiljö, reproduktion »

