Carbocation Formation, Egenskaper, typer, stabilitet
- 841
- 209
- Anders Larsson
En karbokation, Som namnet antyder är det en organisk jon som har en positivt laddad kolatom, som kännetecknas av att vara mycket instabil, existerande under en kort tid. Det är vanligtvis en mellanhand i organiska reaktioner, det vill säga det härstammar som oumbärliga steg i respektive molekylmekanismer.
Historiskt har det varit konfliktpunkter i komprimering av vad Carbocation är. Detta beror på att det finns symfiner med reaktiva molekyler som av någon eller annan anledning skaffar en positiv belastning i en av deras kolhydrater. Klassisk Carbocation, så att säga, är en som kan representeras av bildens allmänna formel nedan.
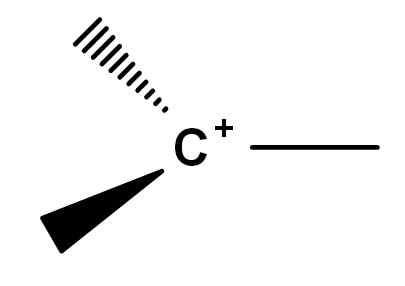 Allmän formel för en Carbocation. Källa: Gabriel Bolívar.
Allmän formel för en Carbocation. Källa: Gabriel Bolívar. Notera hur den positiva belastningen är belägen exakt på kolatomen och saknar också en länk. Därför är Carbococation dåliga elektroner, detta är orsaken till dess höga reaktivitet.
Anta att metan, Cho4. Om kol förlorade en av sina väteatomer, skulle vi eliminera en av de fyra C-H-bindningarna. Då har metylkarbokokationen sitt ursprung, Ch3+, som vi kunde representera bara genom att placera väteatomerna i ändarna av ränderna i den övre formeln. Ch3+ Det är det enklaste av alla Carbocations.
[TOC]
Träning
Hur bildas Carbocations? Svaret finns i reaktionsmekanismer. Emellertid är den stora majoriteten i gemensamt en av följande två aspekter:
-Heterolytisk brott
-Tillsats av elektroner π till en elektrofil
Heterolytisk brott
I det heterolitiska brottet C-G-bindningen, G är vilken atom eller grupp som. Till exempel:
Kan tjäna dig: arsenik: historia, struktur, egenskaper, användningar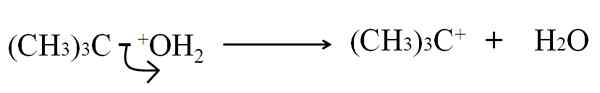 Heterolytiskt brott i tertbutanoluttorkning. Källa: Gabriel Bolívar.
Heterolytiskt brott i tertbutanoluttorkning. Källa: Gabriel Bolívar. Nu kan denna paus ges för flera metoder, som i sin tur kommer att förändra mekanismen och reaktionen som övervägs.
Tillsats av elektroner π till en elektrofil
Den andra processen genom vilken en Carbocation bildas, som är mycket vanlig i aromatiska alkener och föreningar, är genom att attackera elektroner av en dubbelbindning till en elektrofil. De vanligaste fallen är hydreringen av alkener genom verkan av en syra:
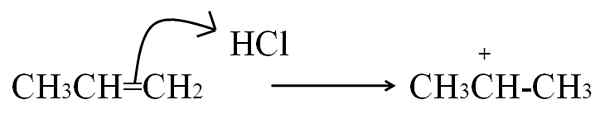 HCL -reaktion med propeno för att bilda en Carbocation som mellanhand. Källa: Gabriel Bolívar.
HCL -reaktion med propeno för att bilda en Carbocation som mellanhand. Källa: Gabriel Bolívar. Denna ekvation motsvarar bildandet av Carbocation, som det är en mellanhand, Inte en produkt. Dubbelbindningselektronerna attackerar HCL -väte, elektrofilen. Väte tillsätts till kolet till höger om dubbelbindningen, så gruppen bildas3, Medan kolet till vänster får den positiva belastningen.
Egenskaper
Hybridisering
Den allmänna formeln som presenterades i början avslöjar en trigonal platt geometri runt kolatomen. Detta beror på att hybridiseringen lidit av kolatomiska orbitaler för att bli hybrid sporbitaler2, som är separerade i en vinkel på 120º. Även om det inte är representerat har Carbocation en orbital p Ren och tom, kapabel att acceptera elektroner.
Aciditet
Carbocation är en sur art, antingen enligt definitionen av Brönsted eller Lewis. Deras positiva laddning kräver elektroner eller väteatomer som ges. Det är av denna anledning som carbocations inte kan bildas i mycket grundläggande media, eftersom de omedelbart skulle reagera för att komma från andra produkter.
Stabilitet
Hybridiseringen sp2 av Carbocation gör det sårbart för attacker av rika arter i elektroner. Denna funktion accentueras ytterligare av dess stora surhet. Följaktligen är Carbococation en mycket reaktiv art, som knappast bildas och snart (i fråga om nanosekunder) reagerar för att ge upphov till den verkliga produkten från den kemiska reaktionen.
Kan tjäna dig: sulfaminsyra: struktur, egenskaper, syntes, användningTyper av Carbocations
Det finns flera typer av Carbocations. Dessa kan dock klassificeras enligt följande:
-Primär
-Sekundär
-Tertiär
-Aromatisk eller arillos
-Vinyl och alilisk
Primär
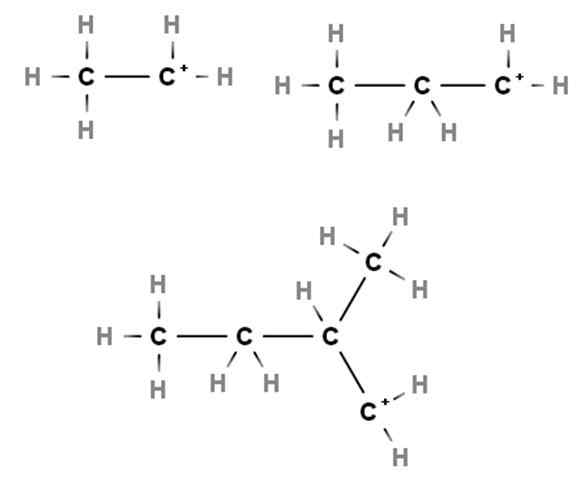 Primär carboces. Källa: Gabriel Bolívar via Molview.
Primär carboces. Källa: Gabriel Bolívar via Molview. Ankomster visar exempel på primära karbokaer. De kallas det eftersom den positiva belastningen ligger i ett primärt kol, 1: a, så det är bara kopplat till en kolatom. Etano, ch3Ch3, När en h förlorar något av sina ändar, Carbocation Cho3Ch2+ antingen +Ch2Ch3.
Sekundär
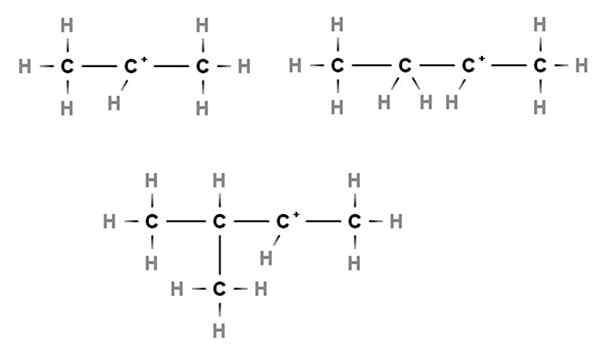 Sekundär carbocations. Källa: Gabriel Bolívar via Molview.
Sekundär carbocations. Källa: Gabriel Bolívar via Molview. I sekundära Carbocations är den positiva belastningen belägen i ett sekundärt kol, 2: a, som är kopplat till två kolatomer. Till exempel, om propan, cho3Ch2Ch3, Vi tar bort en H av det centrala kolet, vi kommer att ha Carbocation Cho3Ch2+Ch3.
Tertiär
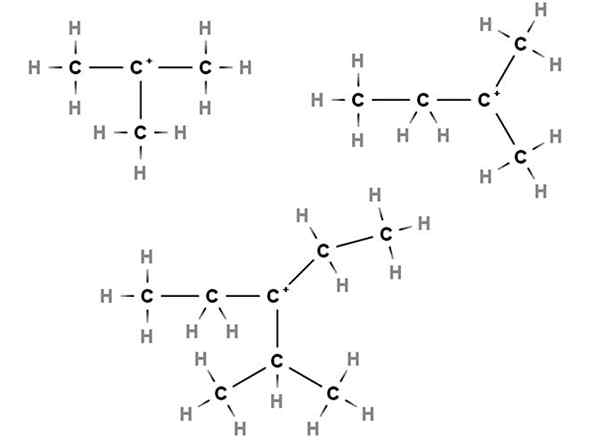 Tertiär carboces. Källa: Gabriel Bolívar via Molview.
Tertiär carboces. Källa: Gabriel Bolívar via Molview. I tertiära carbocations är den positiva belastningen belägen i ett tertiärt kol, 3: e, kopplade till tre kolatomer. Observera att till skillnad från de två första typerna av Carbocations saknar de väteatomer.
Således har vi metylpropan eller isobutan, ch (Ch (välj3)3, Som genom att förlora ett väte bildar det centrala kolet Carbocation +C (ch3)3.
Aromatisk
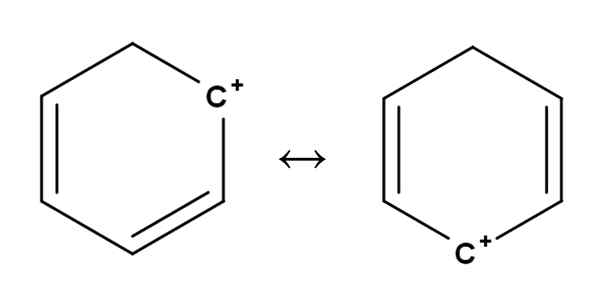 Bensen carbocat. Källa: Gabriel Bolívar.
Bensen carbocat. Källa: Gabriel Bolívar. Aromatiska eller aromatiska Carbocations är kanske de mest speciella av alla. Din träning är mycket lik den som beskrivs för alkener i det första avsnittet.
I dem är den positiva belastningen i princip belägen i en av kolen av en aromatisk ring, såsom bensen. Den positiva belastningen är emellertid inte fixerad, men är spridd i andra ringpositioner genom resonans.
Det kan tjäna dig: Ribulosa-1,5-bifosfat (RUBP): Egenskaper, CarbolixationSå här passerar den positiva belastningen, som ses ovan, från ett kol till en annan inuti bensenringen. Denna egenskap ger denna Carbococation stor stabilitet mot de andra typerna av Carbocations.
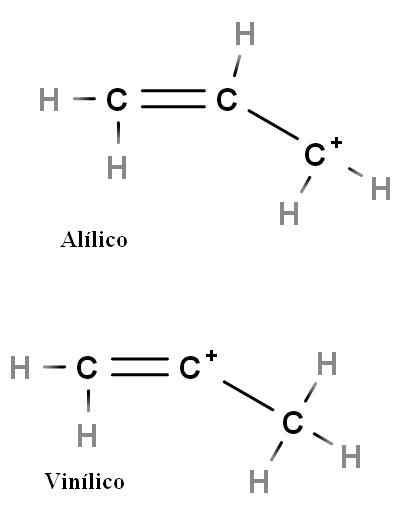
Allylisk och vinyl
 Allyl- och vinylkarbokok. Källa: Gabriel Bolívar.
Allyl- och vinylkarbokok. Källa: Gabriel Bolívar. Andra speciella typer av Carbocations är aliliska och vinyl. Skillnaden mellan dem (ovan) är positionen för den positiva laddningen relaterad till dubbelbindning.
I vinylkarbokt finns den positiva belastningen i en av dubbelbindningskolhydrater; När den är i allyisk kolhydrater är den positiva belastningen belägen i kolet efter dubbelbindningen. Det räcker för att ersätta hydrogener med andra grupper och vi kommer att ha en enorm familj av allyiska och vinylkarbokationer.
Relativ stabilitet
Genom att veta vilka som är de viktigaste typerna av carbocations kan de beställas baserat på deras relativa stabilitet:
Vinyl < Primario < Secundario < Alílico < Terciario < Aromático
Nu kan det finnas allic carbocations som är mer stabila än en specifik tertiär. Allt beror på deras substituenter.
Varför denna stabilitet? Till molekylens förmåga att sprida eller minska den positiva belastningen av Carbocation. För att göra detta behöver du nära atomer som ger en del av dess elektroniska Carbocation Density genom hyperkonjugering. Under tiden uppnås detta i alumiska och aromatiska Carbocations genom resonans.
När det gäller vinylkarbokering är den positiva belastningen på ett kol som redan var SP2, vilket gör det väldigt instabilt.
Referenser
- Graham solomons t.W., Craig b. Fryhle. (2011). Organisk kemi. (10th Utgåva.). Wiley Plus.
- Carey f. (2008). Organisk kemi. (Sjätte upplagan). MC Graw Hill.
- Morrison och Boyd. (1987). Organisk kemi. (Femte upplagan). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Karbokation. Hämtad från: i.Wikipedia.org
- James Ashenhurst. (20 februari 2020). 3 faktorer som stabiliserar Carbocations. Återhämtat från: Masterorganicchemistry.com
- Clark Jim. (2000). Carbocations (eller karbonjoner). Återhämtat sig från: Chemguide.co.Storbritannien
- Doktor. Kennepohl, prof. S. Bonde & t. Soderberg. (10 augusti 2020). Carbocation Structure and Stability. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- « Miljöetiska koderkoncept, egenskaper och exempel
- Årets fyra stationer i Mexiko och dess egenskaper »

