Carnot -cykelsteg, applikationer, exempel, övningar
- 2954
- 673
- Anders Larsson
han Karnotcykel Det är sekvensen av termodynamiska processer som äger rum i en Carnot -motor, en idealisk enhet som endast består av reversibla processer; det vill säga de som, som har ägt rum, kan återvända till det ursprungliga tillståndet.
Denna typ av motor anses vara idealisk, eftersom den saknar spridning, friktion eller viskositet som uppstår i verkliga maskiner och förvandlar den termiska energin till användbart arbete, även om omvandlingen inte genomförs 100%.
 Figur 1. En ånglok. Källa: Pixabay
Figur 1. En ånglok. Källa: Pixabay En motor byggs baserat på ett ämne som kan göra arbete, till exempel gas, bensin eller ånga. Detta ämne är föremål för olika temperaturförändringar och upplever i sin tur variationer i dess tryck och volym. På detta sätt är det möjligt att flytta en kolv inuti en cylinder.
[TOC]
Vad är Carnot -cykeln?
Carnot -cykeln sker inom ett system som kallas Carnot eller C -motor, som är en idealisk gas som är låst i en cylinder och försedd med en kolv, som är i kontakt med två källor vid olika temperaturer1 och t2 Som den som visas i följande figur till vänster.
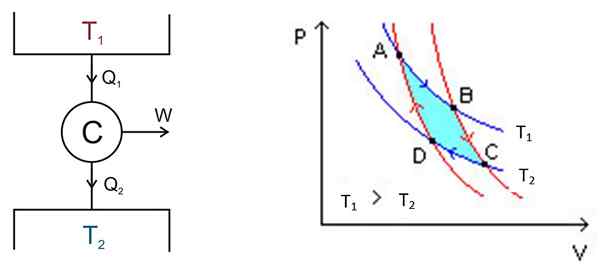 figur 2. Till vänster ett schema för C -arnotmaskinen, till höger PV -diagram. Källa till vänster figur: keta - eget arbete, cc av 2.5, https: // commons.Wikimedia.org/w/index.Php?Curid = 681753, höger figur Wikimedia Commons.
figur 2. Till vänster ett schema för C -arnotmaskinen, till höger PV -diagram. Källa till vänster figur: keta - eget arbete, cc av 2.5, https: // commons.Wikimedia.org/w/index.Php?Curid = 681753, höger figur Wikimedia Commons. Det finns följande processer i ett grovt läge:
- En viss mängd värme levereras till enheteningång = Q1 Från den termiska tanken vid hög temperatur t1.
- Carnot C -motorn utför ett arbete W tack vare denna värme som levereras.
- En del av värmen som används: avfallet Qutgång, Den överförs till termisk tank som är vid en lägre temperatur t2.
Carnot -cykelsteg
Analysen görs med ett P -V -diagram (tryck -volym), som visas i figur 2 (höger figur). Motorns mål kan vara att hålla termisk insättning 2 kallt och extrahera värme från den. I detta fall är det en Kylmedelsmaskin. Om du tvärtom vill ge värme till den termiska insättningen 1 är det en Värmepump.
P -V -diagrammet visar tryckförändringar - motortemperatur under två förhållanden:
- Bibehålla den ständiga temperaturen (isotermisk process).
- Ingen värmeöverföring (värmeisolering).
De två isotermiska processerna måste anslutas, vilket uppnås med hjälp av termisk isolering.
Punkt
Du kan börja när som helst i cykeln, där gas har vissa tryck-, volym- och temperaturförhållanden. Gasen lider av en serie processer och kan återgå till startförhållandena för att starta en annan cykel, och alltid är den slutliga inre energin densamma som den första. Eftersom energi bevaras:
Arbete utförd av C = ingångsvärme - Avgångsvärme
ΔW = qingång - Qutgång
Området som ingår i denna cykel eller slinga, i turkos i figuren, är lika exakt med det arbete som gjorts av Carnot -motorn.
Punkter A, B, C och D är markerade i figur 2. Det börjar med punkten att följa den blå pilen.
Första steget: isotermisk expansion
Temperaturen mellan punkterna A och B är t1. Systemet absorberar värme från termisk insättning 1 och lider av en isotermisk expansion. Då ökar volymen och trycket minskar.
Temperaturen förblir dock i T1, Sedan när gasen expanderar svalnar den. Därför förblir dess inre energi konstant.
Det kan tjäna dig: Graff Van Generator: Fester, hur det fungerar, applikationerAndra steg: adiabatisk expansion
Vid punkt B börjar systemet en ny expansion där systemet inte vinner eller tappar värmen. Detta uppnås genom att sätta det i kalorisolering som anges tidigare. Därför är det en adiabatisk expansion som fortsätter att peka C efter den röda pilen. Volymen ökar och trycket minskar tills det når sitt lägsta värde.
Tredje steg: isotermisk kompression
Börja vid punkt C och slut i D. Isoleringen tas bort och systemet kommer i kontakt med termisk insättning 2, vars temperatur t2 Det är mindre. Systemet ger avfallsvärme till termisk tank, trycket börjar öka och volymen för att minska.
Fjärde steget: adiabatisk komprimering
Nås till punkt D, systemet går tillbaka till termisk isolering, trycket ökar och volymen minskar tills de når de ursprungliga förhållandena för punkten a. Sedan upprepas cykeln igen.
Carnots teorem
Carnots teorem postulerades först i början av 1800 -talet av den franska fysikern Sadi Carnot. Under året 1824 publicerade Carnot, som var en del av den franska armén, en bok där han föreslog svaret på följande fråga: Under vilka förhållanden en termisk maskin har maximal effektivitet? Carnot etablerade sedan följande:
Ingen termisk motor som kör mellan två termiska avlagringar är effektivare än Carnot -motorn.
Ηutbytet av en termisk motor ges med förhållandet mellan det utförda arbetet W och den absorberade värmen Q:
prestanda = arbete gjort/värme absorberad
På detta sätt är prestandan för alla termiska motorer I: η = w/q. Medan prestandan för en Carnot R -motor är η '= W/Q', i fallet med båda motorerna kan de utföra samma jobb.
Carnots sats säger att η aldrig är större än η '. Annars faller det i motsats till den andra lagen om termodynamik, enligt vilken en process där resultatet är att värme från en kropp av lägre temperatur är omöjligt att gå till en annan av högre temperatur utan att få extern hjälp. Därför:
η < η'
Carnots teoremdemonstration
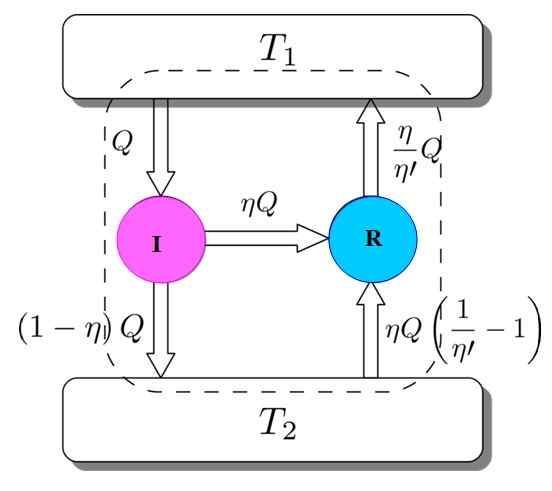
För att visa att detta är så, tänk på Carnot -motorn som fungerar som en kylmaskin som drivs av en I -motor. Detta är möjligt eftersom Carnot -motorn fungerar med reversibla processer, som anges i början.
 Figur 3. Carnots teoremdemonstration. Källa: Netheril96 [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]
Figur 3. Carnots teoremdemonstration. Källa: Netheril96 [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)] Du har båda: Jag och R som arbetar med samma termiska avlagringar och det kommer att antas att η > η'. Om en motsägelse på vägen uppnås med den andra lagen om termodynamik, demonstreras Carnots sats genom reduktion till absurditet.
Figur 3 hjälper till att följa processen. I -motorn tar en mängd värme q, som delar sig på detta sätt: att göra arbete på r motsvarande w = ηq och resten är värmen som överförs (1 -η) q till den termiska tanken t2.
Eftersom energin bevaras uppfylls allt:
OCHingång = Q = arbete w + värme tilldelad t2 = ηq + (1 -η) q = eutgång
Nu tar Carnot R -kylmaskinen termisk tank 2 En mängd värme som ges av:
Det kan tjäna dig: Imantation: Vad består, metod och exempel(η / η ') (1 -η') Q =
Energi måste också hållas i detta fall:
OCHingång = ηq + (η / η ') (1 -η') Q = (η / η ') Q = Q' = Eutgång
Resultatet är överföringen till termisk tank t2 av en mängd värme som ges av (η / η ') Q = Q'.
Om η är större än η 'betyder det att den högsta termiska insättningen har kommit mer värme än jag tog ursprungligen. Eftersom inget externt medel, till exempel en annan termisk källa, har deltagit, är det enda sättet det kan hända att den kallaste termiska insättningen ger värmen.
Detta håller inte med den andra lagen om termodynamik. Det dras slutsatsen att det inte är möjligt att η' Vara mindre än η, därför kan I -motorn inte ha mer prestanda än Carnot R -maskinen.
Satsporoll och begränsningar
Carnot Theorem Corollary säger att två Carnot -maskiner har samma effektivitet om båda arbetar med samma termiska avlagringar.
Det betyder att ämnet inte spelar någon roll, föreställningen är oberoende och inte kan höjas genom att ändra den.
Slutsatsen av den tidigare analysen är att Carnot -cykeln är toppen av den idealiska termodynamiska processen. I praktiken finns det många faktorer som minskar effektiviteten, till exempel det faktum att isolering aldrig är perfekt och i adiabatiska stadier finns det faktiskt kaloriutbyte med utsidan.
När det gäller en bil värms motorblocket. Å andra sidan uppför sig inte gas- och luftblandningen exakt som en idealisk gas, vilket är utgångspunkten för Carnot -cykeln. Detta för att bara nämna några faktorer som kommer att orsaka en drastisk prestationsminskning.
Exempel
En kolv inuti en cylinder
Om systemet är en kolv som är låst i en cylinder som i figur 4 stiger kolven under den isotermiska expansionen, vilket kan ses i det första schemat i extrema vänster och stiger också under den adiabatiska expansionen.
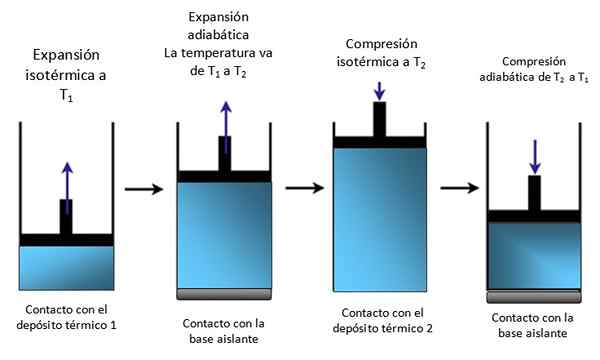 Figur 4. Rörelse av en kolv inuti en cylinder. Källa: Självgjord.
Figur 4. Rörelse av en kolv inuti en cylinder. Källa: Självgjord. Sedan isotermiskt komprimerad, ger värme och fortsätter att komprimera adiabatiskt. Resultatet är en rörelse där kolven stiger och ner i cylindern och kan överföras till andra delar av en viss enhet, till exempel en bilmotor, som producerar ett par eller en ångande maskin.
Olika reversibla processer
Förutom utvidgningen och komprimeringen av en idealisk gas inuti en cylinder finns det andra idealiska reversibla processer som en Carnot -cykel kan konfigureras, till exempel:
- Rundturrörelser i frånvaro av friktion.
- En idealisk fjäder som komprimeras och dekomprimeras och som aldrig deformeras.
- Elektriska kretsar där det inte finns något motstånd som sprider energi.
- Magnetiserings- och avmagnetiseringscykler där det inte finns några förluster.
- Laddar och laddar ner ett batteri.
Ett kärnkraftverk
Även om det är ett mycket komplext system, är en första metod för vad som krävs för att producera energi i kärnreaktor den som följer:
- En termisk källa, bestående av ett material som sönderdelas radioaktivt som uran.
Kan tjäna dig: aktuell atommodell- Diskbänken eller den kalla termiska insättningen som skulle vara atmosfären.
- "Carnot Machine" som använder en vätska, nästan alltid rinnande vatten, som tillförs värme från den termiska källan för att förvandla den till ånga.
När cykeln genomförs erhålls el som ett nätarbete. När det förvandlas till hög temperaturång, nås vatten till en turbin, där energi omvandlas till rörelse eller kinetisk energi.
Turbinen aktiverar i sin tur en elektrisk generator som förvandlar energin i dess rörelse till elektricitet. Förutom fisteningmaterial som uran kan naturligtvis fossila bränslen användas som värmekälla.
Löst övningar
-Exempel 1: Effektivitet för en termisk maskin
Effektiviteten för en termisk maskin definieras som förhållandet mellan utgångsarbetet och ingångsarbetet och är därför en dimensionslös mängd:
Maximal effektivitet = (qingång - Q utgång) /Qingång
Betecknar maximal effektivitet som Emax, Det är möjligt att visa sitt temperaturberoende, som är den enklaste variabeln att mäta, till exempel:
ochmax = 1 - (T2/T1)
Där t2 Det är temperaturen på handfat och t1 Det är den termiska källtemperaturen. Eftersom den senare är större visar sig effektiviteten alltid vara mindre än 1.
Anta att en termisk maskin kan arbeta på följande sätt: a) mellan 200 K och 400 K, B) mellan 600 K och 400 K. Vad är effektiviteten i båda fallen?
Lösning
a) I första fallet är effektiviteten:
ochMax1 = 1 - (200/400) = 0.femtio
b) För det andra läget kommer effektiviteten att vara:
ochMax2 = 1- (400/600) = 0.33
Även om temperaturskillnaden är densamma mellan båda lägena, är effektiviteten inte. Och ännu mer anmärkningsvärt är att det mest effektiva läget fungerar vid lägre temperatur.
-Exempel 2: Absorberad värme och cedt värme
En termisk maskin på 22 % producerar 1530 J arbete. Hitta: a) mängden värme som absorberas från termisk insättning 1, b) mängden värme kasserad till termisk tank 2.
a) I detta fall används effektivitetsdefinitionen, eftersom det utförda arbetet, inte om temperaturen för de termiska avlagringarna är tillgängliga. 22% effektivitet innebär att E Max = 0.22, därför:
Maximal effektivitet = arbete /qingång
Mängden som absorberas är exakt Qingång, Så rensar att du har:
Qingång = Arbete/effektivitet = 1530 J/0.22 = 6954.5 J
b) Mängden värme som tilldelats den kallaste tanken är från ΔW = qingång - Qutgång
Qutgång = Qingång - ΔW = 6954.5 -1530 J = 5424.5 J.
Ett annat sätt är från ochmax = 1 - (T2/T1). Eftersom temperaturer inte är kända, men dessa är relaterade till värme, kan effektiviteten också uttryckas som:
ochmax = 1 - (QSken/Qabsorberad)
Referenser
- Bauer, w. 2011. Fysik för teknik och vetenskap. Volym 1. MC Graw Hill. 654-657
- Kärnenergi. Drift av ett kärnkraftverk. Återhämtat sig från: energinukleär.netto
- Serway, R., Jewett, J. (2008). Fysik för vetenskap och teknik. Volym 1. 7th. Ed. Cengage Learning. 618-622.
- Tippens, s. 2011. Fysik: koncept och applikationer. Sjunde upplagan. Macgraw Hill. 414-416.
- Walker, J.2008. Fysik. 4: e upplagan.Addison Wesley. 610-630
- « Respekt i skolan hur man tillämpar det och konsekvenser
- Uppvärmningskurva Vad är, hur är det, exempel »

