Natriumklorit (NaClo2) struktur, egenskaper, användningar, risker

- 913
- 179
- Johan Olsson
han natriumklorit Det är ett oorganiskt fast ämne som bildas av en jon natrium Na+ och en jonklorit Clo2-. Dess kemiska formel är NaClo2. Det är ett kristallint vitt fast ämne, förutom att det är ett starkt oxidationsmedel. Därför måste det vara mycket försiktigt.
Dess huvudanvändning är som ett desinfektionsmedel för många applikationer. Det gör det möjligt att eliminera mikrober på ytor som golv, väggar och laboratorieutrustning på sjukhus och kliniker och i deras vattensystem.
 Natriumklorit naklo2 fast. Författare: kemisk interest . Källa: Wikimedia Commons.
Natriumklorit naklo2 fast. Författare: kemisk interest . Källa: Wikimedia Commons. Även i jordbruks- och veterinäranläggningar, för att hygienisera fågelägginkubatorer, för att kontrollera infektioner av mjölkkor, för att desinficera vattensystem för djur etc.
I livsmedelsindustrin tjänar deras surgörade vattenhaltiga lösningar till att tvätta kött, kycklingar, frukt, grönsaker, liksom utrustningen för sådana anläggningar.
Med natriumklorit kan klortioxid framställas2 På användningsstället, som gör att du kan eliminera mikrober, dålig lukt och smaker av vatten så att det är trevligt och kan dricka utan problem.
Det tjänar också till blekmedel pappersmassa, vegetabiliska textilfibrer och oljor, bland andra applikationer.
Naklo2 Fast måste hanteras med försiktighet, eftersom i kontakt med vissa material kan explosioner uppstå. Deras lösningar är lite lättare att manipulera men de är mycket oxiderande och frätande.
[TOC]
Strukturera
Natriumklorit består av en natriumn -katjon+ och en anjonklorit Clo2- Därför är de förenade av en jonisk bindning.
Kloritanjonen har en kloratom i ett +3 oxidationstillstånd och två syreatomer med Valencia -2 vardera. Av denna anledning har kloritanjonen en negativ börda.
Den har också en vinkelformad struktur.
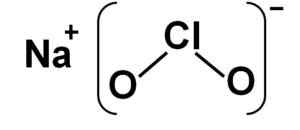 Naklo natriumkloritstruktur2. Författare: Marilú Stea.
Naklo natriumkloritstruktur2. Författare: Marilú Stea. Nomenklatur
- Natriumklorit
- Natriumklorit
- Natriumsalt av kloro
Egenskaper
Fysiskt tillstånd
Kristallint vitt fast ämne.
Molekylvikt
90,44 g/mol.
Smältpunkt
Det sönderdelas när det smälter mellan 180 och 200 ºC.
Densitet
2 468 g/cm3
Löslighet
Vattenlöslig: 64 g/100 g vatten vid 17 ºC. Något lösligt i metanol.
Andra egenskaper
Det är något hygroskopiskt.
Det är ett starkt oxidationsmedel. Reagerar våldsamt med brännbara material och reducerare. Reagerar våldsamt med syror och genererar klordioxid CLO2.
Kan tjäna dig: Hume-rothery reglerDess alkaliska lösningar (det betyder i närvaro av till exempel NaOH) är ganska stabila, medan i surt medium är klorsyra HCLO bildad2, som sönderdelas snabbt:
4 hclo2 → 2 CLO2↑ + Clo3- + Kli- + 2 h+ + H2ANTINGEN
Risker
Båda NaClo2 Fast eftersom deras vattenhaltiga lösningar är potentiellt farliga och kräver mycket försiktighet och erfarenhet under deras manipulation och lagring.
Naklo2 Fast kan explodera när du kommer i kontakt med organiska ämnen inklusive handskar och kläder, spill -kontrollmaterial som sågspån och avfallsbomull, samt oljor och fetter.
Den fasta formen är därför mycket svår att transportera och den föredras att använda den i form av vattenhaltiga lösningar.
Dessa lösningar är extremt frätande. De bör helst hålla ett pH över 8, det vill säga ett alkaliskt pH.
Naklo2 påskyndar förbränningen av föreningar eller brandfarliga material, så att det kan bilda explosiva blandningar med dessa.
Om det är uppvärmt, avge toxiska röker av HCl -saltsyra och natriumoxid Na2ANTINGEN. Om det är förlängt förlängt till värme eller avfyra kan det utnyttja.
Erhållande
Den är beredd på början med den kemiska eller elektrokemiska reduktionen av Sodio Naclo3, I närvaro av HCl -saltsyra för att producera klordioxid CLO2.
Det senare reagerar med väteperoxid h2ANTINGEN2 I NaOH -natriumhydroxid vattenlösning och en natriumnatriumkloritlösning erhålls2, som avdunstar och kristalliserar det fasta.
Det kan också erhållas genom att passera klordioxidgas2 För en NaOH -lösning.
2 Clo2 + 2 NaOH → Naclo2 + Naklo3 + H2ANTINGEN
Ansökningar
Som mikrobicid och desinfektionsmedel i flera applikationer
Det är en ingrediens i många produkter som tjänar till att kontrollera bakterier, svampar och slam eller alger silt. Produkter som innehåller det för detta ändamål används inom jordbruk, handel, industri och bostäder eller hem.
Det fungerar som ett desinfektionsmedel för många typer av material och ytor.
Inom jordbruk är fjäderfä- och liknande industrier desinficerade hårda ytor, utrustning, anläggningar för inkubering av fågelägg, växthus för svampar som svamp och kylvatten och vattenvattensystem för fåglarpennor.
Det har veterinäranvändning som ett aktuellt desinfektionsmedel i kontrollen av mastit av mjölkkreatur, för att fördjupa djurets bröstvårtor. Mastit är en infektion av kor udrar.
Kan tjäna dig: adiabatisk process: typer, exempel, lösta övningar Ibland måste du fördjupa kor i natriumkloritlösningar för att undvika infektioner i dem. Författare: Hans Braxmeier. Källa: Pixabay.
Ibland måste du fördjupa kor i natriumkloritlösningar för att undvika infektioner i dem. Författare: Hans Braxmeier. Källa: Pixabay. Det används också i naturliga forskningsanläggningar för att dekontaminera laboratorier.
Kommersiella, industriella och medicinska användningsområden inkluderar desinficering av ventilationssystem, hårda ytor (som golv, väggar, laboratorieutrustning) och vattensystem.
I vårdinrättningar som kliniker och sjukhus används det för att dekontaminera rum, korridorer, isoleringsområden och materialsterilisering.
Det är också användbart för hygienisering i anläggningar där människor genomgår vatten- eller spa -hälsobehandlingar.
I livsmedelsindustrin används det som ett rökmedel för att spara mat.
Det används i form av surd natriumklorit. Detta produceras genom att tillsätta livsmedelskvalitet (till exempel citronsyra, fosforsyra, hjulsyra eller natriumsyra sulfat) till en vattenhaltig lösning av natriumklorit.
Surmed natriumklorit har antimikrobiella egenskaper och används som dagg eller kycklingtvätt eller blötlösning, kött, grönsaker, frukt och havsprodukter. Också i vatten för att frysa kyckling eller fåglar.
I hushåll gör det att desinficera hårda ytor, såsom golv och badrum, uppvärmning eller luftkonditioneringssystem och poolvattencirkulationssystem.
 För att desinficera pooler kan du använda natriumklorit NaClo2. Författare: Age Global Group. Källa: Pixabay.
För att desinficera pooler kan du använda natriumklorit NaClo2. Författare: Age Global Group. Källa: Pixabay.  Produkter som innehåller natriumklorit tillåter toalettbadrum. Författare: Michal Jarmoluk. Källa: Pixabay.
Produkter som innehåller natriumklorit tillåter toalettbadrum. Författare: Michal Jarmoluk. Källa: Pixabay. Det säljs också i små påsar tillsammans med andra föreningar för att frigöra gas- och kontrolllukt i hem.
Att desinficera dricksvatten
Det används vid rening av vatten för att dricka, fungerar som en oxidant, vilket förbättrar smaken och lukten av dricksvatten.
Natriumklorit används allmänt som föregångare för generering av Clo -klordioxid2 som tjänar till att behandla dricksvatten för livsmedel, det vill säga att eliminera mikroorganismer, lukt och obehagliga smaker och kan dricka.
För att generera CLO2 HCL kan användas:
5 NaClo2 + 4 HCl → 4 CLO2↑ + 5 NaCl + 2 h2ANTINGEN
Clo2 Det är ett antimikrobiellt medel för högverkande oxidant och brett spektrum. Det vill säga handlingar mot ett stort antal mikroorganismer.
Det kan tjäna dig: kaliumnitrit (KNO2): Struktur, egenskaper och användningarMikroorganismer är inaktiverade eftersom CLO2 stör viktiga enzymer av dessa och med cellmembranproteiner. Det har också fördelen att den inte producerar organoklorföreningar, som är toxiska.
Det finns till salu natriumklorittabletter blandade med andra föreningar som löses i vattnet och producerar omedelbart CLO2 på ett kontrollerat sätt och därmed desinficera vattnet.
 Natriumklorit används med andra föreningar för att få dricksvatten redo att dricka. Författare: Ulrike Leone. Källa: Pixabay.
Natriumklorit används med andra föreningar för att få dricksvatten redo att dricka. Författare: Ulrike Leone. Källa: Pixabay. Det största problemet med att behandla vatten för att ta bort smaker och lukt genom CLO2 Det består av att toxisk klorit och kloresalter kan bildas under behandlingen.
För kontaktlinsvård
Naklo2 Det är en del av de lösningar som används för att desinficera kontaktlinser.
En NaClo -kombination används2 och spår (mycket små mängder) väteperoxid h2ANTINGEN2.
H2ANTINGEN2 Stabilisera CLO2 som bildas och kombinationen av båda är mycket effektiv mot bakterier, svampar och jäst. De produkter som då är är natriumklorid, vatten och syre, vilket är ofarligt, vilket innebär att de inte är skadliga för ögat.
När linserna tas bort från lösningen, NaClo2 återstående sönderdelas snabbt i nall och o2. Återstående peroxid irriterar inte ögat. Därför är dessa lösningar mycket säkra.
 Lösningarna för att desinficera kontaktlinser har natriumklorit bland sina ingredienser. Författare: Nieuw ~ Commonswiki. Källa: Wikimedia Commons.
Lösningarna för att desinficera kontaktlinser har natriumklorit bland sina ingredienser. Författare: Nieuw ~ Commonswiki. Källa: Wikimedia Commons. I olika applikationer
Natriumklorit används för klordioxidpreparat2 för omedelbar användning i ett stort antal tillämpningar som vissa behandlades i tidigare stycken.
Det tjänar till att bleka trämassa, textilier som bomull, växtfibrer, ätliga och icke -ätliga oljor, fetter, lack, lack och vaxer.
Det är en del av ögondroppar och vissa lösningar för oral tvätt.
Det används i läderbearbetningsindustrin och i medel för metallelektrod (metallbeläggning).
Referenser
- Williams, L. et al. (2019). Mikrobiologi, linsvård och underhåll. I kontaktlinser (sjätte upplagan). Återhämtat sig från Scientedirect.com.
- ELLER.S. National Library of Medicine. (2019). Natriumklorit. Återhämtat sig från pubchem.Ncbi.Nlm.Nih.Gov.
- Grå, n.F. (2014). Klordioxid. Processteknik. I mikrobiologi av vattenburna sjukdomar (andra upplagan). Återhämtat sig från Scientedirect.com.
- McKen, L. (2012). Introduktion till matradition och medicinsk sterilisering. Klordioxid. I effekt av sterilisering på plast och elastomerer (tredje upplagan). Återhämtat sig från Scientedirect.com.
- Ortenberg, e. och Telsch, b. (2003). Smak- och luktproblem i dricksvatten. I handbok för vatten- och avloppsmikrobiologi. Återhämtat sig från Scientedirect.com.
- Karsa, D.R. (2007). Biocider. Klordioxid. I handbok för rengöring/dekontaminering av ytor. Återhämtat sig från Scientedirect.com.
- Bomull, f. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Ullmanns Encyclopedia of Industrial Chemistry. (1990). Femte upplagan. VCH Verlagsgellschaft MBH.

