Deuterium
- 2056
- 68
- Erik Eriksson
Vad är deuterium?
han deuterium Det är en av de isotopiska vätearter, som representeras som D eller 2H. Dessutom har namnet på tungt väte ges, eftersom dess massa är dubbelt så mycket som protonen. En isotop är en art som kommer från samma kemiska element, men vars massantal skiljer sig från detta.
Denna distinktion beror på skillnaden i antalet neutroner den har. Deuterium anses vara en stabil isotop och kan hittas i föreningar som bildas av väte av naturligt ursprung, även om det är i en ganska liten andel (mindre än 0,02 %).
Med tanke på dess egenskaper, mycket lik de av vanligt väte, kan den ersätta väte i alla reaktioner där det deltar och blir likvärdiga ämnen.
Av detta och andra skäl har denna isotop många tillämpningar inom olika vetenskapsområden och blir ett av de viktigaste.
Deuteriumstruktur
Deuteriums struktur utgörs huvudsakligen av en kärna som har en proton och en neutron, med en atomvikt eller en massa på cirka 2 014 g.
På samma sätt är denna isotop skyldig sin upptäckt till Harold C. Urey, en kemist från USA, och dess kollaboratörer Ferdinand Brickwedde och George Murphy, 1931.

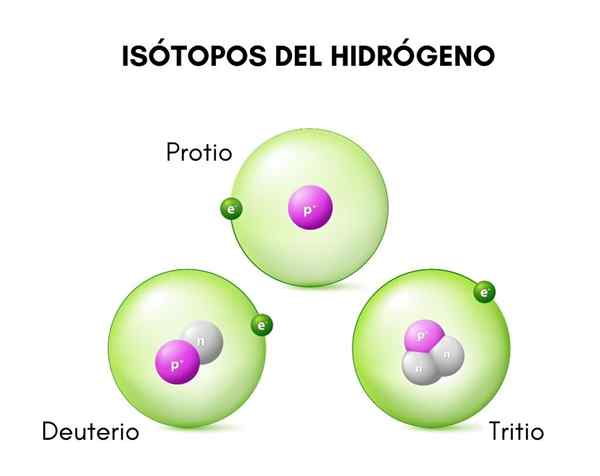
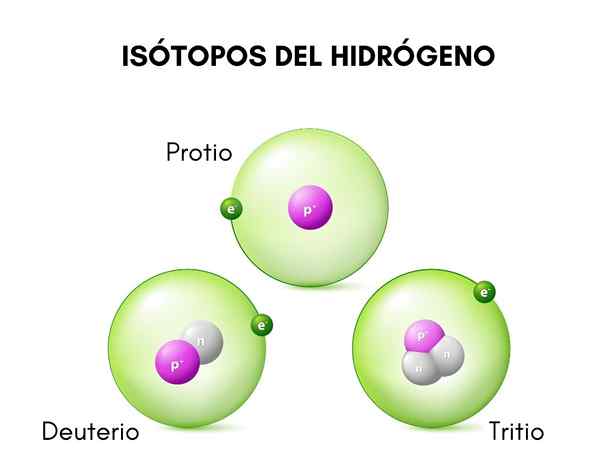
I den övre bilden kan du se jämförelsen mellan strukturerna i isotoperna av väte, som finns i protioform (dess vanligaste isotop), deuterium och tritium, beställt från vänster till höger.
Beredningen av deuterium i dess rena tillstånd genomfördes framgångsrikt för första gången 1933, men sedan 1950 -talet har ett fast fasämnet använts och som har visat stabilitet, kallad litium deuteride (lock), för ersättning deuterium och tritium i ett stort antal kemiska reaktioner.
Kan tjäna dig: kloroxid (iii): egenskaper, struktur, användningarI detta avseende har överflödet av denna isotop studerats och det har observerats att dess andel i vattnet kan variera något, beroende på källan från vilken provet tas.
Genom spektroskopi -studier har dessutom förekomsten av denna isotop på andra planeter i denna galax fastställts.
Vissa uppgifter om deuterium
Den grundläggande skillnaden mellan isotoperna av väte (som är de enda som har namngivits på olika sätt) ligger i deras struktur, eftersom mängden protoner och neutroner hos en art ger dess kemiska egenskaper.
Å andra sidan elimineras det befintliga deuterium inuti de stellar kropparna med en snabbare hastighet än vad som har sitt ursprung.
Dessutom anses det att andra naturfenomen endast bildar en mycket liten mängd av det, så dess produktion fortsätter att generera intresse idag.
På liknande sätt har en serie undersökningar avslöjat att de allra flesta atomer som har bildats av denna art har sitt ursprung i Big Bang; Detta är anledningen till att dess närvaro på stora planeter som Jupiter varnas.
Eftersom det vanligaste sättet att uppnå denna art i naturen är när den kombineras med väte i form av protio, väcks intresset för det vetenskapliga samfundet fortfarande av förhållandet som fastställs mellan andelen båda arter inom olika vetenskapsområden, sådana som astronomi eller väder.
Kan tjäna dig: renio: upptäckt, egenskaper, struktur, användningarDeuteriumegenskaper
- Det är en isotop som saknar radioaktiva egenskaper; det vill säga det är ganska stabilt i naturen.
- Det kan användas för att ersätta väteatomen i kemiska reaktioner.
- Denna art manifesterar ett annat beteende än vanligt väte i biokemiska reaktioner.
- När de två väteatomerna byts ut i vattnet erhålls d2Eller förvärva namnet på tungt vatten.
- Väte som finns i havet som är i form av deuterium finns i en andel av 0,016 % i förhållande till protioen.
- I stjärnorna har denna isotop en tendens att smälta snabbt för att ge upphov till helium.
- D2Eller utgör en toxisk art, även om dess kemiska egenskaper liknar de för H2
- När deuteriumatomer utsätts för kärnfusionsprocessen vid höga temperaturer erhålls frigöring av stora mängder energi.
- Fysikaliska egenskaper som kokpunkt, densitet, förångningsvärme, trippelpunkt, bland andra, har stora storlekar i deuteriummolekyler (D2) att i väte (h2).
- Det vanligaste sättet det finns är kopplat till en väteatom, vilket orsakar väte -deuteride (HD).
Användning/applikationer
På grund av dess egenskaper används deuterium i en mängd olika tillämpningar där väte är involverat. Vissa av dessa användningar beskrivs nedan:
- Inom biokemi används det i den isotopiska markeringen, som består av att "markera" ett prov med den isotop som valts för att spåra det genom dess passage genom ett givet system.
Kan tjäna dig: stark syra- I kärnreaktorer som utför fusionsreaktioner används den för att minska hastigheten med vilken neutroner rör sig utan den höga absorptionen av dessa som det vanliga väteet presenterar.
- Inom området med kärnmagnetisk resonans (NMR) används lösningsmedel baserat på deuterium för att erhålla prover av denna typ av spektroskopi utan närvaro av störningar som produceras med hjälp av hydrerade lösningsmedel.
- Inom biologi studeras makromolekyler genom neutrondispersionstekniker, där proverna som är försedda med deuterium används för att avsevärt minska brus i dessa kontrastegenskaper.
- Inom farmakologiområdet används väteersättning av deuterium med den kinetiska isotopiska effekten som genereras och gör att dessa läkemedel kan ha ett längre halva livet.