Pi -länk
- 3568
- 958
- Lars Eriksson
Vi förklarar vad PI -länken är, hur dess egenskaper bildas, och vi ger flera exempel
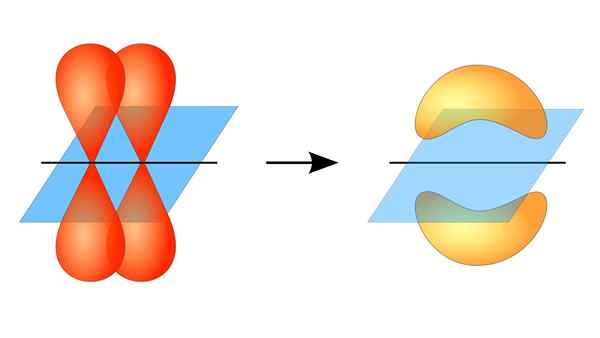
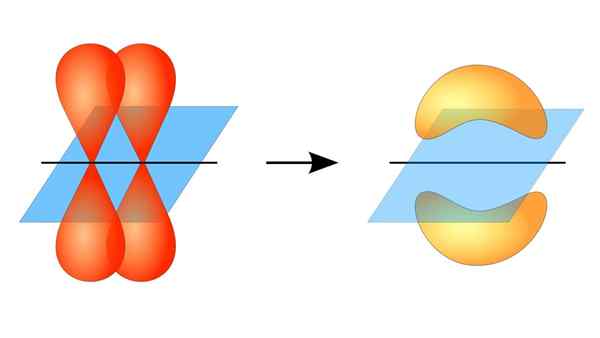 Två orbitaler P bildar en länk π
Två orbitaler P bildar en länk π Vad är en PI -länk?
En Pi -länk (π) Det är en kovalent typ av länk som kännetecknas av att förhindra fri rotationsrörelse av atomer och härstammar mellan ett par rena atomorbitaler, bland andra särdrag. Det finns länkar som kan bildas mellan atomer av deras elektroner, som gör att de kan bygga större och mer komplexa strukturer: molekyler.
Dessa länkar kan vara av olika sorter, men de vanligaste inom detta studieområde är det kovalenta. De kovalenta bindningarna, även kallade molekylära, är en typ av länk där de involverade atomerna delar elektronpar.
Detta kan uppstå på grund av behovet av atomer för att söka stabilitet och därmed bilda de flesta av de föreningar som är kända. I detta avseende kan kovalenta bindningar vara enkla, dubbla eller tredubbla, beroende på konfigurationen av deras orbitaler och mängden elektronpar som delas mellan de involverade atomerna.
Det är därför det finns två typer av kovalent bindning som bildas mellan atomer baserat på orienteringen av deras orbitaler: Sigma (σ) länkar och PI (π) länkar (π).
Det är viktigt att differentiera båda länkarna, eftersom Sigma -länken presenteras i enkla fackföreningar och PI i flera fackföreningar mellan atomer (två eller flera elektroner delas).
Hur är PI -länkformuläret?
För att beskriva bildningen av PI -länken bör den först diskuteras om hybridiseringsprocessen, eftersom den ingriper i vissa viktiga länkar.
Hybridisering är en process där hybridelektroniska orbitaler bildas; det vill säga där atomiska undernivå orbitaler och p kan blandas. Detta orsakar bildandet av SP, SP -orbitaler2 och sp3, som kallas hybrider.
Kan tjäna dig: reversibel reaktion: egenskaper och exempelI detta avseende inträffar bildningen av Pi -länkarna tack vare överlappningen av ett par lober som tillhör en atomisk orbital på ett annat par lober som är i en omloppsbana som är en del av en annan atom.
Denna orbitalöverlappning sker i sidled, så den elektroniska fördelningen koncentreras mestadels över och under planet som bildar de länkade atomkärnorna och får PI -bindningarna att vara svagare än sigmabindningarna.
När man talar om orbital symmetri för denna typ av förening, bör det nämnas att det är lika med den för P Orbitals typ P så länge den observeras genom axeln som bildas av länken. Dessutom utgörs dessa fackföreningar mestadels av orbitaler p.
PI -bindningsbildning i olika kemiska arter
Eftersom PI -bindningarna alltid åtföljs av en eller två länkar till (en sigma eller en annan PI och en sigma) är det relevant att veta att dubbelbindningen som bildas mellan två kolatomer (består av en sigma -bindning och en PI) har lägre länkenergi än den som motsvarar två gånger Sigma -länken mellan de två.
Detta förklaras av stabiliteten i Sigma -länken, som är större än för Pi -bindningen eftersom överlappningen av atomorbitaler i det senare inträffar parallellt i regionerna ovan och under lobarna, ackumulerar elektronisk distribution i ytterligare bort är atomiska atomiska kärnor.
Trots detta, när PI- och Sigma -länkar kombineras en flera högre länkar än den enkla länken av sig själv, som kan verifieras genom att observera länklängderna mellan olika atomer med enkla och flera länkar.
Kan tjäna dig: icke -metalliska oxiderDet finns några kemiska arter som studeras av deras exceptionella beteende, såsom koordinationsföreningar med metallelement, där de centrala atomerna endast är förenade med PI -bindningar.
PI -länkegenskaper
Tillåter inte atomernas fria rotationsrörelse
Egenskaperna som skiljer PI -länkarna från andra typer av interaktioner mellan atomarter beskrivs nedan, börjar med det faktum att denna förening inte tillåter den fria rotationsrörelsen av atomer, såsom kol. Av denna anledning, om det finns en rotation av atomerna, inträffar bindningsbrottet.
Överlappning mellan orbitaler med två parallella regioner
På samma sätt sker överlappningen mellan två parallella regioner i dessa länkar, vilket gör att de har en större diffusion än sigmabindningarna och att de av denna anledning är svagare.
Mellan ett par rena atomorbitaler
Å andra sidan, som nämnts ovan, genereras PI -länken alltid bland ett par rena atomorbitaler; Detta medel genereras bland orbitaler som inte har drabbats av hybridiseringsprocesser, där densiteten för elektroner mestadels är koncentrerad över och under planet som bildas av Covalent Union.
I detta avseende kan mer än en PI -länk presenteras bland ett par atomer, alltid åtföljs av en sigma -länk (i dubbelbindningar).

På liknande sätt kan du ge en trippellänk mellan två angränsande atomer, som bildas av två PI -bindningar i positioner som bildar vinkelräta plan med varandra och en sigma -länk mellan de två atomerna.
Kan tjäna dig: huminsyra: struktur, egenskaper, erhållning, användningExempel på PI -länkar
Etylenmolekyl
Som tidigare nämnts har molekylerna som utgörs av förenade atomer med en eller flera PI -bindningar alltid flera länkar; det vill säga dubbel eller trippel.
Ett exempel på detta är etenmolekylen (h2C = ch2), som består av en dubbelförening; Det vill säga en PI och en sigmabindning mellan dess kolatomer, utöver Sigma -bindningarna mellan kol och väten.
Acetylenmolekyl
För sin del har acetylenmolekylen (H-C≡C-H) en tredubbla koppling mellan dess kolatomer; Det vill säga två PI-bindningar som bildar vinkelräta plan och en Sigma-bindning, utöver dess motsvarande kolvätebindningar.
Bensen och derivat
PI -bindningar mellan cykliska molekyler presenteras också, såsom bensen (c6H6) och dess derivat, vars disposition resulterar i en effekt som kallas resonans, vilket gör att elektronisk densitet kan migrera mellan atomer och bidrag bland annat.
Dikarbon
För att exemplifiera de tidigare nämnda undantagen, fallen av den dikarbonala molekylen (C = C, där båda atomerna har ett par parade elektroner) och koordinationsföreningen som kallas hexacarbonildihierro (representerad som tro2(Co)6, som endast bildas av PI -länkar mellan dess atomer).

