Erytropoiesis -stadier och dess egenskaper, reglering, stimulerande
- 2034
- 250
- PhD. Lennart Johansson
De erytropoies Det är processen genom vilken röda blodkroppar eller erytrocyter bildas. Dessa blodceller, hos människor, har en genomsnittlig livslängd på fyra månader och kan inte reproducera sig själva. På grund av detta måste nya erytrocyter skapas för att ersätta dem som dör eller går förlorade i blödningar.
Hos män är antalet erytrocyter cirka 54 miljoner per milliliter, medan hos kvinnor är det lite lägre (48 miljoner). Cirka 10 miljoner erytrocyter går förlorade dagligen, så en liknande mängd måste återvinnas.
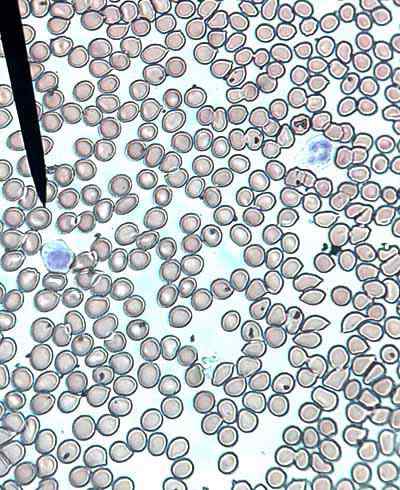
 Mänskligt blod, erytrocyter eller röda blodkroppar och två vita blodkroppar. Tagen och redigerad från: Viascos [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)].
Mänskligt blod, erytrocyter eller röda blodkroppar och två vita blodkroppar. Tagen och redigerad från: Viascos [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Erytrocyter bildas av kärnbildade erytroblaster som finns i den röda benmärgen hos däggdjur, medan i andra ryggradsdjur huvudsakligen förekommer i njurarna och mjälten.
När de når slutet av sina dagar fragmenterar de; Då inkluderar vissa celler som kallas makrofager dem. Dessa makrofager finns i levern, den röda benmärgen och i mjälten.
När röda blodkroppar förstörs återvinns järn för att användas igen, medan resten av hemoglobin förvandlas till ett gallpigment som kallas bilirubin.
Erytropoiesis stimuleras av ett hormon som kallas erytropoietin, men processen regleras av olika faktorer, såsom temperatur, syretryck, bland andra.
[TOC]
Steg och dess egenskaper
I vuxna organismer förekommer erytropoies på specialiserade platser i den röda benmärgen som kallas erytroblastiska öar. För bildning av erytrocyter måste flera processer som sträcker sig från cellproliferation till mognad av röda blodkroppar ske, genom flera stadier av celldifferentiering.
När cellerna genomgår mitotiska divisioner minskar de sin storlek och deras kärna, liksom kondensationen av kromatin och hemoglobinisering. Dessutom flyttar de sig bort från ursprungsområdet.
I de sista stadierna kommer de att förlora kärnan och andra organeller och går in i cirkulation och migrerar genom cytoplasmiska porer av endotelceller.
Vissa författare delar upp hela erytropoiseringsprocessen i två faser, den första av cellproliferation och differentiering; Medan andra delar upp processen baserat på specifika egenskaper hos cellen i varje steg, när de observeras med Wright -färgning. Baserat på det senare är stadierna av erytropoies:
1-enheter kolonier i Burst
De är de första cellerna som är känsliga för erytropoietin, vissa författare kallar dem myeloida föräldrar, eller även BFU-E, för dess akronym på engelska på engelska. De kännetecknas av att uttrycka ytantigener såsom CD34, såväl som närvaron av erytropoietinreceptorer i några mängder.
2-erytroidkolonier som bildar vägar
Förkortade på engelska som CFU-E, de kan producera små kolonier av erytroblaster. En annan egenskap hos dessa celler är att mängderna av erytropoietinreceptorer är mycket högre än i kolon -formande enheter i skurar.
3-Proeritroblastos
Betraktas som det första mognadstillståndet för erytrocyter. De kännetecknas av sin stora storlek (14 till 19 um enligt vissa författare, upp till 25 um enligt andra). Kärnan är rundad och presenterar också nukleoli och riklig kromatin.
Betraktas som det första mognadstillståndet för erytrocyter. De kännetecknas av sin stora storlek (14 till 19 um enligt vissa författare, upp till 25 um enligt andra). Kärnan är stor, rundad, med kromatin arrangerad i form av filament och 2 eller 3 nukleoli.
Kan tjäna dig: endocytos: typer och deras egenskaper, funktioner, exempelI detta skede börjar fångsten av plasmajärn. De har ett halvt timmars liv för att ge plats för mitos till nästa steg.
4-basofila erritroblaster
Även kallad normoblaster, de är mindre än deras föregångare. Dessa celler är färgade blå med vital färgning, det vill säga de är basofiler. Kärnan är kondenserad, nukleolierna har försvunnit och har ett stort antal ribosomer. I detta skede börjar hemoglobinsyntesen.
I början är de kända som basofila erytroblaster och efter en mitotisk uppdelning förvandlas de till typ II, som förblir basofiler och har större syntes av hemoglobin. Den ungefärliga varaktigheten för båda cellerna tillsammans liknar den för proeritroblaster.
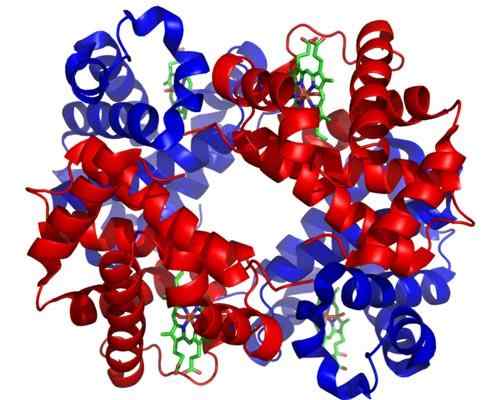 Hemoglobin. Tagen och redigerad från: Zephyris på engelska Wikipedia [CC BY-SA 3.0 (http: // Creativecommons.Org/licenser/BY-SA/3.0/]].
Hemoglobin. Tagen och redigerad från: Zephyris på engelska Wikipedia [CC BY-SA 3.0 (http: // Creativecommons.Org/licenser/BY-SA/3.0/]]. 5-polychromatofila erritroblaster
De bildas av mitotisk uppdelning av typ II -basofil erytroblaster och är de senaste cellerna med förmågan att dela med mitos. Dess storlek sträcker sig mellan 8 och 12 um, och de har en rundad och kondenserad kärna.
Cytoplasma av dessa celler färgas med blygrå med färgningen av Wright. Det presenterar en hög koncentration av hemoglobin och mängden ribosomer förblir hög.
6-ortokromatiska eryroblaster
Färgen av dessa celler är rosa eller rött på grund av mängden hemoglobin de har. Storleken är något lägre än för föregångarna (7 till 10 um) och har en liten kärna, som kommer att utvisas av exocytos vid mognad celler.
7-Reticulocyter
De bildas genom differentiering av ortokromatiska erytroblaster, förlorar organellerna och fyller deras hemoglobincytoplasma. De förblir i den röda benmärgen i två till tre dagar tills de migrerar till blodet där deras mognad kommer att kulminera.
8-eritrocyter
De är de mogna formelementen, den slutliga produkten av erytropoies och som bildas av mognad av retikulocyterna. De har en bicócava -form på grund av frånvaron av kärna och interaktionen mellan erytrocytcytoskelet och två proteiner som kallas spektrin och aktin.
De är de vanligaste blodkropparna, de bildas från retikulocyterna. Hos däggdjur har de en biconcava -form på grund av frånvaron av kärna och interaktionen mellan erytrocytcytoskeletten och två proteiner som kallas spektrin och aktin. I andra ryggradsdjur är de rundade och behåller kärnan.
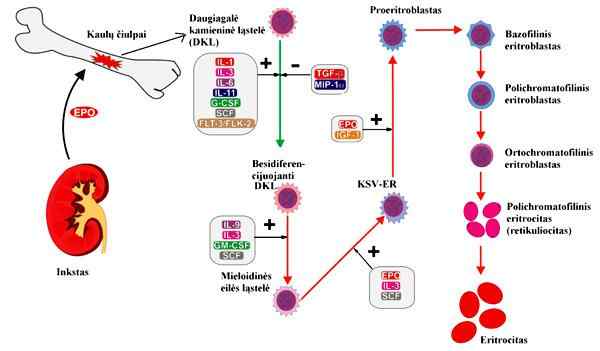 Erytropoicingprocess. Tagen och redigerad från en.Mikalauskas på det lithuanska språket Wikipedia [CC BY-SA 3.0 (http: // Creativecommons.Org/licenser/BY-SA/3.0/]]
Erytropoicingprocess. Tagen och redigerad från en.Mikalauskas på det lithuanska språket Wikipedia [CC BY-SA 3.0 (http: // Creativecommons.Org/licenser/BY-SA/3.0/]] Reglering av erytropo
Medan erytropoietin stimulerar bildningen av röda blodkroppar för att förbättra blods syretransportkapacitet, finns det flera grundläggande mekanismer för att reglera denna formation, inklusive:
Syrotryck
Koncentrationen av syre i blodet reglerar erytropoies. När denna koncentration är mycket låg i blodflödet som kommer njuren, stimuleras produktionen av röda blodkroppar.
Denna låga vävnadskoncentration kan uppstå på grund av hypoxemi, anemi, njurischemi eller när affiniteten hos hemoglobin med denna gas är större än normalt.
Miescher 1893 var den första som föreslog förhållandet mellan vävnadshypoxi och erytropoiesis. Denna hypoxi stimulerar emellertid inte direkt benmärgen att producera röda blodkroppar, som Miescher höjde. Tvärtom, det inducerar njurarna till produktionen av erytropoietinhormonet.
Erytropoietinproduktion på grund av vävnadshypoxi är genetiskt reglerad och receptorer som upptäcker att sådan hypoxi är inom njurarna. Erytropoietinproduktion ökas också på grund av ett partiellt tryck på vävnadssyre efter blödning.
Det kan tjäna dig: myitos: faser, egenskaper, funktioner och organismerCellerna som producerar erytropoietin finns i njurarna och levern. Ökningen av produktionen av detta hormon under anemi beror på en ökning av antalet celler som producerar det.
Testosteron
Testosteron reglerar indirekt erytropoies och reglerar järnnivåer i blodet. Detta hormon verkar direkt på verkan av ett cytoplasmiskt protein som kallas BMP -SMAD (morfogenetiskt protein av ben -Mad av dess akronym på engelska) på hepatocyter.
På grund av verkning av testosteron undertrycks hepcidintranskription. Denna hepcidin förhindrar passage av järn från cellerna till plasma från makrofager som återvinner järn, vilket leder till drastisk minskning av blodjärn.
När hypofysen inträffar kommer det att finnas en hämning av erytropoietin, eftersom det inte kommer att finnas något järn för produktion av erytrocyter.
Temperatur
Temperaturen har visat sig ha en effekt på erytripoyesis. Utställningar vid mycket låga temperaturer orsakar behovet av att producera värme i vävnaderna.
Detta kräver att man ökar mängden erytrocyter för att leverera syre till perifera vävnader. Men denna typ av reglering klargörs inte helt som.
Paracrinreglering
Uppenbarligen finns det en erytropoietinproduktion av neuronerna i centrala nervsystemet, för att bearbeta ischemisk skada och apoptos. Men forskare har ännu inte kunnat verifiera det.
Erytropoyesis stimulerande medel
Stimulerande medel av erytropoies (dessa) är agenter ansvariga för att stimulera erytrocytproduktion. Erytropoietin är hormonet naturligt ansvarigt för denna process, men det finns också syntetiska produkter med liknande egenskaper.
Erytropoietin är ett syntetiserat hormon främst i njuren. Under de tidiga utvecklingsstadierna deltar levern också i den aktiva produktionen av erytropoietin. Men när utvecklingen fortskrider har detta sista organ ett mindre viktigt deltagande i processen.
Erytrocyt börjar sprida receptorer för erytropoietin på membranytan. Erytropoietin aktiverar en serie intercellulära signaltransduktionsvattenfall.
De konstgjorda
Dessa konstgjorda klassificeras i generationer (först till tredje), beroende på det datum då de skapades och marknadsfördes. De liknar strukturellt och funktionellt erytropoietin.
Den första generationen är kända som Alpha, Beta och Delta Epoetin. De två första produceras genom rekombination från djurceller och har ett halvt liv på cirka 8 timmar i kroppen. Delta Epoetine syntetiseras under tiden från mänskliga celler.
Darbepoetina alfa är en andra generation som, producerad från kinesiska hamsterceller genom tekniken som kallas rekombinant DNA. Det har ett halvt liv mer än tre gånger högre än den första generationen. Liksom med epoetiner har vissa idrottare med hög yield använt darbepoetina som ett doping medel.
Kontinuerlig aktivator av erytropoetin eller vaxreceptor) är det generiska namnet på de tredje generationen. De försöker inte simulera strukturen och funktionen av erytropoietin, men de verkar genom att stimulera mottagaren av detta och därmed öka dess effekter.
Kan tjäna dig: mikrofilament: egenskaper, struktur, funktioner, patologiHans halvliv är flera veckor i stället för timmar, till exempel de tidigare läkemedlen. Kommersiellt använt sedan 2008, men dess olagliga användning i sportaktiviteter går tydligen tillbaka två eller tre år före dess lagliga kommersialisering.
Ineffektiv erytropoies
Ineffektiva eller ineffektiva erytropoier inträffar när de röda blodkropparna är defekt och i allmänhet förstörs innan de lämnar benmärgen eller en kort tid efter detta.
Ineffektiva erytropoies kan bero på defekter i syntesen av nukleinsyror, hemo -gruppen eller globinorna. Dessa defekter orsakar olika typer av anemi.
Defekter i nukleinsyrasyntes
I detta fall finns det brist på folsyra och kobalamin, DNA -syntes hämmas i kärnan hos erytrocytfrämjande celler, så dessa kan inte dela mitotiskt. Cytoplasma ökar under tiden sin volym (makrocytos) och har sitt ursprung i en stor cell som kallas megaloblasto.
I dessa fall har en serie anemier som kallas megaloblastiska anemier sitt ursprung, varav den vanligaste är skadlig anemi. I denna sjukdom finns det ingen absorption av vitamin B12 i tunntarmen.
Andra orsaker till megaloblastisk anemi inkluderar matsmältningssjukdomar, kannor, folsyrabrist och på grund av vissa mediciner.
Bland symtomen på denna typ av anemi är onormal blekhet, irritabilitet, olämplig, diarré, svårigheter att gå eller muskelsvaghet. Beroende på orsaken kan det behandlas med vitamin- eller folsyratillskott.
Defekter i syntesen av hemo -gruppen
Ineffektiva erytropoies på grund av järnsyntes kan orsaka två typer av anemi; Mikrocytisk anemi genom järnunderskott och sideroblastisk anemi.
Det är känt som mikrocytisk anemi till en grupp anemier som kännetecknas av erytrocyter med reducerad storlek och blek färg, de kan ha olika ursprung, inklusive talasyemia och ineffektiva erytropoiesis.
I sideroblastiska anemi är järn- och hemosiderinnivåerna mycket höga. Herniderin är ett gult pigment som härstammar från hemoglobin och visas när metallnivåerna är normala än normalt. Denna typ av anemi orsakar död av basofiler i den röda benmärgen och det finns ingen hemoglobinsyntes.
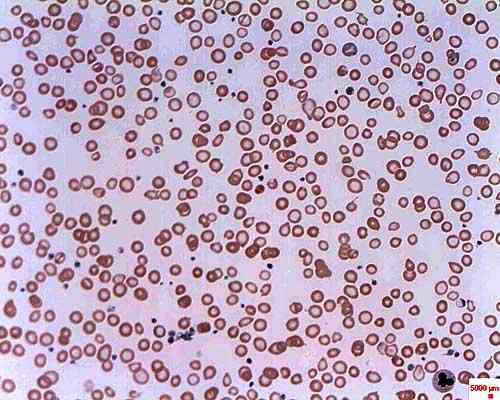 Järnbristanemi. Tagen och redigerad från: Erhabor Osaro (docent) [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)].
Järnbristanemi. Tagen och redigerad från: Erhabor Osaro (docent) [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Det kallas sideroblastisk anemi eftersom erytrocyter utvecklas onormalt genom ackumulering av järn i form av granuler och får namnet på sideroblaster. Sideroblastisk anemi kan vara medfödd eller kan vara sekundär och ha olika orsaker.
Defekter i globinsyntes
I detta fall presenteras drapanocytisk anemi och beta talasmia. Drepanocytisk anemi är också känd som falciform anemi. Det produceras av en genetisk mutation som leder till ersättning av glutaminsyra med valin under syntesen av beta globin.
På grund av sådan substitution minskar affiniteten hos hemoglobin genom syre och det finns atrofi av erytrocyt, vilket får HOZ -form istället för den normala formen av en bicócavo -skiva. Patienten med drapanocytisk anemi kommer sannolikt att drabbas av mikroinfartos och hemolys.
Talaasemia är en sjukdomsprodukt av en olämplig genetisk kodning av a- och ß-globiner som leder till en tidig död av erytrocyt. Det finns cirka hundra olika mutationer som kan orsaka talaasemi med olika grader av svårighetsgrad.
Referenser
- Erytropoies. I Wikipedia. Hämtas från.Wikipedia.org.
- J.P. Labbrozzi (2015). Erytrocytproduktion från CD34 -celler+ av navelsträngsblod. Doktorsavhandling. Autonomt universitet i Barcelona. Spanien.
- H. Parrales (2018). Fysiologi för erytropoies. Cerebromedical återhämtad.com.
- Anemi. I Wikipedia. Hämtas från.Wikipedia.org.
- Erytropoiesis stimulerande medel. I Wikipedia. Hämtas från.Wikipedia.org.
- Ineoffective erishropoiesis. I Wikipedia. Hämtas från.Wikipedia.org.
- « Gregarias Relations Egenskaper, fördelar och exempel
- Pinus ayacahuite -egenskaper, livsmiljö, vård, skadedjur »

