Spridningsfas
- 3743
- 1119
- Johan Olsson
 Källa: Gabriel Bolívar
Källa: Gabriel Bolívar Vad är den spridda fasen?
De spridningsfas Det är den som är till en mindre andel i en spridning och består av mycket små partikelaggregat. Under tiden kallas den vanligaste och kontinuerliga fasen där partiklarna ligger spridningsfasen. Ett exempel är vatten med socker, där den spridda fasen skulle vara socker och spridande vatten.
Dispersionerna klassificeras beroende på storleken på partiklarna som bildar den spridda fasen och kan skilja tre typer av spridningar: oförskämda spridningar, kolloidala lösningar och riktiga lösningar.
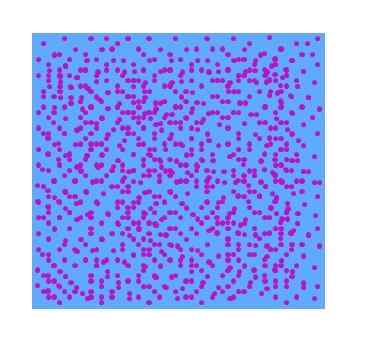
I den överlägsna bilden kan en hypotetisk dispergerad fas av lila partiklar i vatten ses. Som ett resultat kommer ett glas fullt av denna spridning inte att visa transparens för synligt ljus; det vill säga det kommer att se ut som en lila flytande yoghurt. Typen av dispersioner varierar beroende på storleken på dessa partiklar.
När de är "stora" (10-7 m) det talas om oförskämda spridningar och kan sediment genom tyngdkraften; kolloidala lösningar, om deras storlekar varierar mellan 10-9 M och 10-6 M, vilket gör dem synliga endast med ultramikroskop eller elektroniskt mikroskop; och sanna lösningar, om deras storlekar är mindre än 10-9 M, att kunna korsa membran.
Sanna lösningar är därför alla de som är populärt kända, till exempel vinäger eller sockerhaltigt vatten.
Egenskaper för den spridda fasen
Lösningarna utgör ett särskilt fall av spridningar, dessa är av stort intresse för kunskapen om fysioquimica of levande varelser. De flesta biologiska ämnen, både intracellulära och extracellulära, finns i form av samtalspridningar.
Brownian Movement och Tyndall Effect
Partiklarna i den spridda fasen av kolloidala lösningar har en liten storlek som hindrar deras sedimentation. Dessutom rör sig partiklar ständigt i slumpmässig rörelse och kolliderar med varandra, vilket också gör sedimentation svårt. Denna typ av rörelse kallas Brownian.
Kan tjäna dig: Violet GlassPå grund av den relativt stora storleken på de spridda faspartiklarna har kolloidala lösningar ett skumt eller till och med ogenomskinligt utseende. Detta beror på att ljuset sprids när kolloiden korsar, ett fenomen som kallas Tyndall -effekt.
Heterogenitet
Kolloidala system är icke -homogena system, eftersom den spridda fasen består av partiklar med en diameter mellan 10-9 M och 10-6 m. Medan lösningspartiklarna har en mindre storlek, vanligtvis mindre än 10-9 m.
Partiklarna i den spridda fasen av kolloidala lösningar kan korsa filterpapper och lerafilter. Men de kan inte korsa dialysmembran som cellofan, kapillärendotel och colodion.
I vissa fall är partiklarna som bildar den spridda fasen proteiner. När de är i vattenfasen viker proteinerna och lämnar den hydrofila delen utanför för en större interaktion med vatten, genom jon-dipolo-krafterna eller med bildandet av vätebroar.
Proteiner bildar ett retikulärt system inuti cellerna och kan ta en del av dispergeringsmedlet. Dessutom tjänar proteinernas yta till att förena små molekyler som ger en ytlig elektrisk laddning, vilket begränsar interaktionen mellan proteinmolekyler, vilket hindrar dem från att utgöra blodproppar som orsakar sedimentation.
Stabilitet
Kolloider klassificeras enligt attraktionen mellan den spridda fasen och spridningsfasen. Om spridningsfasen är flytande klassificeras kolloidala system som solar. Dessa är indelade i deliphilos och liofober.
Det kan tjäna dig: kaliumklorat (KCLO3)Liofilkolloider kan bilda verkliga lösningar och är termodynamiskt stabila. Å andra sidan kan Liofobes -kolloiderna bilda två faser, eftersom de är instabila, även om de är stabila ur den kinetiska synvinkeln. Detta gör att de kan stanna i ett spridd tillstånd under lång tid.
Spridda fasexempel
Både spridningsfasen och den spridda fasen kan uppstå i de tre fysiska tillstånden i saken, det vill säga: fast, flytande eller gasformigt.
Normalt är den kontinuerliga eller spridande fasen i ett flytande tillstånd, men kolloider vars komponenter finns i andra tillstånd av aggregering av materia kan hittas.
Möjligheterna för kombination av spridningsfasen och den spridda fasen i dessa fysiska tillstånd är nio.
Var och en kommer att förklaras med några respektive exempel.
- Fasta lösningar: När spridningsfasen är solid kan den kombineras med en spridd fas i fast tillstånd och bildar de så kallade fasta lösningarna.
Dessa är exempel på dessa interaktioner: många stållegeringar med andra metaller, några färgglada ädelstenar, förstärkt gummi, porslin och pigmenterad plast.
- Fasta emulsioner: Den fasta tillståndet som sprider sig kan kombineras med en flytande spridningsfas och bildar de så kallade fasta emulsionerna. De är exempel på dessa interaktioner: ost, smör och gelé.
- Fasta skum: Den spridande fasen som ett fast ämne kan kombineras med en spridd fas i ett gasformigt tillstånd, som utgör de så kallade fasta skummen. Exempel på dessa interaktioner är svamp, gummi, pimpsten och gummikum.
- Sulor och geler: Den spridande fasen i flytande tillstånd kombineras med den spridda fasen i fast tillstånd och bildar solen och geler. Exempel på dessa interaktioner är magnesimjölk, målningar, lera och pudin.
Kan tjäna dig: stötdämpare lösningar- Emulsioner: Den spridande fasen i flytande tillstånd kombineras med den spridda fasen också i ett flytande tillstånd, vilket producerar de så kallade emulsionerna. Exempel på dessa interaktioner är mjölk, ansiktskräm, salladdressing och majonnäs.
- Skum: Den spridande fasen i flytande tillstånd kombineras med den spridda fasen i ett gasformigt tillstånd och bildar skummen. Exempel på dessa interaktioner är rakkräm, vispgrädden och ölskummet.
- Fasta aerosoler: Den spridande fasen i ett gasformigt tillstånd kombineras med den spridda fasen i fast tillstånd, vilket orsakar de så kallade fasta aerosolerna. Exempel på dessa interaktioner är rök, virus, korpuskulära material i luften, materialen som släpps ut av bilarnas avgasrör.
- Flytande aerosoler: Den spridande fasen i ett gasformigt tillstånd kan kombineras med den spridda fasen i flytande tillstånd, som utgör de så kallade flytande sprayerna. Exempel på dessa interaktioner är dimma, dimma och dagg.
- Sann lösningar: Den spridande fasen i ett gasformigt tillstånd kan kombineras med den gasformiga fasen i gasformigt tillstånd och bildar de gasformiga blandningar som är riktiga lösningar och inte kolloidala system. Exempel på dessa interaktioner är belysningens luft och gas.
Referenser
- Whitten, Davis, Peck & Stanley. Kemi (8.ª ed.). Cengage Learning.
- Topppr (s.F.). Klassificering av kolloider. Återhämtat sig från: toppr.com
- Jiménez Vargas, J och Macarulla. J. M. (1984). Fysiologisk fysikaliskik, sjätte upplagan. Inter -amerikansk redaktion.
- Madhush. Skillnaden mellan spridningsfasen och dispersionsmedum. Återhämtat sig från: pediaa.com

