Galvanoplastik

- 1002
- 76
- Anders Larsson
Vi förklarar vad galvanoplastik består av, även kallad elektrodeposition, hur är dess process, praktiska exempel och dess tillämpningar.
 Galvanoplasti av en sked
Galvanoplasti av en sked Vad är galvanoplastik?
Galvanoplastik eller elektrodeposition är en elektrokemisk teknik som består, som namnet antyder, vid avsättningskikt av metaller vid mottagande av objekt; Det vill säga att täcka dem från ett metallskydd, vars tjocklek sträcker sig mellan 5-20 μm.
Denna teknik är också känd som elektrochapado eller elektrolytisk pläterad, eftersom ett elektrolytiskt medium bestående av metalljoner av metallen som önskas att avsätta är oumbärlig för dess implementering. Därför, om vi vill ha en kopparpläterad (koppar), kommer vi att behöva kopparlösliga salter, såsom kopparsulfat, upplöst i vatten.
Det föregående resonemanget gäller för någon annan metall: en guldelektrolytisk pläterad kommer att kräva guldsalter, vanligtvis guldcyanider, vilket kan bli mycket giftigt. Således kan vissa föremål, såsom att äta redskap, beläggas med guld för att tilldela större värde och adel.
Men galvanoplastik går utöver estetik: de tilldelas. Det tillåter också att spara naturresurser, eftersom det inte är nödvändigt att spendera stora mängder metall för beläggningar.
Galvanoplastik
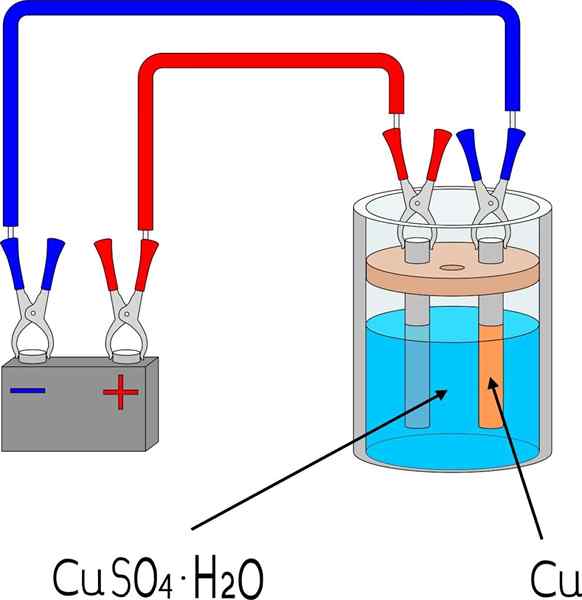 Kopparelektrodeposition i ett badrum för kopparsulfat
Kopparelektrodeposition i ett badrum för kopparsulfat Föremål
För att elektrodapose en metall på en yta behövs vissa grundelement, vars dimensioner och läge kommer att variera beroende på omgången av föremål som ska täckas.
I den övre bilden visas till exempel liten skala kopparelektrod, reproducerbar i alla laboratorier eller utrymmen.
Elektrolytisk medium
Först behövs ett elektrolytmedium för metall till elektrodeposit. Kopparsulfat salt, Cuo4, Det är mycket lösligt i vatten, så det ger joner cu2+ som sedan kommer att reduceras till atomer cu0. Dessa atomer är de som kommer att monteras på mottagningsytan för att ge upphov till metallkristaller.
Det elektrolytiska mediet är nödvändigt för att kretsen ska fungera och joniska belastningar kan röra sig eller mobilisera mot regionen där elektrodepositionen inträffar.
Elektroder
Elektroderna är ytorna på vilka elektrodepositionen sker från dess kemiska bas. Enkelt uttryckt finns det två elektroder: katoden, där metallen är elektrodepos; Och anoden, där en kemisk reaktion äger rum som donerar elektroner till metalljonerna som täcker katoden.
Det kan tjäna dig: uretan: struktur, egenskaper, erhålla, användningarDet vill säga katoden blir det stycke som är önskvärt. Samtidigt är anoden varje yta på vilken en art oxiderar och donerar sina elektroner till katoden. Många gånger är anoden gjord av samma metall som löses i den elektrolytiska miljön. Om det finns kopparjoniskt i mitten, kommer anoden i detta fall att vara metallisk koppar.
Yttre krets
Den externa kretsen är ett batteri som tillhandahåller de ursprungliga elektronerna som främjar elektrodeposition. Dess närvaro innebär att reaktionen inte är spontan: elektricitet behövs för att generera en kemisk förändring, vilket är reduktionen av upplösta metalljoner.
Elektrodrengöring
Den bit som ska täckas måste vara helt ren. Annars kommer den pläterade eller beläggningen att vara defekt.
För att göra detta måste du se till att ytan är helt hydrofil, det vill säga att den inte har fett eller något smuts. Ett sätt att säkerställa att detta, efter kemisk tvätt, är att våta biten med vatten, och om bildningen av vatten sjunker eller en icke -enhetlig vätskedroppe observeras, betyder det att elektroden inte är ren ännu.
Reaktioner och betydelse av elektroner
Galvanoplastik är en redoxreaktion. Därför: en art måste minskas, medan den andra oxideras eller vice versa. I koppar har vi en anod gjord av koppar, och en katod gjord av en metall ME (järn, zink, tenn, etc.).
När vi slår på batteriet kommer de att flöda elektroner till katoden, som börjar ladda negativt.
Den negativa belastningen av katoden lockar katjoner cu2+ av den elektrolytiska miljön, som äger rum reduktionen:
Cu2+(AC) +2E- → CU (S)
Det kan tjäna dig: Maillard -reaktionBatteriet måste återställa de donerade elektronerna, och även jonerna Cu måste återvinnas2+ reducerad för att upprätthålla neutraliteten i den elektrolytiska miljön. Detta är när anoden kommer i funktion: kopparatomer oxiderar:
CU (S) → CU2+(AC) +2E-
Och de släppta elektronerna riktas tillbaka till batteriet, som i sin tur mobiliserar dem mot katoden för att fortsätta elektrodepositionen.
Anoden får en positiv belastning, som lockar SO -jonerna42- av det elektrolytiska mediet (se bilden igen).
Det vill säga reaktionerna som inträffar är reduktion och oxidation av koppar, metallen som är elektrodepos:
Cu2+(AC) +2E- → CU (S)
CU (S) → CU2+(AC) +2E-
Anoden, av koppar, förlorar degen medan katoden, av en annan metall, är täckt med ett fint kopparskikt.
Exempel på galvanoplastik
Silver
Metaller kan vara "elektroplatta", som elektrolytiskt täcker dem från ett silverlager. Detta är särskilt fördelaktigt i elektroniska komponenter som måste utföra el. Silver kan vara elektrodeposita på stål, koppar, nickel och andra metaller.
Konserverad
Tinnaren är elektrodepositionen av tenn. Det är mycket användbart vid produktion av järnburkar, som är täckta med tenn för att göra dem motståndskraftiga mot korrosion, och därmed inte skada maten eller produkterna som lagrar.
Latin eller solbränna
Även om det är lite mer detaljerat, kan mässing och brons också vara elektrodepos på vissa metaller för att förbättra deras utseende.
Zincado
Zink eller zinkgalvanoplastik (inte förvirrande med termisk galvaniserad) används mest för att ge järnmotstånd mot korrosion och ljusare och mer attraktiva ytor. Således är dess funktion estetisk och samtidigt funktionell och finns i kroppsdelar som hjulen.
Metallplast
Plast, som tidigare behandlats för att ha en ledande yta, kan också täckas med metall, vilket är som om de följdes till ett ark aluminiumfolie.
Kan tjäna dig: Kitasato -kolvGalvanoplastik
Galvanoplastik eller elektrodepositioner kan delas upp i funktionella eller estetiska.
Funktionell
 Ett tunt elektrodepos av guld i tittarna på astronauternas fall gör att de kan skydda sina ögon från solljus
Ett tunt elektrodepos av guld i tittarna på astronauternas fall gör att de kan skydda sina ögon från solljus Att belägga en bit eller föremål är att förse sin yta med egenskaper som ensam saknar. Till exempel gör koppar- eller guldelektrodposition de bitar de har, så det är idealiskt i elektroniska kretsar att dra fördel av egenskaperna hos dessa metaller, utan att behöva spendera massor av guld på tillverkningen av hela och solida bitar.
Guld skyddar å andra sidan värme- och strålningsytor. Det är av detta skäl som det används allmänt i satelliterna och i astronauternas hjälmar, eftersom det återspeglar solljuset så att de fördriver deras ögon, eller snabbt heta.
Krom eller nickade stål är mycket resistenta mot korrosion tack just dessa metalllager. Det är därför galvanoplastik används i branschen för att skydda metaller som är känsliga för Corrod.
Estetik
Metallfanér. Zink, nickel och krom används mycket för detta ändamål. Guld och silver är också elektrodepos i ringar, kedjor, armband, chokers, sluttningar, etc., Och därför hittar dess galvanoplastik många tillämpningar i smyckebutiker och prydnader, för att förbättra bilden och prestige i dessa plagg.
Referenser
- Shiver & Atkins. (2008). Oorganisk kemi. (Fjärde upplagan). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Wikipedia. (2021). Galvanisering. Hämtad från: i.Wikipedia.org
- Chris Woodford. (28 juli 2020). Hur elektroplätering fungerar. Hämtad från: Explinthatstuff.com
- Rob Snyder. (s.F.). Nanoskala elektrodeposition. STEM Education Institute. [Pdf]. Återhämtat sig från: nanoskala.Inte ens.Edu
- Elsevier b.V. (2021). Elektroposition. Vetenskaplig. Hämtad från: Scientedirect.com
- Vaishali Mittal. (10 december 2020). Galvanisering. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- Singh Davneet. (9 juni 2020). Olika typer av elektropling. Återhämtat sig från: Teachoo.com
- Helmestine, Anne Marie, PH.D. (26 augusti 2020). Vad är elektroplätering och hur fungerar det? Återhämtat sig från: tankco.com

