Gilbert Newton Lewis
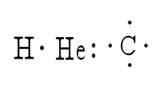
- 1634
- 155
- PhD. Emil Svensson
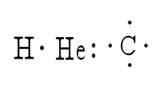 Gilbert Newton Lewis
Gilbert Newton Lewis Gilbert Newton Lewis (1875-1946) var en av de viktigaste amerikanska forskarna under det tjugonde århundradet. Hans arbete producerade en strukturell revolution i kemiska studier tack vare de flera bidrag som han gjorde under hela sitt liv för vetenskapens utveckling.
Bland bidrag från denna fysikalisk -kemiska utmärker formeln som bär hans namn, med vilka paren av elektroner är grafiskt representerade. Lewis forskningsarbete var mycket brett, även om hans berömmelse i princip berodde på teorin om kemiska bindningar och definitionen av syra-bassyra 1923.
Lewis kom att ha stort inflytande på USA: s vetenskapliga och akademiska värld, särskilt vid Harvard University, där ordförande bildades och dikterades. Hans arbete för den amerikanska armén under första världskriget fick honom det största erkännandet och de högsta utmärkelserna.
Det bildades vid universiteten i Nebraska, Harvard, Leipzig och Gontinga i Tyskland. Han arbetade på Massachusetts Institute (MIT), vid Harvard University och vid University of California, där han dog och arbetade.
Under hela sitt liv fick han otaligt erkännande och utmärkelser, bland vilka flera Honoris doktorander i Chicago, Madrid, Liverpool, Wisconsin och Pennsylvania sticker ut. Han var hedersmedlem i flera vetenskapliga institutioner i England, Indien, Sverige, Danmark och USA.
Biografi
Födelse och tidiga år
Gilbert Newton Lewis föddes i Weymouth, Massachusetts, den 23 oktober 1875. Hans föräldrar var Frank Wesley Lewis och Mary Burr White Lewis. Under sina tidiga år fick han läror i sitt eget hem och klockan 10 gick han in i den offentliga skolan, där han tog examen 1889.
1884 var Lewis tvungen att bosätta sig med sin familj i Lincoln, Nebraska. Vid 13 års ålder var han inlagd på gymnasiet vid University of Nebraska.
Kan tjäna dig: Berylliumhydrid (Beh2)Studier
När han tog examen fortsatte han med sina universitetsstudier i två år och registrerade sig sedan vid Harvard University 1893.
Ursprungligen var han intresserad av ekonomin, men valde äntligen fysik och kemi. Gilbert fick sin titel i kemi 1896 och under ett år undervisade han på Phillips Academy, en privatskola för Andover.
Han återvände till Harvard för att göra forskarutbildningen och få magisterexamen 1898 med sin avhandling om Elektronen och en molekyl. Ett år senare fick doktorsexamen och hans avhandling titeln Vissa elektrokemiska och termokemiska förhållanden mellan zink och kadmiumamalgamer".
I Harvard tjänade han som instruktör i ett år och reste sedan till Europa med ett stipendium. Han studerade med tidens stora fysikaliska kemiska.
1899 reste han till Tyskland för att studera med Wilhelm Ostwald Leipzig och sedan med Walter Nernst vid University of Gontinga; Sedan arbetade han för den filippinska regeringen.
Akademiskt arbete och deltagande i krig
Mellan 1999 och 1906 utfärdade han en kemi ordförande vid Harvard University och anlitades sedan av Massachusetts Institute of Technology, där han var från 1907 till 1912.
Senare blev han professor i fysisk kemi vid University of California (Berkeley), där han fick graden av dekan vid School of Chemistry.
1908 publicerade han sin första artikel om relativitetsteorin i parallellism med Albert Einstein. I detta konstaterar det att det finns en koppling mellan energimasa, men i en annan riktning än den som används av Einstein.
Den 21 juni 1912 gifte sig Lewis med Mary Fanckley Sheldon, med vilken han hade tre barn: Margery S. Lewis, Edward S. Lewis och Richard Newton Lewis.
Det kan tjäna dig: Giberélic Acid: Egenskaper, syntes, funktionerHans arbete i Kalifornien avbröts av utbrottet av första världskriget. 1917 fick han i uppdrag att arbeta för den amerikanska armén, där han blev chef för Division of Defense of the Chemical War Service.
Lewis leverans och arbetsförmåga tillät armén. I slutet av kriget tilldelades han för sina tjänster med de högsta utmärkelserna.
Död i laboratoriet
Gilbert n. Lewis dog vid 70 års ålder för en hjärtattack när han arbetade i sitt laboratorium vid University of Berkeley, den 23 mars 1946.
Kanske på grund av dess introverade personlighet fick denna framstående forskare aldrig Nobelpriset. Nästan i slutet av sin karriär lyckades han bevisa att fosforescensen av organiska molekyler styrs av ett upphetsat triplettillstånd, till och med beräkna dess magnetiska egenskaper.
Bidrag till vetenskapen
Några av Gilbert Newton Lewis viktigaste bidrag till vetenskapen är följande:
Lewis -strukturer
De är flera metoder som tjänar till att representera strukturen för en molekyl. I dessa representerar symbolerna för elementen atomer, medan punkterna representerar elektronerna som omger dem. Ett exempel på detta är representationen av väte, helium och kol:
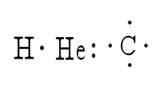
Lewis var den första som föreslog idén att atomer kunde förbli förenade genom att jämföra elektronpar; Det är därför han skapade strukturerna i strukturerna.
Den breda länkteorin som föreslagits av Lewis tjänade till att gruppera i ett koncept alla typer av kemiska länkar. På detta sätt demonstrerades förhållandena mellan joniska, molekylära, kovalenta och metalliska ämnen. Fram till dess hade dessa element inte haft någon konceptuell anslutning.
Kan tjäna dig: typ av länk på 02Kovalent bindning
Konceptualiserade den kovalenta bindningen som bildas mellan två atomer när de går med för att uppnå stabil oktet och dela elektroner på den sista nivån, med undantag för väte, som lyckas nå stabilitet genom att ha 2 elektroner.
Oktetteori
Det anges av Lewis 1916. Detta konstaterar att jonerna som tillhör elementen i det periodiska systemet tenderar att slutföra med ett antal 8 elektroner deras senaste energinivåer. Detta gör att de kan skaffa en mycket stabil konfiguration.
Foton
Det var skaparen 1926 av termen foton för att utse den minsta enheten för ljusenergi. Denna energipartikel överför alla befintliga former av elektromagnetisk strålning (x -rays, infraröd, gamma, ultraviolett, mikrovågor, radiovågor, etc.).
Kemisk attraktion och Valencia
Tillsammans med sin kemiska kollega Irwing Langmir utvecklade han teorin om attraktion och kemisk valens, som kallas Langmuir-Lewis Theory. För detta var det baserat på atomstrukturen hos ämnen.
Kraftigt vatten
Lewis var också den första forskaren som studerade och producerade tungt vatten (deuterium) i sin renaste form. Han var också den första som tillämpade principerna för termodynamik i studien av kemiska problem.
Upplösningsteori
På samma sätt erkänns Lewis sitt arbete om teorin om lösningar; Det vill säga de homogena blandningar som erhållits från interposition av atomer, molekyler eller joner som finns i två eller flera ämnen. Dessa ämnen som kallas komponenter ingriper i proportioner som varierar.

