Halogener
- 3585
- 419
- Johan Gustafsson
 Elementen är 5: fluorid, klor, brom, jod och omarbetning
Elementen är 5: fluorid, klor, brom, jod och omarbetning Vad är halogener?
De halogener De är icke -metalliska element som tillhör grupp VIIA eller 17 i det periodiska tabellen. De har höga elektroniska elektronegativiteter och affiniteter, som har starkt påverkat den joniska karaktären hos deras bindningar med metaller. Ordet "halogenos" är av grekiskt ursprung och betyder "salter av salter".
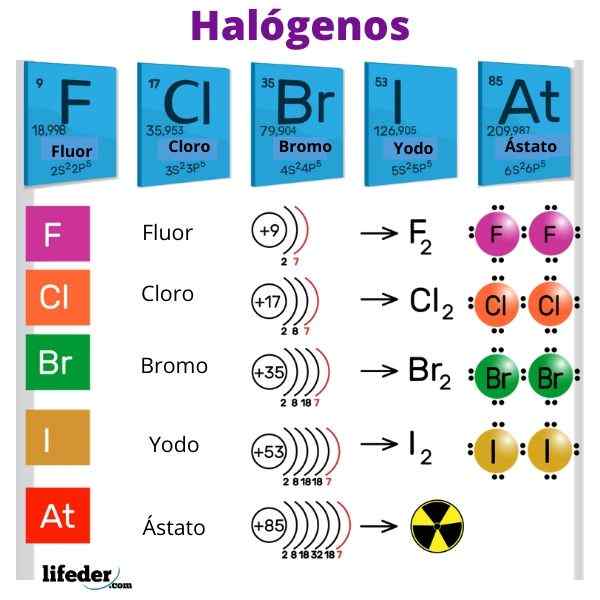
Halogenerna är fluor (F), klor (CL), brom (BR), jod (I) och det radioaktiva och flyktiga elementet Ástato (AT). De är så reaktiva att de reagerar med varandra för att bilda diatomiska molekyler: F2, Kli2, Bras2, Yo2 och vid2.
Dessa molekyler kännetecknas av att ha liknande strukturella egenskaper (linjära molekyler), även om de med olika fysiska tillstånd.
Vad är utseendet på halogener?
I den nedre bilden visas tre halogener. Från vänster till höger: klor, brom och jod. Varken fluor eller jantate kan förvaras i glasbehållare, eftersom de senare inte motstår deras korrosivitet. Observera hur de organoleptiska egenskaperna hos halogener förändras när deras grupp är härstammad till jodelementet.
 Halogener utseende. Källa: Källa: av W. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)], via Wikimedia Commons
Halogener utseende. Källa: Källa: av W. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)], via Wikimedia Commons Fluor är en gas med gulaktiga toner; Klor också, men gulgrön; Bromo är en mörkrödvätska; Joden, ett svart fast ämne med violetta visos; Och astaten, ett mörkt och ljust metalliskt fast ämne.
Halogenerna kan reagera med nästan alla element i det periodiska bordet, även med några ädla gaser (som Xenon och Kripton). När de gör det kan de oxidera atomer till sina mest positiva oxidationstillstånd, vilket gör dem till kraftfulla oxiderande medel.
På samma sätt ger de specifika egenskaper till molekyler när några av deras atomer är kopplade eller ersättas. Dessa typer av föreningar kallas haluros. I själva verket utgör haluros den huvudsakliga naturliga källan till halogener, och många av dem löses i havet eller är en del av ett mineral; Sådant är fallet med fluorit (CAF2).
Både halogener och haluros har ett brett utbud av användningsområden, från industriell eller teknisk, för att helt enkelt lyfta fram smaken på vissa livsmedel, som pärlsaltet (natriumklorid) gör (natriumklorid).
Fysiska och kemiska egenskaper hos halogener
Atomvikter
Fluorid (F) 18,99 g/mol; Klor (Cl) 35,45 g/mol; Bromo (BR) 79,90 g/mol; Jod (i) 126,9 g/mol och astato (vid) 210 g/mol.
Fysiskt tillstånd
F gas; Gaseous cl; Flytande; Jag är solid och solid.
Färg
F, blekgul-slipning; Cl, blekgrön; Br, rödbrun; Jag, violet och på, metallisk svart * * (antagen)
Fusionspunkter
F -219.6º C; Cl -101,5º C; BR -7,3º C; I 113,7 ° C och vid 302 ° C.
Kokpunkter
F -118,12º C; Cl -34,04º C; BR 58,8º C; I 184,3º C och ?Vid 337 ° C.
Densitet vid 25 ° C
F- 0,0017 g/cm3; CL- 0,0032 g/cm3; BR- 3,102 g/cm3; I- 4,93 g/cm3 och AT- 6.2-6,5 g/cm3
Vattenlöslighet
Cl- 0,091 mmol/cm3; BR- 0,21 mmol/cm3 och I- 0,0013 mmol/cm3.
Joniseringsenergi
F- 1.681 kJ/mol; Cl- 1.251 kJ/mol; BR- 1,140 kJ/mol; I- 1 008 kJ/mol och vid 890 kJ/mol.
Elektronnegativitet
F- 4.0; Cl- 3.0; 2,8; I- 2,5 och AT-2,2.
Halogenerna har 7 elektroner i sitt valensskikt, därmed deras stora aviditet för att vinna en elektron. Halogener har också hög elektronegativitet på grund av deras små atomradio och den stora attraktion som kärnan på elektronerna i Valencia utövar.
Kan tjäna dig: Mass Action LawReaktivitet
Halogener är mycket reaktiva, vilket då skulle förklara deras toxicitet. Dessutom oxiderar de agenter.
Den minskande ordningen av reaktivitet är: f> cl> b> i> vid.
Stat i naturen
På grund av deras stora reaktivitet är halogenatomer inte fria i naturen, men bildar aggregat eller som diatomiska molekyler kopplade av kovalenta bindningar.
Molekylstrukturer
Halogener finns inte i naturen som elementära atomer, men som diatomiska molekyler. Men de har alla gemensamt en linjär molekylstruktur, och den enda skillnaden ligger i längden på deras länkar och i deras intermolekylära interaktioner.
De x-x linjära molekylerna (x2) De kännetecknas av att vara instabila, eftersom båda atomerna lockar starkt elektronparet till dem. Därför att? Eftersom dess externa elektroner upplever en mycket hög effektiv kärnbelastning, ZEF. En stor zef, mindre kommer att vara avståndet till X-X-länken.
När gruppen går ner blir Zef svagare och stabiliteten hos dessa molekyler ökar. Således är den minskande ordningen av reaktivitet: f2> Cl2> BR2> I2. Det är emellertid inkongruöst att jämföra ostaten med fluor, eftersom det är okänt isotop.
Intermolekylär interaktioner
Å andra sidan saknar dess molekyler ett dipolmoment och är apolär. Detta faktum är ansvarigt för dess svaga intermolekylära interaktioner, vars enda latenta kraft är spridning eller London, vilket är proportionellt mot atommassa och molekylområde.
På detta sätt2 har inte tillräckligt med massa eller elektroner för att bilda ett fast ämne. Till skillnad från i2, Jodmolekylen, som ändå fortsätter att vara ett fast ämne som avger lila ångor.
Bromo representerar ett mellanliggande exempel mellan båda ändarna: BR -molekyler2 De interagerar tillräckligt för att dyka upp i ett flytande tillstånd.
Restaten, troligen på grund av dess växande metalliska karaktär, presenterar sig inte som vid2 Men som atomer i Athe som bildar metalllänkar.
Beträffande dess färger (gulgul grönröd-mudad-negro) är den mest lämpliga förklaringen baserad på molekylära orbitalteorin (TOM). Energiavståndet mellan den sista fulla molekylära orbitalen och nästa av större energi (antienlace) överskrids genom absorption av en foton med allt större och större våglängder.
Haluro
Halogener reagerar på att bilda haluros, vare sig det är oorganiskt eller organiskt. De mest kända är vätehalogenider: vätefluorid (HF), väteklorid (HCl), vätebromid (HBR) och vätejodid (HI).
Alla upplösta i vattengenererar syralösningar; Så surt, att HF kan försämra alla glasbehållare. Dessutom beaktas utgångsmaterial för syntes av extremt starka syror.
Det finns också de så kallade metallhalogeniderna, som har kemiska formler som beror på metallen Valencia. Till exempel har alkaliska metallhalider MX -formel, och bland dem är: NaCl, natriumklorid; KBR, kaliumbromid; CSF, cesiumfluorid; och LII, litiumjodid.
De alkalinoteriska metallerna, övergångsmetallerna eller metallerna i P -blocket har en MX -formeln, N är den positiva metallbelastningen. Således är några exempel på dem: FECL3, järntric triklorid; Mgbr2, magnesiumbromid; Alf3, Aluminium trifluoruro; och cui2, Kopparjodid.
Kan tjäna dig: kaliumsulfat (K2SO4): Struktur, egenskaper, användningar, syntesHalogener kan emellertid också bilda kopplingar till kolatomer; Därför kan de störa den komplexa världen av organisk kemi och biokemi. Dessa föreningar kallas organiska halider och är i allmänhet kemisk formel, som är x någon av halogenerna.
Användning/halogenapplikationer
Klor
Inom industrin
-Bromo och klor används i textilindustrin för att bleka och behandla ull, vilket undviker din krympa när du blir våt.
-Det används som en Ditritus -desinfektionsmedel och för rening av dricksvatten och pooler. Dessutom används klor -härledda föreningar i tvättstugor och inom pappersindustrin.
-Hitta användning vid tillverkning av specialbatterier och klorerade kolväten. Det används också vid bearbetning av kött, grönsaker, fisk och frukt. Klor fungerar också som bakteriedödande medel.
-Det används för att rengöra och avfärda läder och för att bleka cellulosa. Tidigare användes kväve triklorid som mixer och mjölkonditionering.
-Fosfengas (cocl2) Det används i många industriella syntesprocesser, liksom i tillverkningen av militära gaser. Fosfanen är mycket giftig och ansvarar för många dödsfall under första världskriget, där gas användes.
-Denna gas finns också i insekticider och rökmedel.
-NaCl är ett mycket rikligt salt som används för att krydda mat och i bevarande av nötkreatur och fågelkött. Dessutom används det i kroppsliga rehydratiseringsvätskor, både oralt och intravenöst.
Inom medicin
-Halogenatomer som binder till läkemedel gör dem mer lipofila. Detta gör att läkemedel kan gå igenom lättare cellmembran som upplöses i lipiderna som bildar det.
-Kloren sprids i det inre av neuronerna i det centrala nervsystemet genom joniska kanaler kopplade till neurotransmitteren GABA -receptorer, vilket ger en lugnande effekt. Detta är verkningsmekanismen för flera ångestdik.
-HCL är närvarande i magen, där den ingriper och skapar en reducerande miljö som gynnar matbearbetning. Dessutom aktiverar HCl pepsinen, ett enzym som börjar hydrolysen av proteinerna, ett steg före tarmsabsorptionen av proteinmaterialet.
Andra
-Saltsyran (HCl) används för att rengöra badrummen, i undervisning och forskningslaboratorier och i många branscher.
-PVC (polyvinylklorid) är en vinylkloridpolymer som används i kläder, golv för golv, elektriska kablar, flexibla rör, rör, uppblåsbara strukturer och takplattor. Dessutom används klor som mellanhand i utarbetandet av andra plastmaterial.
-Klor används i bromsextraktion.
-Metylklorid uppfyller en bedövningsfunktion. Det används också vid utarbetandet av vissa silikonpolymerer och vid utvinning av fetter, oljor och hartser.
-Kloroform (CHCL3) är ett lösningsmedel som används i många laboratorier, särskilt i organiska och biokemi kemi laboratorier, från undervisning, till forskare.
-Och slutligen, med avseende på klor, används trikloretylen för att avfett metalldelar.
Brom
-Bromo används i guldbrytningsprocessen och i borrningen av olje- och gasbrunnar. Det används som en förbränningsskyddare inom plast- och gasindustrin. Bromo isolerar syrebranden som får den att stänga av.
Kan tjäna dig: Natriummetabisulfite (Na2S2O5): Struktur, egenskaper, användningar, risker-Det är en mellanhand i tillverkningen av hydrauliska vätskor, kylmedelsmedel och avfuktare och beredda att forma hår. Kaliumbromid används vid tillverkning av plattor och fotografiska papper.
-Kaliumbromid används också som antikonvulsiv, men på grund av möjligheten att salt kan orsaka neurologiska dysfunktioner har dess användning reducerats. Dessutom är en annan av dess vanliga användningsområden som ett piller för fasta prover av infraröd spektroskopi.
-Bromo -föreningar finns i mediciner som används vid lunginflammationsbehandling. På samma sätt införlivas bromföreningar i läkemedel som används i testerna som utförs i behandlingen av Alzheimers sjukdom.
-Bromo används för att minska kvicksilverföroreningar i elektriska växter som använder kol som bränsle. Det används också i textilindustrin för att skapa olika färgfärgämnen.
-Metylbrominat användes som bekämpningsmedel för rökning av jord och hem, men dess skadliga effekt på ozon har begränsat dess användning.
-Halogenlampor är glödande och aggregatet av små mängder brom och jod möjliggör en minskning av glödlamporna.
Jod
-Jod ingriper i funktionen av sköldkörteln, kroppsmetabolismreglerande hormon. Sköldkörteln hemligheter hormonerna T3 och T4, som utövar deras handling på deras vita organ. Till exempel orsakar hormonell verkan på hjärtmuskeln en ökning av blodtrycket och hjärtfrekvensen.
-På samma sätt används jod för att identifiera närvaron av stärkelse. Silver Yoduro är ett reagens som används i uppenbarelsen av fotografierna.
Fluor
-Vissa fluoridföreningar läggs till tandpasta för att förhindra kariesutseende. Fluorderivat finns i flera bedövningsmedel. I läkemedelsindustrin integrerar de fluor till läkemedel för att studera möjliga förbättringar på deras effekter på kroppen.
-Fluorhorinsyra används för att spela in glas. Även i produktionen av haloner (brandsläckare gaser, till exempel yngel). En fluoridförening används i aluminiumelektrolys för att uppnå dess rening.
-Antirreflejantes -beläggningar innehåller en fluorförening. Detta används vid tillverkning av plasmaskärmar, plattskärmar och mikroelektromekaniska system. Fluor finns också i leran som används i vissa keramik.
Röda
Man tror att restatet kan bidra till jod i regleringen av sköldkörteln. Dessutom dess radioaktiva isotop (210Vid) har använts i cancerstudier hos möss.
Referenser
- Encyclopedia of Health and Safety på jobbet. Halogener och dess föreningar. [Pdf]. Tagen från:
- sysselsättning.Gabb.är
- Kemi librettexts. Grupp 17: Allmänna egenskaper för halogener. Taget från: Chem.Librettexts.org
- Wikipedia. (2018). Halogen. Taget från: i.Wikipedia.org
- Jim clark. (Maj 2015). Atomiska och fysiska egenskaper hos grupp 7 -element (halogenerna). Taget från: Chemguide.co.Storbritannien
- Whitten, K. W., Davis, r. OCH., Peck, m. L. Och Stanley, G. G. Chemistry (2003), 8: e upplagan. Cengage Learning.
- Föremål. Halogener. Taget från: element.org.är
- Brun, lagrar. (24 april 2017). Halogenegenskaper. Forskning. Återhämtat sig från: forskning.com

