Aromatiska kolvätenegenskaper, exempel, applikationer
- 4971
- 792
- PhD. Emil Svensson
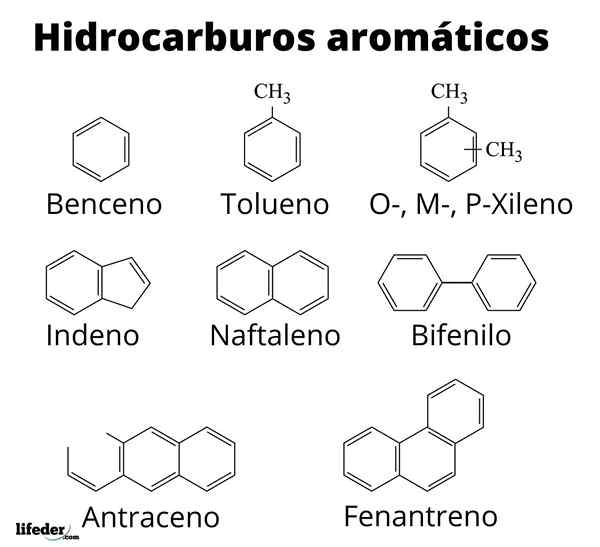
De aromatiska eller sandkolonben De är en uppsättning organiska föreningar som endast är sammansatta av kol och kolhyden, och som kännetecknas av att ha enheter av bensenringar i sina molekylstrukturer.
Vissa, som hans namn betonar, skjuter söta och trevliga luktar; Anledningen till att de första organiska kemikalierna hänvisade till dem som aromatiska. Metangas, till exempel, är ett toalettväte; Medan toluen, flyktig vätska, presenterar en ganska speciell och stark lukt.
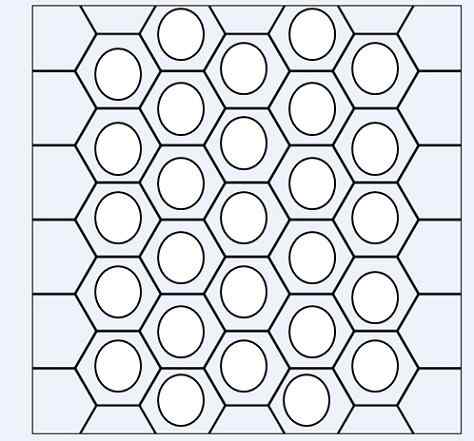 Aromatiska kolväten erkänns av Benncytenic Rings -enheter
Aromatiska kolväten erkänns av Benncytenic Rings -enheter I den övre bilden har vi ett slags nätverk eller nät som består av benseniska ringar. Notera dina hexagonala geometrier och cirkeln inuti. Denna cirkel representerar det som kallas aromatiskhet, som är en helt kemisk och icke -fysisk egenskap, oberoende av lukten av dessa kolväten.
Aromatiska kolväten är bland de viktigaste, extraherade eller producerade olje- och kolmineralerna. Benzen är hörnstenen i dessa kolväten och deras tillämpningar, eftersom från den härstammar symfiner av föreningar som används som råmaterial för produktion av gödselmedel, plast, lim, tvättmedel, parfymer, mediciner, etc.
[TOC]
Hur heter aromatiska kolväten?
En enda bensenring
För aromatiska kolväten har vi den egenhet som deras traditionella eller vanliga namn vanligtvis råder över de som styrs av IUPAC -nomenklaturen.
Alla innehåller bensenringen, eller en ring som möter aromaticitetsegenskapen. Det enklaste kan namnges enligt bensen och de relativa positionerna för deras substituenter.
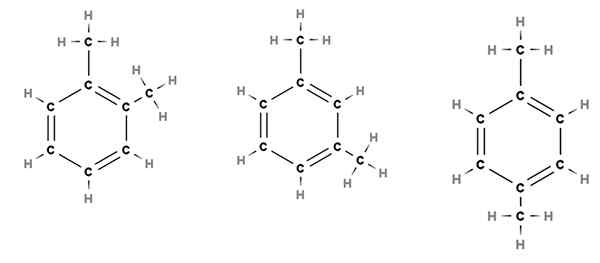 Relativa positioner för substituenterna i en bensenisk ring för dimetylbensenmolekylen. Källa: Gabriel Bolívar via Molview.
Relativa positioner för substituenterna i en bensenisk ring för dimetylbensenmolekylen. Källa: Gabriel Bolívar via Molview. Tänk till exempel på den övre bilden. I de tre strukturerna ser vi bensenens hexagonala ring, som har två metylsubstituenter, CHO3. Således kallas denna förening dimetylbensen, eftersom den består av en bensen med två metylos.
Kan tjäna dig: kaliumsulfat (K2SO4): Struktur, egenskaper, användningar, syntesFrån vänster till höger ser vi att separationen mellan de två3 Det blir större, vilket inte bara påverkar molekylens fysiska egenskaper, utan ändrar också deras respektive namn. För att differentiera dem, eftersom de alla kallas dimetylbensen används orto-prefix (O-), mål (m-) och för (p-) (p-).
Därför, och återigen, från vänster till höger har vi: orto-dimetylbensen, meta-dimetylbensen och parameterbensen. Det traditionella namnet för denna förening är emellertid xylen, så namn blir: orto-xylen, meta-xylen och para-xylen.
Om det finns mer än två olika substituenter används det för att räkna upp kol efter samma nomenklaturregler som för alla kolväten.
Flera ringar
För aromatiska kolväten med mer än en bensenisk ring blir traditionella namn ännu viktigare. Detta beror på att de systematiska namnen som beskriver deras strukturer är besvärliga och svåra att memorera. Tänk på exemplet med naftalen:
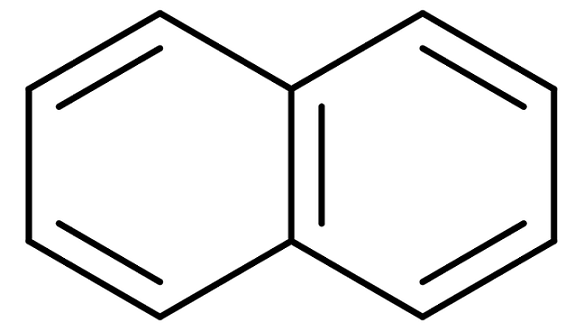 Naftalenstruktur
Naftalenstruktur Naftalen är också kommersiellt känd som naftalin eller vit kamfer. Emellertid är dess systematiska namn: Biciclo [4,4,0] dec-1,3,5,7,9 Pentane. Och detta endast för en förening med två sammanslagna benseniska ringar; Nomenklaturen blir mycket mer komplicerad för föreningar med tre eller fler ringar.
Egenskaper hos aromatiska kolväten
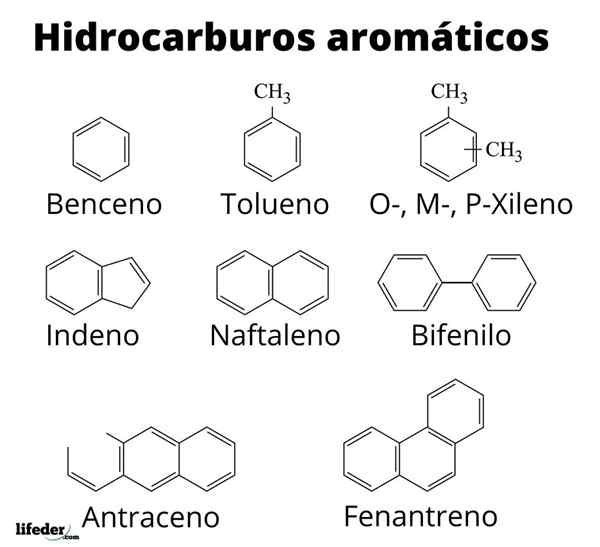 Struktur av vissa aromatiska kolväten
Struktur av vissa aromatiska kolväten Aromatiskhet
Aromatiska kolväten innehåller ringar som följer Huckel -reglerna. Det vill säga deras ringar måste ha atomer med SP -hybridiseringar2, vara så platt som möjligt och ha ett antal elocerade π -elektroner lika med 4n + 2. Till exempel är bensen aromatisk eftersom den har 6 demokerade elektroner för n= 1 (4 · 1 + 2 = 6).
Höga C/H -relationer
C/H -relationer för aromatiska kolväten är höga eller större än 1. Till exempel för bensen, c6H6, Din C/H är lika med 6/6 eller 1. Under tiden för naftalen, c10H8, Din C/H är lika med 10/8 eller 1.25. Vad betyder det här? Att dessa kolväten är mycket "kolsyrade" jämfört med andra föreningar.
Kan tjäna dig: sulfonsyra: struktur, nomenklatur, egenskaper, användningarGula lågor
Precis på grund av deras höga C/H -förhållanden, när aromatiska kolväten bränns eldgula lågor, bildas produkten av kolpartiklarna (sot).
Ersättningsreaktioner
Aromatiska kolväten kan ersätta sina väteatomer med någon annan substituent. Detta uppnås genom två typer av organiska reaktioner: aromatisk elektrofil substitution (Sear) eller aromatisk nukleofil substitution (SNAR).
Doft
Aromatiska kolväten, som deras namn antyder, kännetecknas av att ha söta eller starka dofter. Den här egenskapen tillät dem att i princip differentiera dem från gasformiga kolväten och några paraffiner.
Exempel på aromatiska kolväten
Aromatiska kolväten, berör strikt sett endast de som består av kol och väte. Det bör inte finnas några heteroátomos (eller, p, n, s, etc.). Därför lämnar följande exempel som kommer att nämnas ut till föreningar som pyridin, furano eller fenol.
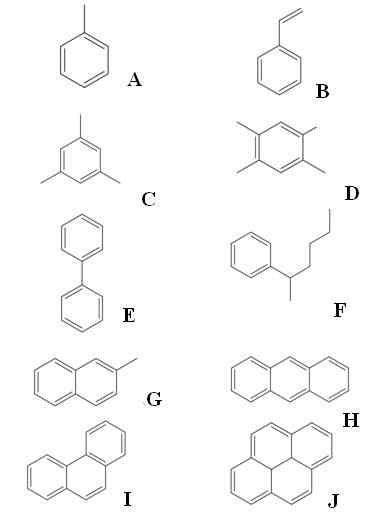 Exempel på aromatiska kolväten. Källa: Gabriel Bolívar via Molview.
Exempel på aromatiska kolväten. Källa: Gabriel Bolívar via Molview. Upp vi har tio exempel på aromatiska kolväten. Observera att alla har minst en bensenisk ring. Deras namn är:
A: Toluen
B: Sträck
C: mesitileno
D: sent
E: bifenyl
F: 2-Fenilhexan
G: 2-metylnaftalen
H: Anthracen
I: Fenantreno
J: Pireno
Av dem alla är Toluene den med det största industriella värdet.
Applikationer/användningar
De flesta tillämpningar av aromatiska kolväten består av att tjäna som råmaterial för syntes eller produktion, produkter med högt kommersiellt värde. Nästan alla börjar från Benzene, som utsätts för flera organiska reaktioner för att erhålla funktionella derivat.
Fibrer och plast
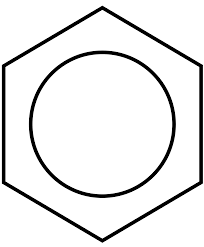 Bensen
Bensen Från bensen finns cyklohexan, som därefter omvandlas till andra föreningar för att syntetisera nylon 6 eller nylon 66. Å andra sidan kan sträckan också erhållas från bensen, som består av polystyrenmonomeren. Således har vi polymerer som är nödvändiga för produktion av fibrer och plast.
Kan tjäna dig: aktiveringsenergiEpoxihartser
Från bensen kan också bisfenol A syntetiseras, med vilka efter olika syntesvägar, epoxihartser, lim, lim och till och med målningar förekommer.
Tvättmedel
Alkybentes med långsiktiga kedjor tjänar för produktion av tvättmedel; Bland dem, alkybenzeosulfonates.
Tnt
Från toluen kan du producera TNT: trinitrotoluen, en av de mest kända sprängämnena.
Bensoesyra
Från toluen erhålls bensoesyra som härledd, väsentlig förening för formuleringarna av många parfymer, mediciner och mat.
Lösningsmedel
Benzen, Toluene och Xileno (BTX), är de mest använda organiska lösningsmedlen inom oljeforskning.
Bensin
Aromatiska kolväten är också en del av sammansättningen av bensin, med huvudrollen att höja sitt oktan- eller oktanindex.
Referenser
- Graham solomons t.W., Craig b. Fryhle. (2011). Organisk kemi. (10th Utgåva.). Wiley Plus.
- Carey f. (2008). Organisk kemi. (Sjätte upplagan). MC Graw Hill.
- Morrison och Boyd. (1987). Organisk kemi. (Femte upplagan). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Aromatisk förening. Hämtad från: i.Wikipedia.org
- ED Vitz et al. (8 september 2020). Aromatiska kolväten. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- Wyman Elizabeth. (2020). Aromatiska kolväten: Definition, exempel och användning. Studie. Återhämtat sig från: studie.com
- Boluda, c. J., Macías, m., & González Marrero, J. (2019). Den kemiska komplexiteten hos fordonsbensin. Vetenskap, teknik och applikationer,2(2), 51-79. Doi: doi.org/10.22206/CYAP.2019.V2i2.Pp51-79
- « Bevarande av den linjära momentia -principen, exempel, övningar.
- Böner med G -exempel och användningsregler »

