Alkalinetermetaller
- 3974
- 154
- Anders Svensson
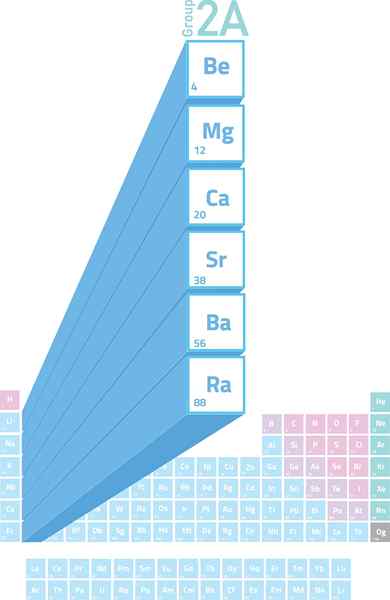
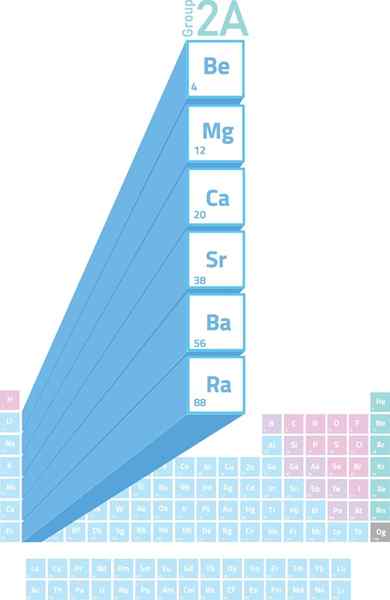 Plats för alkalinoterösa metaller i det periodiska tabellen
Plats för alkalinoterösa metaller i det periodiska tabellen Vad är alkalinellt metaller?
De Alkalinetermetaller De är elementen i grupp 2 (tidigare kallad grupp 2a) i det periodiska tabellen. Det vill säga att de bildas av de 6 elementen i den andra kolumnen i den periodiska tabellen som sträcker sig från Beryllium (BE) till radion (RA).
De är en grupp av ganska reaktiva och relativt vanliga metallelement. De har bara två valenselektroner belägna i en orbital. Av denna anledning tillhör de block S i det periodiska tabellen.
Namnet "Alkalinoterreo" kommer från föreningen av "alkaliska" ord, som är ett annat sätt att säga grundläggande och jorden, vilket är hur de fick höra innan oxider. Så alkalinoterösa metaller betyder bokstavligen metaller som bildar basoxider.
Dessa metaller har många tillämpningar som gör dem viktiga i vårt nuvarande samhälle, särskilt magnesium. Dessa applikationer beror på deras specifika egenskaper, som beskrivs nedan.
Egenskaper hos alkalinoterösa metaller
De har metallutseende
Alla alkalinoteriska metaller har silverfärg med metallisk ljusstyrka. Radonen är också radioaktiv så att den lyser i den mörka avger ett karakteristiskt grönt ljus.
De är små täta metaller
Alla alkalinoterösa metaller är tätare än vatten, men är mindre täta än de flesta andra metallelement i det periodiska bordet.
Densiteterna i denna grupp sträcker sig från 1,54 g/cm3 För kalcium upp till 5,5 g/cm3 För radion, som är betydligt mindre än tätheten hos andra metaller som järn (7,9 g/cm3), koppar (9,0 g/cm3), bly (11,3 g/cm3) och El Mercurio (13,5 g/cm3), för att nämna några.
De har relativt låga smält- och kokpunkter
Att vara metaller, dess smält- och kokpunkter är större än de flesta icke -metaller. De är emellertid lägre än fusions- och kokpunkterna för de flesta andra metaller, med några undantag.
Kan tjäna dig: Arrhenius -ekvationDe har Valencia +2
På grund av deras elektroniska konfiguration tenderar dessa metaller att förlora två elektroner när de reagerar med andra element som icke -metaller. Av denna anledning är hans enda Valencia +2.
De är relativt reaktiva
Alkalinoterösa metaller är mycket mer reaktiva än metaller såsom järn eller koppar, men är mindre reaktiva än alkaliska metaller (elementen i grupp 1). Ju lägre gruppen, desto mer reaktiv är metallen.
Till exempel reagerar beryllium (gruppens första) inte med vatten medan följande två kan reagera med varmt vatten och de sista kan till och med reagera med kallt vatten.
Reagera med luft för att bilda grundläggande oxider
Dessa metaller tenderar att bilda grundläggande oxider när de reagerar med luftsyre. I själva verket är det därför de kallas alkaliners. Dessa oxider, när de löses i vatten, blir hydroxider som producerar alkaliska eller grundläggande lösningar.
Alkalinotera metallapplikationer
Inom teknikbranschen
Några av de alkalinoteriska metallerna används vid halvledartillverkning. Dessa är viktiga i konstruktionen av elektroniska kretsar som de som innehåller praktiskt taget alla moderna elektriska apparater, från datorer och mobiltelefoner, till tvättmaskiner, bilar och andra.
I livsmedelsindustrin
Kalcium är ett viktigt näringsämne för livet. Det är en del av benens struktur och har andra viktiga funktioner i kroppen. Av denna anledning tillsätts detta element som en befästare till många mat från spannmål till mejeriprodukter. Dessutom används det också i osttillverkning.
Det kan tjäna dig: cirkonium: historia, egenskaper, struktur, risker, användningarI bilindustrin
Några av de alkalinoteriska metallerna har mycket bra mekaniska egenskaper, vilket innebär att de är hårda och resistenta. Dessutom är de korrosionsbeständiga, så de används ofta vid tillverkning av lyxhjul för bilar såväl som andra delar av dem.
I militärindustrin
På grund av deras mekaniska egenskaper och låg densitet används metaller såsom magnesium och beryllium vid konstruktion av stridsflygplan, satelliter och helikoptrar.
På grund av deras elektriska egenskaper används de också för tillverkning av olika typer av sensorer och optiska och elektroniska system som den militära industrin använder för att skapa vapen och kommunikationssystem.
De sex alkaliska metallerna
Det finns bara sex alkaliska metaller. Därefter finns det en kort beskrivning av var och en av dem:
Beryllium (BE)
Det är elementnummer 4 i det periodiska tabellen och den första av gruppen av alkalinoterösa metaller. Det är en mycket lätt, stark metall med unika egenskaper som gör den användbar vid tillverkning av halvledare.
Magnesium (mg)
Magnesium är en relativt lätt silvermetall, med en låg smält- och kokpunkt (jämfört med andra metaller). Det är mycket hårt och resistent och används ofta vid tillverkning av bildelar och som ett tillsatsmedel i beredningen av legeringar såsom vissa typer av stål.
Det är den andra alkalinother metall och element nummer 12 i det periodiska tabellen. Liksom andra element i denna grupp är det ett viktigt näringsämne för livet.
Kalcium (CA)
Kalcium är det femte vanligaste elementet i jordens cortex. Det finns som kalciumkarbonat i många mineraler och stenar och är också ett väsentligt element för livet på grund av dess deltagande i bildandet av ben och dess betydelse i nervsystemet.
Kan tjäna dig: strontiumklorid (SRCL2)Denna metall är element nummer 20 i det periodiska tabellen, är i den fjärde perioden och är den tredje alkalinother metallen.
Strontium (SR)
Elementnummer 38 och fjärde alkaliska metallen är strontium. Det är tyngre än kalcium, men det verkar mycket när det gäller dess kemiska och fysiska egenskaper. I själva verket kan strontium ersätta kalcium i ben.
Detta är särskilt problematiskt när vi utsätter oss för radioaktivt strontium som inträffar efter en kärnreaktion, eftersom det är mycket svårt att eliminera från kroppen och förgiftar oss med strålning lite efter att hålla fast vid benen.
Barium (BA)
Detta element har atomnummer 56 och har också egenskaper som är ganska lik kalcium och strontium. Det är en ganska mjuk och mycket reaktiv metall som inte är elementär. Det är en av de alkalinoterösa metallerna med större metallkaraktär.
Radio (RA)
Det sista elementet i Alcalinoterreos -gruppen är radio, en radioaktiv metall (därmed dess namn) som avger ett svagt grönt ljus som är lätt att observera i mörkret.
Det brukade användas mycket vid beredningen av målningar som lyser i mörkret, men efter att risken för hälsa upptäcktes var dess användning förbjuden.

