Quiraral rankic blandning, exempel
- 2988
- 166
- Anders Svensson
En Racmisk blandning O RACMATICS är den som består av två enantiomerer i lika delar och är därför optiskt inaktiv. Denna optiska aktivitet avser förmågan hos sina lösningar att rotera, i ett schema eller anti -folie, en stråle av polariserat ljus som reser genom dem i en riktning.
En enantiomer har förmågan att rotera det polariserade ljuset, säg till vänster (Levógiro), så dess rena lösning kommer att vara optiskt aktiv. Men om detta börjar lägga till enantiomeren som roterar ljuset till höger (dextrogyr) kommer dess optiska aktivitet att minska tills den är inaktiverad.
 Druvkluster, som delar ett släktskap med rankiska blandningar utöver etymologi. Källa: Pexels.
Druvkluster, som delar ett släktskap med rankiska blandningar utöver etymologi. Källa: Pexels. När detta händer sägs det att det finns samma mängder av Levogiro- och Dextrógiro -enantiomererna; Om en molekyl bruten det polariserade ljuset till vänster kommer dess effekt att avbrytas omedelbart när den är "snubblar" med en annan molekyl som roterar den till höger. Och så vidare. Därför kommer vi att ha en rankic blandning.
Den första förbättringssynen gjordes av den franska kemisten Louis Pasteur 1848, som studerade en blandning av enantiomer kristaller av vinsyra (vid den tiden kallad rankinsyra). När denna syra från druvorna som används för vinproduktion, slutade denna blandning på ett allmänt sätt för alla molekyler.
[TOC]
Skor och kiralitet
För det första finns det en resonemangsblandning, det måste finnas två enantiomerer (vanliga), vilket innebär att båda molekylerna är kiraler och att deras spegelbilder inte är överlappbara. Ett par skor illustrerar detta perfekt: oavsett hur mycket den vänstra skon försöker till höger kan de aldrig passa.
Kan tjäna dig: svag syraDen högra skon, för att säga, avleder det polariserade ljuset till vänster; Medan den vänstra skon gör det till höger. I en hypotetisk lösning där skor är molekylerna, om det bara finns rättigheter skor, chirals, kommer detta att vara optiskt aktivt. På samma sätt kommer det att hända om det bara finns vänsterskor i lösning.
Men om det finns tusen vänsterskor blandade med tusen rättighetsskor, finns det då en rankisk blandning, som också är optiskt inaktiv, eftersom avvikelserna som lidit av ljuset inuti avbryts ömsesidigt.
Om de istället för skor var bollar, föremål som är akvirala, skulle det vara omöjligt för dem att existera rankiska blandningar av dessa, eftersom de inte ens skulle kunna existera som en enantiomer par.
Exempel
Vinsyra
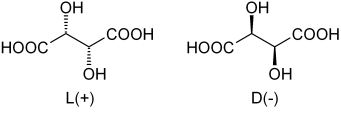 Vinsyra -enantimer. Källa: Dschanz [Public Domain]
Vinsyra -enantimer. Källa: Dschanz [Public Domain] Återvända till vinsyra var dess rankic blandning den första som träffades. I den övre bilden visas dess två enantiomerer, var och en kan bilda kristaller med morfologiska ansikten av "vänster" eller "höger". Pasteur, genom att hjälpa ett mikroskop och en rigorös ansträngning, lyckades separera dessa enantiomerkristaller från varandra.
Kristallerna i enantiomererna l (+) och d (-) separat, presentera optisk aktivitet genom att avleda det polariserade ljuset till höger eller vänster, respektive. Om båda kristallerna i samma molära proportioner upplöses i vatten, kommer en optiskt inaktiv rankisk blandning att erhållas.
Observera att båda enantiomererna har två chirala kol (med fyra olika substituenter). I L (+) ligger OH bakom planet som bildas av kolskelettet och COOH -grupperna; Medan i d (-) dessa OH är ovanför nämnda plan.
De som syntetiserar vinsyra kommer att få en rankic blandning. För att separera enantiomer l (+) från d (-) är en quiral upplösning nödvändig, där denna blandning reageras med en kiral bas för att producera diasteroisomere-salter, som kan separera sedan genom fraktionskristallisation.
Kan tjäna dig: kopparsulfid: struktur, egenskaper, användningarKinin
 Kininmolekyl. Källa: Benjah-Bmm27.
Kininmolekyl. Källa: Benjah-Bmm27. I det föregående exemplet, för att hänvisa till en rankic blandning av vinsyra, är den vanligtvis skriven som syra (±) -tartarisk. Således, i fallet med kinin (överlägsen bild) kommer det att vara (±) -quinina.
Kininens isomeria är komplex: den har fyra chirala kol, vilket ger upphov till sexton diasteroisomerer. Intressant nog är två av dess enantiomerer (en med OH ovanför planet och den andra under det) faktiskt diasthelisomerer, eftersom de skiljer sig åt i konfigurationerna av sina andra chirala kol (de på cykeln med N -atomen för N).
Nu är det svårt att specificera vilka av stereoisomererna i kininet som kommer att avleda det polariserade ljuset till höger eller till vänster.
Talidomid
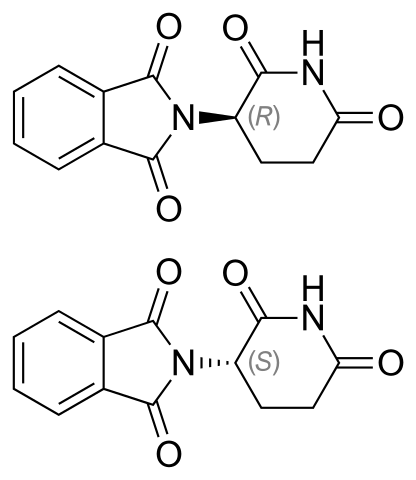 Talaidomide -enantimerer. Källa: Vaccinationist [Public Domain]
Talaidomide -enantimerer. Källa: Vaccinationist [Public Domain] Talidomid -enantiomerer visas ovan. Den har bara ett quiralt kol: det som är kopplat till kväve som går med i båda ringarna (en av Phthalimida och den andra av gluteramid).
I enantiomeren R (med lugnande egenskaper) är fthalimida -ringen (den till vänster) orienterad ovanför planet; Medan du är i enantiomer (med mutagena egenskaper), nedan.
Procenten av de två är inte känd, vilken av de två avleder ljuset till vänster eller höger. Det som är känt är att en blandning 1: 1 eller 50% av båda enantiomererna bildar den rankiska blandningen (±) -talidomid.
Om du bara vill marknadsföra talidomiden som ett hypnotiskt lugnande medel är det obligatoriskt att skicka sin rankic -blandning till den redan nämnda chirala upplösningen, så att den rena enantiomeren erhålls.
Kan tjäna dig: kvartära föreningar: egenskaper, träning, exempel1,2-epoxipropan
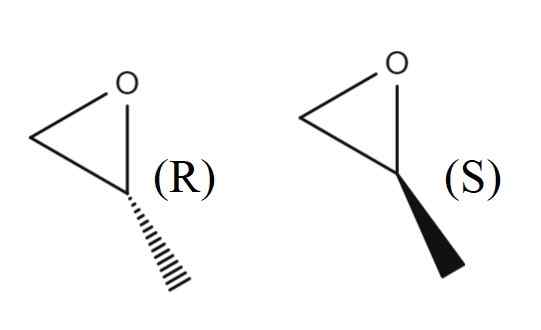 1,2-epoxipropan enantiomerer. Källa: Gabriel Bolívar.
1,2-epoxipropan enantiomerer. Källa: Gabriel Bolívar. I den övre bilden har du paret av enantiomerer på 1,2-epoxipropano. Enantiomer R avleder det polariserade ljuset till höger, medan S avleder det till vänster; Det vill säga, den första är (r)-(+)-1,2-epoxipropano, och den andra (er)-(-)-1.2-epoxipropano.
Den rankiska blandningen av dem två, igen, i ett 1 eller 50%-förhållande, blir (±) -1,2 -epoxipropan.
1-fenyletylamin
 Enantiomerer av 1-penyletylamin. Källa: Gabriel Bolívar.
Enantiomerer av 1-penyletylamin. Källa: Gabriel Bolívar. Över en annan rankicblandning bildad av de två enantiomererna av 1-feniletylamin visas. Enantiomeren R är (R)-(+)-1-fenyletylamin och enantiomer S (S)-(-)-1-feniletilamin; En har metylgruppen, Cho3, pekar utanför det aromatiska ringplanet och det andra pekar under detta.
Observera att när konfigurationen är R, sammanfaller den ibland med det faktum att Enantiómero roterar det polariserade ljuset till höger; Men det gäller inte alltid och kan inte tas som en allmän regel.
Slutkommentar
Viktigare än existensen eller inte av de rankiska blandningarna är den kirala upplösningen av samma. Detta gäller särskilt för föreningar med farmakologiska effekter som beror på sådan stereoisom; Det vill säga en enantiomer kan vara fördelaktig för patienten, medan den andra kan påverka den.
Det är därför dessa chirala upplösningar används för att separera rankiska blandningar i sina komponenter och därmed kunna marknadsföra dem som rena läkemedel fria från skadliga föroreningar.
Referenser
- Morrison, r. T. och Boyd, R, N. (1987). Organisk kemi. Femte upplagan. Redaktör Addison-Wesley Inter-American.
- Carey f. (2008). Organisk kemi. (Sjätte upplagan). MC Graw Hill.
- Graham solomons t.W., Craig b. Fryhle. (2011). Organisk kemi. Aminer. (10: e upplagan.). Wiley Plus.
- Steven a. Botekar. (2017). Illustrerad ordlista för organisk kemi: Racemisk blandning. Institutionen för kemi och biokemi, UCLA. Återhämtad från: kem.Ucla.Edu
- Nancy Devino. (2019). Racemisk blandning: Definition & exempel. Studie. Återhämtat sig från: studie.com
- James Ashenhurst. (2019). Stereokemi och kiralitet: Vad är en racemisk blandning? Återhämtat från: Masterorganicchemistry.com
- John C. Leffingwell. (2003). Kiralitet och bioaktivitet i.: Farmakologi. [Pdf]. Återhämtat sig från: Leffingwell.com

