Metoder för separering av homogena blandningar
- 2899
- 738
- Per Karlsson
De Metoder för separering av homogena blandningar De är alla de som, utan att använda kemiska reaktioner, tillåter att få komponenter eller lösta ämnen som integrerar samma fas; det vill säga av en flytande, fast eller gas.
Sådana homogena blandningar består av lösningar, där lösta partiklar är för små för att kunna skilja dem med blotta ögat. De är så små att det inte finns några smala eller selektiva filter för att behålla dem medan lösningen överför dem. Tekniker som centrifugering eller magnetisering hjälper inte heller.
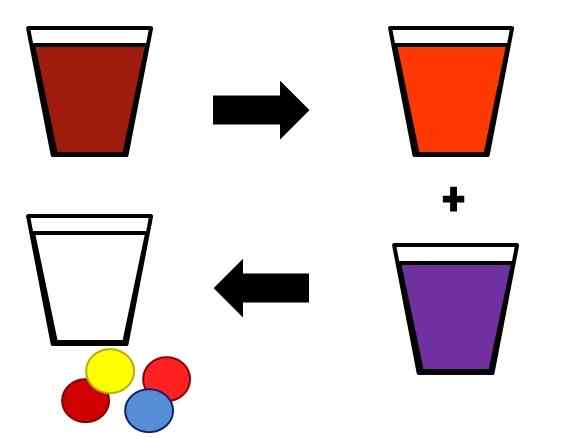 Illustrativt exempel på hur homogena blandningar kan separera i steg. Källa: Gabriel Bolívar.
Illustrativt exempel på hur homogena blandningar kan separera i steg. Källa: Gabriel Bolívar. Ett exempel på hur lösningar separeras i deras komponenter visas ovan. Den initiala blandningen (brun) är separerad i två komponenter, lika homogena (orange och lila). Slutligen, från de två resulterande blandningarna, erhålls lösningsmedlet (vita) och de fyra respektive paren av lösta ämnen (rödgul och rödblå).
Bland metoderna eller teknikerna för separering av lösningar har vi förångning, destillation, kromatografi och fraktionerad kristallisering. Beroende på blandningens komplexitet bör mer än en av dessa metoder användas tills den bryter homogenitet.
[TOC]
De viktigaste metoderna för separering av blandningar
- avdunstning
 Avdunstning är den enklaste metoden för att separera homogena blandningar från ett enda lösta ämnet.
Avdunstning är den enklaste metoden för att separera homogena blandningar från ett enda lösta ämnet. De enklaste homogena blandningarna är lösningarna där ett enda lösta ämnet har upplösts. I den överlägsna bilden finns till exempel en färgstark lösning på grund av absorption och reflektion av synligt ljus med partiklarna i dess lösta ämnen.
Om det har rört sig väl under förberedelserna kommer det inte att finnas några tydligare eller mörka regioner än andra; De är alla desamma, uniformer. Sådana färgglada partiklar kan inte separeras från lösningsmedlet med någon mekanisk metod, så du kommer att behöva energi i värme (röd triangel) för att uppnå det.
Det kan tjäna dig: koldisulfid (CS2): Struktur, egenskaper, användningar, riskerSåledes värms den färgglada lösningen i det fria för att påskynda och tillåta avdunstning av lösningsmedlet utanför dess behållare. När detta händer, minskar volymen som skiljer de lösta partiklarna och därför ökar och slutar dess interaktioner långsamt sedimenterande.
Det slutliga resultatet är att den färgglada lösta ämnet förblir längst ner i behållaren och lösningsmedlet har helt avdunstat.
Bekalven med förångning är att dess mål är att eliminera lösningsmedlet genom att eliminera lösningsmedlet genom att värma det till dess kokpunkt snarare än att eliminera lösningsmedlet genom att värma det till dess kokpunkt. Det återstående fasta ämnet kan bestå av mer än ett lösta ämnet och krävs därför från andra separationsmetoder för att definiera det i dess isolerade komponenter.
- Destillering
 Destillering
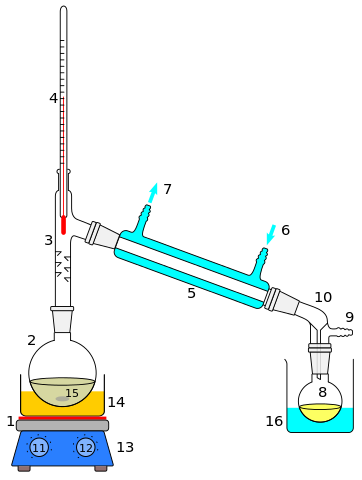
Destillering Destillation är kanske metoden för separering av homogena lösningar eller blandningar. Dess användning sträcker sig till smälta salter eller metaller, kondenserade gaser, lösningsmedel blandningar eller organiska extrakt. Lösningen är i mest av tiden en vätska, vars kokpunkt skiljer sig i flera grader med avseende på lösningsmedlet.
När skillnaden mellan sådana kokpunkter är hög (större än 70 ºC) används enkel destillation; Och om inte, utförs en fraktionerad destillation. Båda destillationerna har flera enheter eller mönster, liksom en annan metod för blandningar av olika kemisk natur (flyktig, reaktiv, polär, apolär, etc.).
Vid destillation bevaras både lösningsmedel och lösta ämnen, och detta är en av dess huvudskillnader när det gäller förångning.
Rotaevapningen kombinerar emellertid dessa två aspekter: en vätskefast eller vätskevätskblandning, såsom en upplöst och blandbar olja, de värms upp tills lösningsmedlet har tagits bort, men det samlas i en annan behållare medan det fasta eller det fasta eller det upplöst och blandbara olja olja kvar i den första behållaren.
Kan tjäna dig: periodisk tabell, vad är det förLuftdestillation
Kondensatluft utsätts för kryogen fraktionerad destillation för att separera syre, kväve, argon, neon, etc. Luften, en homogen gasformig blandning, förvandlas till en vätska där kväve, eftersom det är majoritetskomponenten, verkar i teorin som ett lösningsmedel; Och de andra gaserna, också kondenserade, som flytande lösta ämnen.
- Kromatografi
Kromatografi, till skillnad från andra tekniker, kan inte ge utbyten eller på distans lika; Det vill säga, det är inte användbart att bearbeta en hel blandning, utan en obetydlig fraktion av samma. Informationen som den tillhandahåller är emellertid analytiskt värdefull, eftersom den identifierar och klassificerar blandningar baserat på dess sammansättning.
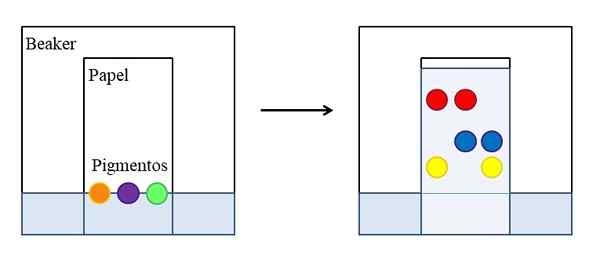 Papper eller fint skiktkromatografi. Källa: Gabriel Bolívar.
Papper eller fint skiktkromatografi. Källa: Gabriel Bolívar. Det finns olika typer av kromatografier, men det enklaste, som förklaras i skolor eller pre -universitetskurser, är den av uppsatsen, vars princip är densamma som den som utvecklats på ett fint lager av ett absorberande material (vanligtvis kiseldioxidgel ).
Den övre bilden visar att i en bägare, full av vatten eller ett specifikt lösningsmedel, placeras ett papper som har markerats en referenslinje med droppar eller punkter på tre utvalda pigment (orange, lila och grön). Bägaren förblir stängd så att trycket är konstant och mättad från lösningsmedelsångorna.
Sedan börjar vätskan stiga upp vid papperet och dra pigmenten. Pigment-pale-interaktioner är inte lika: vissa är starkare och andra svagare. Ju mer affinitet pigmentet känns för papperet, desto mindre kommer det att stiga genom papperet med avseende på den linje som ursprungligen var markerad.
Kan tjäna dig: hastighetskonstantTill exempel: det röda pigmentet är det som känns mindre affinitet för lösningsmedlet, medan den gula knappt steg upp eftersom papperet behåller det mer. Det sägs då att lösningsmedlet är den mobila fasen och papperet den stationära fasen.
- Fraktionerad kristallisation
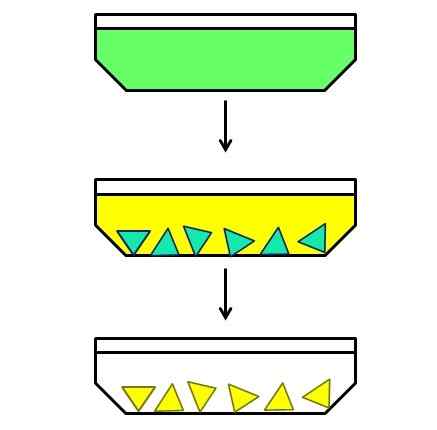 Illustrativt exempel på fraktionerad kristallisering. Källa: Gabriel Bolívar.
Illustrativt exempel på fraktionerad kristallisering. Källa: Gabriel Bolívar. Och slutligen har du fraktionerad kristallisering. Denna metod kan kanske katalogisera som en hybrid, eftersom den börjar från en homogen blandning för att avsluta en heterogen. Anta till exempel att det finns en lösning där ett grönt fast ämne har upplösts (överlägsen bild).
Gröna partiklar är för små för att separera manuellt eller mekaniskt. Det är också så att det gröna fasta ämnet är en blandning av två komponenter och inte en enda förening i denna färg.
Sedan värms en lösning av den och lämnas i vila under kylning. Det visar sig att de två komponenterna, även om de är mycket relaterade till varandra, är deras lösningsmedel lösningsmedel något olika; Därför kommer en av de två att börja kristallisera först och sedan den andra.
Den grönblå komponenten (mitt i bilden) är den första som kristalliseras, medan den gula komponenten fortfarande är upplöst. Att vara gröna blå kristaller är de heta innan gula kristaller dyker upp. Sedan, när lösningsmedlet svalnar lite mer, kristalliseras den gula och en annan filtrering.
Intresse teman
Blandningsseparationsmetoder.
Metoder för separering av heterogena blandningar.
Blandningar: komponenter och typer.
Homogena blandningar.
Heterogena blandningar.
Referenser
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Chelsea Schuyler. (2019). Kromatografi, destillion och filterion: Metoder för att separera blandningar. Studie. Återhämtat sig från: studie.com
- CK-12 Foundation. (16 oktober 2019). Metoder för att separera blandningar. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- Bra vetenskap. (2019). Blandningsseparation. Återhämtat sig från: Goodscience.com.Au
- Clark Jim. (2007). Tunt skiktkromatografi. Återhämtat sig från: Chemguide.co.Storbritannien
- « Utlovad (PM) struktur, egenskaper, erhållning, användning
- Metalinguistic Function Egenskaper, funktioner och exempel »

