Utlovad (PM) struktur, egenskaper, erhållning, användning

- 2163
- 434
- Lars Eriksson
han lovad Det är ett kemiskt element som tillhör klassen Lantanids. Det identifieras med PM -symbolen och dess atomnummer är 61. Det är ett radioaktivt metalliskt fast ämne och är det mest instabila elementet i de första 84 elementen i det periodiska bordet.
Detta element finns naturligtvis i mycket låga koncentrationer (cirka 4 x 10-femton gram per kg) i en typ av uraninit, som är ett uranmineral, där de utlovade är närvarande på grund av spontan klyvning av uran-238.
 Symbol, atomantal och atommassa av löftet. Källa: ME/CC BY-S (https: // CreativeCommons.Org/licenser/BY-SA/2.5). Källa: Wikimedia Commons.
Symbol, atomantal och atommassa av löftet. Källa: ME/CC BY-S (https: // CreativeCommons.Org/licenser/BY-SA/2.5). Källa: Wikimedia Commons. Trots sin brist i jordskorpan har den upptäckts i spektrumet av HR465 -stjärnan i Andromeda -konstellationen, på vars yta den uppskattas att den nyligen har bildats, sedan ingen PM -isotop har en längre halvliv på 17, 7 år.
Det var användbart i föremål som lyser i mörkret, men på grund av deras radioaktivitet stannade det att använda i dessa. Det används för att mäta materialtjocklekar och kärnkraftsbatterier.
[TOC]
Upptäckt
PROMETIOs existens misstänktes 1902 av kemisten tjeckiska Bohuslav Brauner. Senare, 1914, fann den engelska fysikern Henry Moseley i sina studier att ett element saknades mellan Neodymium och Samarium.
Därefter, även om flera grupper av forskare (italienare 1924, amerikaner 1926 och 1938) tillkännagav sin upptäckt, gjorde svårigheten att separera den från andra element och reproducera upplevelserna ingen kunna ta meriter.
 Jacob a. Marinsk. ORNL / PUB -domän. Källa: Wikimedia Commons.
Jacob a. Marinsk. ORNL / PUB -domän. Källa: Wikimedia Commons. Slutligen, 1944, forskarna Marinsky J.TILL., Glendenin l.OCH. och Coryell C.D. De testade sin närvaro och isolerade den från by -produkterna av uranklyvning i kärnreaktorn för Clinton Laboratories i Oak Ridge i Tennessee, USA.
 Larry E. Glendenin. ORNL / PUB -domän. Källa: Wikimedia Commons.
Larry E. Glendenin. ORNL / PUB -domän. Källa: Wikimedia Commons. De hävdade emellertid inte prioriteringen i upptäckten förrän 1946 för att de var helt hängivna till hemliga utredningar relaterade till försvarsaktiviteter under andra världskriget.
Namnuppdrag
Även om forskarna hade föreslagit att kalla honom "Clintonium" för att hedra laboratorierna där de arbetade, övertygade Coryells fru dem att kalla honom "lovade" som ett minne av den grekiska titanen Prometheus eller Prometheus.
 Charles D. Coryell. Författaren till fotot: Christian a. Coryell/GFDL (http: // www.gnu.Org/copyleft/fdl.html). Källa: Wikimedia Commons.
Charles D. Coryell. Författaren till fotot: Christian a. Coryell/GFDL (http: // www.gnu.Org/copyleft/fdl.html). Källa: Wikimedia Commons. Enligt vissa tolkningar av grekisk mytologi stal Prometheus gudarnas eld för att ge den till mänskligheten, så han straffades grymt för all evighet. Andra legender säger att det gav människor matematik, vetenskap, jordbruk och medicin och till och med skapade människan.
Det kan tjäna dig: Clausius-Clapeyron-ekvation: Vad är det för, exempel, övningar Prometheus representation av en tysk skulptör. © El Grafo / CC-by-SA-4.0 / pubdomän. Källa: Wikimedia Commons.
Prometheus representation av en tysk skulptör. © El Grafo / CC-by-SA-4.0 / pubdomän. Källa: Wikimedia Commons. Dessa tvivel om vad som var Prometheus bidrag till mänskligheten liknar osäkerhet om vem som upptäckte elementet. Å andra sidan, enligt Coryells fru, var namnet motiverat eftersom forskare hade "stulit gudarnas eld" när de upptäckte det under Atomic Bomb Secret -programmet.
Elektronisk struktur
Den elektroniska konfigurationen för detta element är:
1s2; 2s2 2p6; 3s2 3p6 3d10; 4s2 4p6 4d10; 5s2 5p6; 4F5 6s2;
som också kan uttryckas som:
[XE] 4F5 6s2.
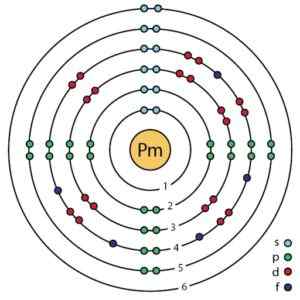 Prometio elektronisk struktur enligt Bohrs förbättrade atommodell. Ahazard.sciencewriter/cc by-sa (https: // creativecommons.Org/licenser/BY-SA/4.0). Källa: Wikimedia Commons.
Prometio elektronisk struktur enligt Bohrs förbättrade atommodell. Ahazard.sciencewriter/cc by-sa (https: // creativecommons.Org/licenser/BY-SA/4.0). Källa: Wikimedia Commons. Nomenklatur
- Lovad, PM -symbol.
- Prometio-147, PM-147 eller 147PM: Isotope del Prometio med atommassa 147.
Prometios egenskaper
Fysiskt tillstånd
Silled Metallic Solid, Hexagonal Crystals.
Atomisk massa
144.91
Smältpunkt
1042 ºC
Kokpunkt
3000 ºC
Densitet
7,26 g/cm3
Kemiska egenskaper
Det tillhör familjen till lantaniderna, lantanoiderna eller "sällsynta jordar", kallade det för att de i jordskorpan alltid är i form av sina oxider. Är en del av period 6 i den periodiska tabellen för elementen.
Enligt källor som konsulterats reagerar statsministern, liksom de andra lantaniderna, direkt med vattnet, långsamt kallt, snabbt vid uppvärmning, frisläppande väte (h2). Det mörknar snabbt i luften och bränner lätt att producera sin oxid.
Mer än 30 Prometio -föreningar har framställts och de flesta presenterar någon typ av färg. Dess oxidationsstatus i dessa föreningar är +3. Bildar inte tetravalenta katjoner.
Bildning av vissa föreningar
Lös upp det i saltsyra (HCl) de utlovade bildar PMCL3 vilket är gult och vattenlösligt. I salpetersyra (HNO3) Pm genereras (nej3)3 Det är rosa och också lösligt i vatten.
Om en lösning som innehåller PM -joner3+ är alkaliserad med NH3, Det vill säga pH ökas, hydroxiden fälls ut (PM (OH)3) ljusbrun.
Kan tjäna dig: jonisk länk: egenskaper, hur den bildas och exempelPM -sulfat2(SW4)3 Det är något lösligt i vatten. Om Prometios oxalat värms upp blir det PM -oxiden2ANTINGEN3 vit eller lavendel.
Radioaktiv utsläpp
Avger beta -strålning i form av elektroner som lämnar kärnan i deras atomer. När det utfärdar det blir det samariumelementet (SM). Å andra sidan kan det bli Neodymium (ND) genom att eliminera en kärna positron och fånga en elektron i samma. Premiärministeren avger inte gammastrålar.
Isotoper
Hittills är 14 isotoper av Prometio kända, med atommassor som sträcker sig från 134 till 155. Alla är instabila (radioaktiva), som skiljer det från andra Lantanides.
Prometio-147 är den med den största nytta och har en halveringstid på 2,6 år.
Isotop med större halvliv
Den längsta isotopen i halveringstiden är Prometio-145 med 17,7 år, som avtar med elektronisk fångst, som består av en atomelektron kombineras med en proton och bildar en neutron och en neutrino.
Det är emellertid den enda isotopen av PM som också kan drabbas av alfa -sönderdelning (utsläpp av 2 neutroner). Detta beror på att det har 84 neutroner och utfärdandet av 2 av dem gör att det är prometio-141 med 82 neutroner, vilket är en stabil konfiguration av kärnan. Men detta är en typ av förfall som inträffar väldigt lite.
Nuvarande erhållning
1963 framställdes cirka 10 gram Prometio med användning av jonbytarkromatografimetoder i atomreaktorbränsleavfall. Idag återhämtar det sig fortfarande på detta sätt som salter av 147P.m3+.
Enligt vissa källor bereddes det också under dessa år genom fluorreduktion (PMF3) Med litiumång (LI). Det är också framställt genom kloridreduktion (PMCL3) Med kalcium (CA) vid höga temperaturer.
Det kan också erhållas från Neodymium-146. Denna isotop utsätts för bombning med neutroner så att varje atom fångar en neutron och blir neodym-147. Det senare tar cirka 11 dagar som lider av beta-sönderdelning och omvandlas således i Prometio-147.
Ansökningar
Isotopen 147 (147Pm) är den som har använts mest, är den enda som kan hittas kommersiellt. Avger inte gammastrålar och levereras i form av oxid eller klorid. Deras transport och manipulation kräver dock skydd mot strålning.
Det kan tjäna dig: Hydrolys: Vad är det och exempel på reaktionerDen hade vissa användningsområden som idag inte längre har, eftersom det för närvarande används i speciella applikationer.
I batterier
Prometio-147 används i långsiktiga atombatterier. I detta fall placeras små bitar av PM i matrisen i en halvledare för att omvandla betautsläpp till el.
Denna typ av kärnkraftsbatterier kan tillhandahålla energi i cirka 5 år och har använts i alla typer av enheter, från missiler till pacemaker, som är enheter placerade hos patienter med hjärtproblem.
 Pacemakers kan ha lastbatterier baserade på Prometio. Författare: 242799. Källa: Pixabay.
Pacemakers kan ha lastbatterier baserade på Prometio. Författare: 242799. Källa: Pixabay. I medicinska tillämpningar
Enligt vissa källor används Prometios oxid i medicin som strålningskälla.
Inom industrin
Det har använts för att mäta tjockleken på vissa material, vilket görs genom att mäta beta -strålningen som passerar genom proverna.
Potentiella applikationer
Det kan användas som en transportabel X -Ray -källa, men tydligen har denna applikation ännu inte utvecklats kommersiellt.
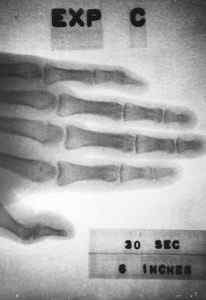 Röntgenbilden erhållen 1963 med en liten enhet (cirka 10 cm x 5 cm x 1 cm) som innehåller Prometio-147. Energi.Gov / pubdomän. Källa: Wikimedia Commons.
Röntgenbilden erhållen 1963 med en liten enhet (cirka 10 cm x 5 cm x 1 cm) som innehåller Prometio-147. Energi.Gov / pubdomän. Källa: Wikimedia Commons. Det skulle också tjäna till att tillhandahålla energi till rymd- och satellitprober eller att skapa enheter som tillåter kommunikation med ubåtar.
Avbruten användning i ljussignaler
Ursprungligen användes Prometio-147 för att ersätta radioelementet i lysande urtavlor, eftersom man lärde sig att radion var för farlig. För detta var PMCl blandat3 Med luminoforer, som lyser från grönaktig gul till blått när strålningen av de utlovade (beta -partiklarna) påverkar dem.
 För några tiotals år sedan kunde nålarna i armbandsklockorna ses i mörkret på grund av ljusstyrkan orsakad av radioaktiviteten i Prometio. Författare: Monacocannes. Källa: Pixabay.
För några tiotals år sedan kunde nålarna i armbandsklockorna ses i mörkret på grund av ljusstyrkan orsakad av radioaktiviteten i Prometio. Författare: Monacocannes. Källa: Pixabay. Den här egenskapen användes i armbandsklockor eller rattar för att lysa i mörkret. Även i tändningsknappen för några lysrörslampor. Dessutom skadade det inte luminoforerna som är fallet med andra källor till beta -strålning, vilket förlängde enhetens livslängd.
Men när det upptäcktes att lovande också är farlig, användningen på marknaden för föremål som lyser i mörkret.
Risker
PM är ett radioaktivt element, så det måste manipuleras med extrem försiktighet och med vederbörlig skydd. Förutom betapartiklarna som den släpper ut kan dessa påverka element med ett stort atomantal och generera röntgenstrålar.
 Prometio -prover måste transporteras inom en tjock blysköld för att undvika de skadliga effekterna av strålningen de avger. Energi.Gov / pubdomän. Källa: Wikimedia Commons.
Prometio -prover måste transporteras inom en tjock blysköld för att undvika de skadliga effekterna av strålningen de avger. Energi.Gov / pubdomän. Källa: Wikimedia Commons. Referenser
- ELLER.S. National Library of Medicine. (2019). Promethium - PM (Element). Återhämtat sig från pubchem.Ncbi.Nlm.Nih.Gov.
- Ganjali, m.R. et al. (2016). Introduktion till Lanthanide -serien (från Lanthanum till Lotetium). Prometium. I Lanthanides -serien Bestämning med olika analysmetoder. Återhämtat sig från Scientedirect.com.
- Chopppin, g. et al. (2013). Universums ursprung och nukleosyntes. Långsam neutronfångst. Inom radiokemi och kärnkemi (fjärde upplagan). Återhämtat sig från Scientedirect.com.
- Bly, D.R. (redaktör) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Press.
- Bomull, f. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Royal Society of Chemistry. (2020). Prometium. RSC återhämtade sig.org.

