Spektralserie
- 1690
- 364
- Per Karlsson
De Spektralserie De består av en uppsättning färgade linjer på mörk bakgrund, eller ljusa ränder separerade av mörka områden som avger ljus från alla slags ämnen.
Dessa linjer visualiseras med hjälp av en spektrometer, en apparat som består av ett prisma eller ett fint uppdelat rack, som kan separera de olika komponenterna i ljuset.
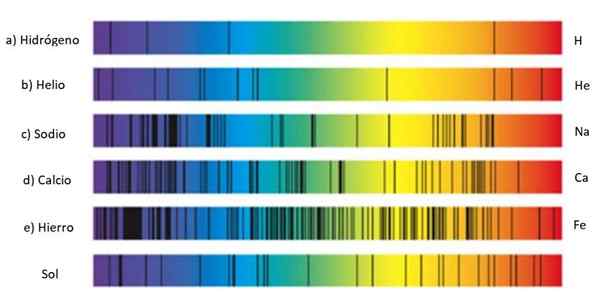
 Absorptionsspektra för olika ämnen och solen. Källa: Wikmedia Commons.
Absorptionsspektra för olika ämnen och solen. Källa: Wikmedia Commons. Dessa uppsättningar linjer kallas spektrum Och varje ämne har ett karacateristspektrum, ett slags fingeravtryck som tjänar till att identifiera dess närvaro i ljuset som kommer från ett objekt. Detta beror på att varje atom har sin egen elektronkonfiguration och tillåtet energinivåer.
Det är därför att hitta de spektrala linjerna är en teknik som används allmänt av astronomer för att ta reda på stjärnornas sammansättning genom ljuset de släpper ut. Faktum är att allt som astronomer vet om stjärnorna kommer från deras spektra, vare sig utsläpp eller absorption.
Spektraens ursprung
Närvaron av spektra beror på atomkonfiguration. Faktum är att elektroner förblir runt kärnan i regioner som kallas Orbitaler, beläget på vissa diskreta avstånd från honom.
Till exempel i väte, det enklaste elementet, orbitalradioerna ges av 0.053 ∙ n2 Nanometrar, där n = 1, 2, 3, 4, .. . Mellanvärden är inte tillåtna mellan dem, så det sägs att orbitalerna är kvantiserad. Även energitillståndet för varje bana kvantiseras.
Sådana begränsningar gör att elektroner uppför sig samtidigt som partiklar och även som vågor, precis som ljus. Emellertid kan elektroner gå från en omlopp till en annan och ändra atomens energitillstånd.
Elektromagnetisk energiabsorption och utsläpp
Till exempel, om en elektron går från en mer intern omlopp, med mindre energi, till en annan mer extern och energisk, är det nödvändigt att förvärva den nödvändiga elektromagnetiska energin, som lagras i atomen. Denna process kallas absorption.
Å andra sidan, om elektronen går från ytterligare en extern omlopp till en mer intern, i övergången släpps en foton, i lätt form, som är den energi som motsvarar energiskillnaden mellan orbitalerna. Våglängden motsvarar denna skillnad och ges av:
Kan tjäna dig: Orion Nebula: Ursprung, plats, egenskaper och data
- E är energi
- λ är våglängden
- H är Plancks konstant
- C är ljusets hastighet
Typer av spektra
Det finns både absorptions- och emissionsspektra, som beror på vissa parametrar för objektet eller ämnet, såsom densitet och temperatur. Spektrumet av en svag gas skiljer sig från det för en fast vid hög temperatur.
Kontinuerligt spektrum
Vissa källor avger spektra vars färgade linjer förändras försiktigt och innehåller alla färger. Detta kallas ett kontinuerligt spektrum, till exempel den som producerar glödtråden för en glödlampa.
Utsläppsspektrum
Det är den som avger vissa heta ämnen och består av några få linjer med en viss våglängd.
Denna typ av spektrum produceras av svaga och heta gaser som de som fyller lysrören. Boreal Aurora är ett annat exempel på utsläpp som inträffar i gasens övre atmosfär. De producerar också utsläppsspektra några interstellära gasmoln.
Absorptionsspektrum
Detta spektrum är det som tas emot när ljuset av ett tätt och mycket hett objekt passeras genom en kallare gas. I den observeras nästan alla färger, men vissa verkar minskade och vissa mörka ränder uppstår i de våglängder som absorberas av atomer eller gasmolekyler.
Kirchoff -lagar om spektroskopi
Kirchoffs spektroskopilagar indikerar under vilka förhållanden de olika spektra som beskrivs ovan bildas:
- Kontinuerliga spektra: De släpps ut av alla objekt vid högt tryck och temperatur.
- Emissionsspektra: De produceras genom ett lågt tryck vid lågt tryck, vilket avger väldefinierade våglängder, motsvarande de elektroniska övergångarna som motsvarar varje element som utgör gasen.
- Absorptionsspektra: produceras av gaser vid låga temperaturer belägna nära teckensnitt av kontinuerlig strålning. Gasatomer eller molekyler absorberar endast vissa våglängder.
Väteutsläppsspektrumet
Väteutsläppsspektrumet är särskilt viktigt, eftersom det är det vanligaste elementet i hela universum och innehåller mycket viktig information om stjärnorna och Vintergatan.
Vätespektrumlinjer upptäcktes av olika forskare och var och en heter.
Balmerserie
Väte avger olika linjer i det synliga spektrumet: När elektronen minskar från orbital 3 till orbital 2 avger rött ljus, vars våglängd är 656.6 nm, och om det sönderfaller från orbital 4 till 2 avger sedan 486 blått ljus.1 nm.
 Väteutsläppsspektrum, som visar linjerna som motsvarar synligt ljus och två ultravioletta linjer till vänster. Källa: Wikmedia Commons.
Väteutsläppsspektrum, som visar linjerna som motsvarar synligt ljus och två ultravioletta linjer till vänster. Källa: Wikmedia Commons. 1885 (innan Bohr föreslog sin teori), konstaterade matematikern och schweizisk professor Johann Balmer (1825-1898) av Tanteo en formel för att bestämma våglängderna λ för dessa linjer:
Var:
- R är Rydbergs konstant: 1.097 × 107 m-1
- N = 3, 4, 5 .. ., det vill säga n ≥ 3 (hela).
Till exempel för n = 3 i Balmer -ekvationen:
Motsvarande den röda linjen till höger, som visas i figuren ovan. Upptäckten av Balmer -serien fick andra forskare att leta efter linjer i resten av vätespektrumet och andra gaser.
Lyman -serie
Observera att vätespektrumet som visas i figuren innehåller några linjer i Ultraviolet, de två av den extrema vänster, vars våglängder är 397.0 nm och 388.9. nm.
Dessa linjer i Ultraviolet motsvarar faktiskt den så kallade Lyman -serien, som upptäcktes 1906 av fysikern Theodore Lyman. Dess formel är:
Kan tjäna dig: BTU (termisk enhet): Ekvivalenser, användningar, exempel)
Paschen -serie
Paschen -serien upptäcktes av den tyska fysikern Friederich Paschen 1908 och är giltig för n ≥ 4, det vill säga: n = 4, 5, 6 ..
Paschen -linjer finns i det nära infraröda området och den slutliga nivån är n = 3, det vill säga deras värden uppstår när elektronen minskar från högre nivåer till n = 3. Eftersom Lyman -serien är i Ultraviolet, dras slutsatsen att Balmer -serien är mellan Lyman och Paschen.
Brackett -serie
Denna serie som upptäcktes 1922 av Frederick Brackett, en amerikansk fysiker, ligger i den avlägsna infraröd och består av de spektrala linjerna som motsvarar väteövergångarna som börjar vid n = 5 och fortsätter:
Pfund -serie
PFUND -serien hittades 1924 av den amerikanska fysikern August Hermann Pfund och hänvisar till övergångarna som börjar vid n = 5, i det avlägsna infraröda bandet:
) Referenser
Referenser
- Arny, t. 2017. Utforskningar: En introduktion till astronomi. 8th. Ed. McGraw Hill.
- Bauer, w. 2011. Fysik för teknik och vetenskap. Volym 2. MC Graw Hill.
- Chang, R. 2013. Kemi. 11VA. Utgåva. MC Graw Hill Education.
- Sears, Zemansky. 2016. Universitetsfysik med modern fysik. 14th. Ed. Volym 2. Pearson.
- Windows öppna för universum. De olika typerna av spektra. Återhämtat sig från: Media4.Osppm.fr.


)
m^-1=656.3&space;\:&space;nm)
)
)