Serinegenskaper, funktioner, metabolism, mat
- 2214
- 495
- Prof. Erik Johansson
De Serin Det är en av de 22 grundläggande aminosyrorna, även om detta inte klassificeras som en essentiell aminosyra för människa och andra djur, eftersom det syntetiseras av människokroppen.
Enligt de tre nomenklaturen beskrivs serinen i litteraturen som att vara i enstaka bokstäver). Denna aminosyran deltar i ett stort antal metaboliska vägar och har polära egenskaper, men har inte en belastning på neutralt pH.
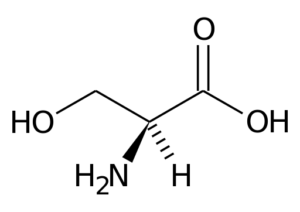 Representation av serien av serinaminosyran (källa: Sidzero vid den.Wikipedia [Public Domain] via Wikimedia Commons)
Representation av serien av serinaminosyran (källa: Sidzero vid den.Wikipedia [Public Domain] via Wikimedia Commons) Många viktiga enzymer för celler har gott om.
Serinen, bland många av dess funktioner, deltar som en föregångare och ställningsmolekyl i biosyntesen av andra aminosyror såsom glycin och cystein och är en del av strukturen hos slamipiderna som finns i cellmembran i cellmembran.
Serinsyntesfrekvensen varierar i varje organ och dessutom förändras den enligt utvecklingsstadiet där individen är.
Forskare har föreslagit att L-serinkoncentrationer i hjärnvävnad ökar med åldern, eftersom permeabiliteten för blodcellbarriären minskar i hjärnan hos den vuxna och kan orsaka allvarliga hjärnstörningar.
Det är känt att L-serin är avgörande för biosyntes av neurotransmittorer, fosfolipider och andra komplexa makromolekyler, eftersom det ger föregångarna för dessa multipla metaboliska vägar.
Olika studier har visat att utbud av tillskott eller koncentrat av L-serin till vissa typer av patienter förbättrar glukoshomeostas, mitokondriell funktion och minskar neuronal död.
[TOC]
Egenskaper och struktur
Alla aminosyror har som en basstruktur en karboxylgrupp och en aminogrupp fäst vid samma kolatom; Dessa skiljer sig emellertid från varandra av sina sidokedjor, kända som R -grupper, som kan variera i deras storlek, struktur och till och med i deras elektriska laddning
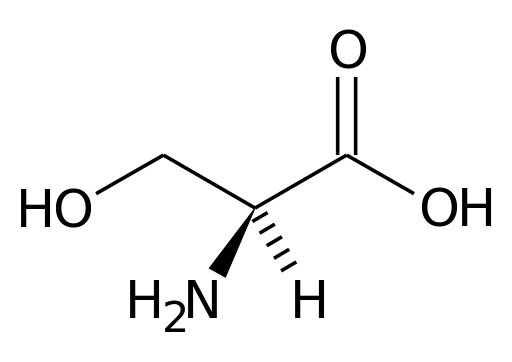
Serinen innehåller tre kolatomer: ett förenat centralt kol, å ena sidan, till en karboxylgrupp (COOH) och å andra sidan en aminogrupp (NH3+). De andra två centrala kolbindningarna är ockuperade av en väteatom och en CH2OH (grupp R), karakteristisk för serinen.
Det centrala kolet till vilket amino- och karboxylgrupperna i aminosyrorna kallas a -kolet. De andra kolatomerna i R -grupper betecknas med bokstäverna i det grekiska alfabetet.
När det gäller serinen, till exempel, är den enda kolatomen i sin R -grupp, som är kopplad till OH -gruppen, känd som Carbon y.
Kan tjäna dig: fosfatidilserine: struktur, syntes, funktioner, platsKlassificering
Serinen klassificeras inom gruppen av polära aminosyror utan belastning. Medlemmarna i denna grupp är mycket lösliga aminosyror i vatten, det vill säga de är hydrofila föreningar. I serinen och treonin beror hydrofilicitet på dess förmåga att bilda vätebroar med vatten genom dess hydroxylgrupper (OH).
Inom gruppen av polära aminosyror utan belastning grupperas också cystein, asparagin och glutamin. Alla dessa har en polär grupp i sin R -kedja, men denna grupp är inte joniserbar och pH nära neutralitet avbryter deras laddningar som producerar en förening i form av "Zwitterion".
Stereokemi
Den allmänna asymmetrin för aminosyror gör stereokemin för dessa föreningar av avgörande betydelse i de metaboliska rutter där de deltar. När det gäller serin kan detta hittas som d-o l-serin, som är den senare syntetiserade uteslutande av cellerna i nervsystemet som kallas astrocyter.
Aminosyrans kolhydrater är chirala kol, eftersom de har fyra olika United -substituenter, vilket genererar att det finns minst två urskiljbara stereoisomerer för varje aminosyra.
En stereoisomer är en spegelbild av en molekyl, det vill säga du kan inte överlappa varandra på den andra. Lösningarna av dessa aminosyror roterar det polariserade ljusplanet i motsatta riktningar i motsatta riktningar betecknas med bokstaven D o som experimentellt.
L-serinen som är syntetiserad i nervsystemceller fungerar som ett substrat för att syntetisera glycin eller D-serin. D-serin är ett av de viktigaste elementen för utbyte av vesiklar mellan neuroner, så vissa författare föreslår att båda serinisoformerna i verkligheten är essentiella aminosyror för neuroner för neuroner.
Funktioner
OH -gruppen av serinen i sin R -kedja R gör det till en bra nukleofil, så den är nyckeln till aktiviteten hos många enzymer med serin på sina aktiva platser. Serin är ett av de nödvändiga substraten för NADPH och glutationisk nukleotidsyntes.
L-serien är nödvändig för utvecklingen och korrekt funktion av centrala nervsystemet. Studier har visat att den exogena tillförseln av L-serin i låga doser till hippocampusneuroner och Purkinje-celler In vitro, Förbättrar din överlevnad.
Flera studier av cancerceller och lymfocyter har funnit att serinberoende kolenheter är nödvändiga för överdriven nukleotidproduktion, liksom efterföljande spridning av cancerceller.
Kan tjäna dig: mikrobiota: komposition, funktioner och var är detSelenocystein är en del av de 22 grundläggande aminosyrorna och erhålls endast som ett derivat av serinen. Denna aminosyran har endast observerats i vissa proteiner, innehåller selen istället för svavel fäst vid cysteinet och syntetiseras baserat på en sterifierad serin.
Biosyntes
Serinen är en icke -essentiell aminosyra, eftersom den syntetiseras av människokroppen. Detta kan emellertid assimileras från dieten för olika källor såsom proteiner och fosfolipider, främst.
Serinen syntetiseras i sin form genom omvandling av en glycinmolekyl, en reaktion medierad av ett hydroximetyltransferasenzym.
Det är känt att huvudplatsen för syntes av L-serin är i astrocyter och inte i neuroner. Det är dessa celler, syntes sker genom en fosforyleringsväg där 3-fosfoglyceratet deltar, en glykolytisk mellanhand.
Tre enzymer verkar på denna väg: 3-fosfoglyceratdehydrogenas, fosfoserin-transferas och fosfoserin-fosfatas.
Andra viktiga organ när det gäller serinsyntes är levern, njurarna, testiklarna och mjälten. Enzymerna som syntetiserar serin.
En av de första syntesvägarna för serin som var känd var den kataboliska vägen involverad i glukoneogenes, där L-serin erhålls som en sekundär metabolit. Emellertid är bidraget från denna rutt till produktion av kroppsserin låg.
Ämnesomsättning
Det är för närvarande känt att serinen kan erhållas från kolhydratmetabolismen i levern, där D-glyceric, 3-fosfoglycerinsyra och 3-fosfohydroxipirúvinsyra produceras. Tack vare en transamineringsprocess mellan 3-hydroxi pyruvinsyra och alanin produceras serin serin.
Experiment med råttor radioaktivt markering av kol 4 av glukos, har kommit fram till att detta kol effektivt införlivas i serinens kolskelett, vilket tyder på att nämnda aminosyra har en föregångare på tre kol troligtvis från pyruvat.
I bakterier är L-serin-desaminasenzymet det huvudsakliga enzymet som ansvarar för att metabolisera serinen: det omvandlar L-serin till en pyruvat. Det är känt att detta enzym är närvarande och aktivt i grödor av OCH. coli Beviljar i minimala medier med glukos.
Det är inte säkert känt vad som är den verkliga funktionen av L-serin-desaminas i dessa mikroorganismer, eftersom dess uttryck induceras av mutationseffektorer som skadar DNA genom ultraviolett strålning, på grund av närvaron av nalidíico, mytomicin och andra, mytomicin och andra, så det följer att det måste ha viktiga fysiologiska konsekvenser.
Kan tjäna dig: Dryopithecus: upptäckt, egenskaper, skalle, matSerinrika livsmedel
Alla livsmedel med höga proteinkoncentrationer är rika på serin, främst ägg, kött och fisk. Detta är emellertid en icke -essentiell aminosyra, så det är inte strikt nödvändigt att äta det med tanke på att kroppen kan syntetisera den själv.
Vissa människor lider av en ovanlig störning, eftersom de har en bristfenotyp med avseende på syntesmekanismerna för serin och glycin, därför måste de äta koncentrerade kosttillskott för båda aminosyrorna.
Dessutom erbjuder kommersiella varumärken som är specialiserade på försäljning av vitamintillskott (Lamberts, nu Sport och Holomega) fosfatidylserin och L-serinkoncentrat för att öka produktionen av muskelmassa i höga konkurrensidrottare och viktlyftare.
Relaterade sjukdomar
Felet av de enzymer som är involverade i biosyntesen av serin kan orsaka allvarliga patologier. Genom att minska serinkoncentrationen i blodplasma och cerebrospinalvätska kan det orsaka hypertoni, psykomotorisk fördröjning, mikrocefali, epilepsi och komplexa störningar i centrala nervsystemet.
Det har för närvarande upptäckts att serinbrist är involverat i utvecklingen av diabetes mellitus, eftersom L-serin är nödvändig för syntes av insulin och dess receptorer.
Spädbarn som presenterar defekter i serinbiosyntes är neurologiskt onormala vid födseln, har förseningar i intrauterin tillväxt, medfödd mikrocefali, grå starr, anfall och en allvarlig försening i neurologisk utveckling.
Referenser
- Elsila, J. OCH., Dworkin, J. P., Bernstein, m. P., Martin, m. P., & Sandford, s. TILL. (2007). Mekanismer för bildning av aminosyror i interstellära isanaloger. The Astrophysical Journal, 660 (1), 911.
- Ichord, r. N., & Bearden, D. R. (2017). Perinatal metabolisk encefalopati. I Swaimans pediatriska neurologi (pp. 171-177). Annars.
- MOTHET, J. P., Förälder, a. T., Wolosker, h., Brady, r. ANTINGEN., Linden, D. J., Ferris, c. D.,... & Snyder, s. H. (2000). D-serin är en endogen ligand för glycinstället för N-metyl-D-apartatmottagaren. Proceedings of the National Academy of Sciences, 97 (9), 4926-4931
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger principer för biokemi. Macmillan.
- Rodríguez, a. OCH., Anka, g. S., Billingham, L. K., Martinez, C. TILL., Mainolfi, n., Suri, v.,... & Chandel, n. S. (2019). Serinmetabolism stöder makrofag IL-1p-produktion. Cellmetabolism, 29 (4), 1003-1011.
- Tabatabaie, l., Klomp, l. W., Berger, r., & Koning, T. J. (2010). L-serinsyntes i centrala nervsystemet: En översyn av serinbriststörningar. Molekylär genetik och metabolism, 99 (3), 256-262.
- « Glyceraldehydstruktur, egenskaper, funktioner
- Zinkhistoria, egenskaper, struktur, risker, användningar »

