Isotoniska lösningskomponenter, beredning, exempel
- 4301
- 1024
- Anders Svensson
En isotonisk lösning Det är en som uppvisar samma koncentration av lösta. Denna barriär tillåter lösningsmedlet att transte, men inte alla lösta partiklar.
I fysiologi hänvisar denna isolerade lösning till intracellulär vätska, det vill säga cellernas inre; Medan den semipermeabla barriären motsvarar cellmembranet, bildat av en lipid Bilay.
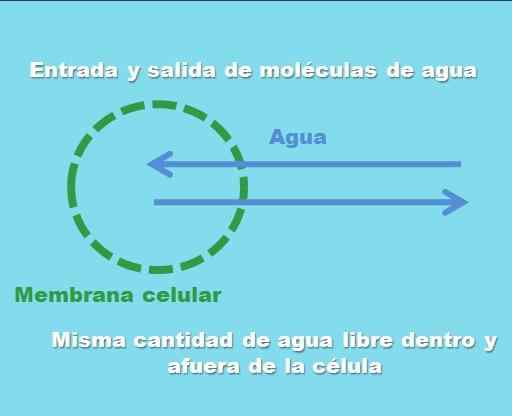
 Interaktion mellan en cell med en isoton lösning. Källa: Gabriel Bolívar.
Interaktion mellan en cell med en isoton lösning. Källa: Gabriel Bolívar. Den överlägsna bilden illustrerar vad som menas med en isotonisk lösning. "Koncentrationen" av vatten är densamma inom och utanför cellen, så deras molekyler kommer in eller kommer ut genom cellmembranet med lika frekvenser. Därför, om två vattenmolekyler kommer in i cellen, kommer två av dem att lämna samtidigt mot det extracellulära mediet.
Detta tillstånd, kallad isotonicitet, äger rum endast när det vattenhaltiga mediet, inom och utanför cellen, innehåller samma antal upplösta lösta partiklar. Således kommer en lösning att vara isoton om koncentrationen av dess lösta ämnen liknar den för vätskan eller det intracellulära mediet. Till exempel är 0,9% saltlösning isotonisk.
[TOC]
Komponenter i isotoniska lösningar
För att det ska finnas en isotonisk lösning måste den först se till att osmosen inträffar i lösningen eller lösningsmedlet. Detta är endast möjligt om en semipermeabel barriär finns, vilket gör det möjligt för lösningsmedelsmolekyler att överföra den, men inte de med lösta ämnen, särskilt elektriskt laddade lösta ämnen, joner.
Således kan inte lösta ämnet spridas från mer koncentrerade regioner till mer utspädda regioner. Istället kommer det att vara vattenmolekylerna som kommer att flytta från en plats till en annan, korsa den semipermeabla barriären och äga rum osmosen. I vattenhaltiga och biologiska system är denna barriär par excellence cellmembranet.
Kan tjäna dig: konkurrens (biologi): egenskaper, typer, exempelAtt ha en semipermeabel barriär och ett lösningsmedelmedium är närvaron av upplösta joner eller salter i båda medierna också nödvändig: den inre (inuti barriären) och den yttre (utanför barriären).
Om koncentrationen av dessa joner är densamma på båda sidor, kommer det inte att finnas något överskott eller underskott av vattenmolekyler för att lösa dem. Det vill säga antalet vattenfria molekyler är detsamma, och därför kommer de inte att överföra den semipermeabla barriären någonstans med syftet att matcha jonernas koncentrationer.
Förberedelse
- Förhållanden och ekvation
Även om en isotonisk lösning kan framställas med något lösningsmedel, eftersom vatten är mediet för cellerna, anses detta vara favoritalternativet. Att veta exakt koncentrationen av salter i en specifik kropp av kroppen, eller i blodomloppet, är det möjligt att uppskatta hur mycket salter den måste upplösas i en given volym.
I ryggradsorganismer accepteras det att koncentrationen av lösta ämnen i blodplasma är cirka 300 mOSM/L (miliosmolaritet) och kan tolka nästan som 300 mmol/L. Det vill säga det är en mycket utspädd koncentration. För att uppskatta miliosmolariteten måste följande ekvation tillämpas:
Osmolaritet = m · v · g
För praktiska ändamål antas det g, Den osmotiska koefficienten har ett värde på 1. Så att ekvationen nu är som:
Osmolaritet = m · v
Var m Det är molariteten i det lösta ämnet, och v Antalet partiklar som nämnda lösta dissocierar i vattnet. Sedan multiplicerar vi detta värde med 1.000 för att få miliosmolariteten för ett visst lösta ämnet.
Kan tjäna dig: vad är homoplasi? (Med exempel)Om det finns mer än ett lösta ämnet kommer lösningens totala miliosolitet att vara summan av tusensmolariteterna för varje lösta ämnen. Ju mer lösta ämnen med avseende på cellernas inre, desto mindre isoton är den beredda lösningen.
- Exempel på förberedelser
Anta att du vill förbereda en liter av en isoton lösning baserad på glukos och natriumdiácid fosfat. Hur mycket som ska väga glukos? Antag att 15 gram nah kommer att användas2Po4.
Första steget
Vi måste först bestämma nah osmolariteten2Po4 beräkna dess molaritet. För att göra detta vänder vi oss till dess molmassa eller molekylvikt, 120 g/mol. Eftersom vi uppmanas om en liter lösning bestämmer vi molen och vi kommer direkt att ha molaritet:
Moles (nah2Po4) = 15 g ÷ 120 g/mol
= 0,125 mol
M (nah2Po4) = 0,125 mol/l
Men när nahen2Po4 Det löses upp i vatten, frigör en na katjon+ och en anjon h2Po4-, därav v Den har ett värde på 2 i osmolaritetsekvationen. Vi fortsätter att beräkna då för nah2Po4:
Osmolaritet = m · v
= 0,125 mol/l · 2
= 0,25 osm/l
Och genom att multiplicera det med 1.000 Vi har miliosmolariteten i nah2Po4:
0,25 osm/l · 1.000 = 250 mOSM/L
Andra steg
Eftersom lösningens totala milioolaritet måste vara lika med 300 mOSM/L, subtraherar vi oss för att veta vad glukosen ska vara:
MOSM/L (glukos) = MOSM/L (total) - MOSM/L (NAH2Po4)
= 300 mOSM/L - 250 mOsm/L
= 50 mOsm/L
Eftersom glukos inte dissocierar, v Vale 1 och dess osmolaritet är lika med dess molaritet:
M (glukos) = 50 mOsm/l ÷ 1.000
= 0,05 mol/L
Som molar av glukos 180 g/mol bestämmer vi äntligen hur många gram vi måste väga för att lösa upp den i den liter av isotonisk lösning:
Kan tjäna dig: Renina: Struktur, produktion, utsöndring, funktionerMassa (glukos) = 0,05 mol · 180 g/mol
= 9 g
Därför denna nah isotonisk lösning2Po4/Glukos förbereder 15 gram nah2Po4 och 9 gram glukos i en liter vatten.
Exempel på isotoniska lösningar
Isotoniska lösningar eller vätskor orsakar inte någon gradient eller förändring i koncentrationen av joner i kroppen, så deras verkan fokuserar i huvudsak på att fuktiga patienter som får den vid blödning eller uttorkning.
Normal saltlösning
En av dessa lösningar är normal saltlösning, med en 0,9% NaCl -koncentration.
Ringer -laktatlösning
Andra isotoniska lösningar som används för samma ändamål är Ringer -laktat, vilket minskar surhet på grund av dess buffert eller dämpningskomposition, och Sorensens fosfatlösningar, som består av fosfater och natriumklorid.
Icke -varhaltiga system
Isotonicitet kan också tillämpas på icke -vattenhaltiga system, såsom de där lösningsmedlet är en alkohol; Så länge det finns en semipermeabel barriär som gynnar transparensen hos alkoholmolekyler och behåller de lösta partiklarna.
Referenser
- Från Lehr Spilva, till. Och Muktans, och. (1999). Guide till läkemedelsspecialiteter i Venezuela. Xxxvª edition. Globala utgåvor.
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Elsevier b.V. (2020). Isotonisk lösning. Hämtad från: Scientedirect.com
- Adrienne Brundage. (2020). Isotonisk lösning: Definition & exempel. Studie. Återhämtat sig från: studie.com
- Felicitas Merino de la Hoz. (s.F.). Intravenös seroterapi. University of Cantabria. [Pdf]. Återhämtat sig från: ocw.Oanisk.är
- Farmaceutiska och sammansatta laboratoriet. (2020). Oftalmiska beredningar: isotoniska buffertar. Återhämtat sig från: Pharmlabs.Unc.Edu

