Kopparsulfidstruktur, egenskaper, användningar

- 4741
- 994
- Per Eriksson
han kopparsulfid Det är en familj av oorganiska föreningar vars allmänna kemiska formel är cuxSoch. Ja x Det är större än och Det betyder att denna sulfid är rikare i koppar än i svavel; Och om tvärtom, x Det är mindre än och, Då är sulfid rikare i svavel än i koppar.
I naturen dominerar många mineraler som representerar naturliga källor till denna sammansättning. Nästan alla av dem är rikare på koppar än i svavel, och deras sammansättning uttrycks och förenklas av formeln medxS; här x Du kan till och med ta fraktionella värden, vilket indikerar ett stökiometriskt fast ämne (CU1.75S, till exempel).
 Ett prov av Covellita Mineral, en av de många naturliga källorna till kopparsulfid. Källa: James ST. John [CC av 2.0 (https: // CreativeCommons.Org/licenser/av/2.0)]
Ett prov av Covellita Mineral, en av de många naturliga källorna till kopparsulfid. Källa: James ST. John [CC av 2.0 (https: // CreativeCommons.Org/licenser/av/2.0)] Även om svavelet i elementet är gult ser dess derivatföreningar mörka färger; Sådan förekommer också med kopparsulfid. Covelita Mineral (överlägsen bild), som huvudsakligen består av CUS, ställer ut metallglitter och en blåaktig irisescens.
De kan framställas från olika koppar- och svavelkällor, med olika tekniker och variera syntesparametrarna. Således kan du få CUS -nanopartiklar med intressanta morfologier.
[TOC]
Kopparsulfidstruktur
Länkar
Denna förening har utseendet att vara kristallin, så du kan omedelbart tro att den består av cujoner+ (Monovalent koppar), CU2+ (Divalent Copper), s2- E, jämnt, s2- och s22- (Disulfur -anjoner), som interagerar genom elektrostatiska krafter eller jonbindning.
Det finns emellertid en liten kovalent karaktär mellan Cu och S, och därför kan CU-S-länken inte uteslutas. Från detta resonemang börjar den kristallina strukturen hos CU: er (och den för alla dess härledda fasta ämnen) att skilja sig från de som finns eller karakteriseras för andra joniska eller kovalenta föreningar.
Med andra ord kan det inte talas om rena joner, men att mitt i dess attraktioner (katjon-anion) finns det en liten överlappning av dess yttre orbitaler (elektrondelning).
Koordinationer i covelita
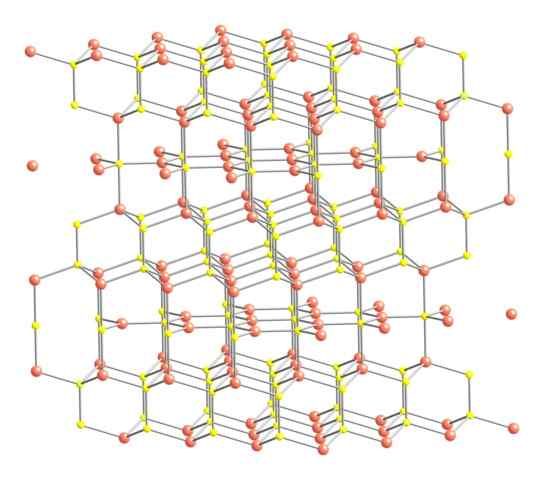 Kristallinstrukturen i Covellita. Källa: Benjah-Bmm27 [Public Domain].
Kristallinstrukturen i Covellita. Källa: Benjah-Bmm27 [Public Domain]. Efter att ha sagt ovanstående visas den kristallina strukturen hos covelite i bilden. Den består av hexagonala kristaller (definierade av parametrarna för deras enhetsceller), där jonerna binder och styr i olika koordinationer; Dessa är, med ett varierat antal närliggande grannar.
Kan tjäna dig: typ av länk på 02På bilden representeras kopparjoner med rosa sfärer, medan svavel med gula sfärer.
Fokuserar uppmärksamhet först på rosa sfärer, kommer det att noteras att vissa är omgiven av tre gula sfärer (trigonal platt koordination) och andra för fyra (tetraedral koordination).
Den första typen av koppar, trigonal, kan identifieras i planen vinkelrätt mot de hexagonala ansikten de ger mot läsaren, där de i sin tur är den andra typen av kol, tetraedrala.
När de nu deltar i de gula sfärerna har vissa fem rosa sfärer (trigonal bipyramidkoordination) och ytterligare tre och en gul sfär (igen, tetraedral koordination); I det senare är det före disulfidanjonen, som kan visualiseras ner och inom samma struktur av covelite:
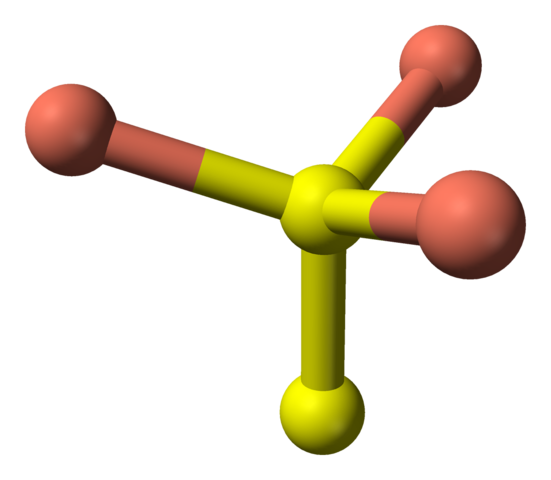 Tetraedral samordning av disulfidanjonen i Covellita. Källa: Benjah-Bmm27 [Public Domain].
Tetraedral samordning av disulfidanjonen i Covellita. Källa: Benjah-Bmm27 [Public Domain]. Alternativ formel
Det finns då cu -joner2+, Cu+, S2- och s22-. Studier genomförda med XPS (XPS) fotoelektronikspektroskopi påpekar emellertid att alla koppar är som katjoner CU+; Och därför uttrycks den initiala CUS -formeln "bättre" som (cu+)3(S2−) (S2)-.
Lägg märke till att förhållandet CU: s för den tidigare formeln fortsätter att vara 1, och även belastningarna avbryts.
Andra kristaller
En kopparsulfid kan anta ortorrombiska kristaller, som i polymorf, y-CU2S, av calcocita; kubik, som i en annan polymorf av calcocite, a-cu2S; Tetragonal, i Anilita Mineral, Cu1.75S; monoklinisk, i Djurleita, cu1.96S bland andra.
För varje definierat glas finns ett mineral, och i sin tur har varje mineral sina egna egenskaper och egenskaper.
Egenskaper
Allmän
Egenskaperna för kopparsulfid är föremål för förhållandet CU: S av deras fasta ämnen. Till exempel de som presenterar anjoner s22- De har hexagonala strukturer och kan vara antingen halvledare eller metalliska ledare.
Kan tjäna dig: kaliumfosfat (K3PO4): Struktur, egenskaper, användningarOm å andra sidan svavelinnehållet består av anjoner2-, Sulfider beter sig som halvledare och presenterar också joniska konduktiviteter vid höga temperaturer. Detta beror på att deras joner börjar vibrera och röra sig in i kristallerna och därmed transporterar elektriska laddningar.
Optiskt, även om det också beror på dess koppar- och svavelkomposition, kan sulfider kanske eller inte absorbera strålning i det infraröda området i det elektromagnetiska spektrumet. Dessa optiska och elektriska egenskaper gör potentiella material som ska implementeras i olika enheter.
En annan variabler att tänka på, utöver Cu -förhållandet: s, är kristallernas storlek. Det handlar inte bara om mer "svavel" eller "koppary" kopparsulfider, utan deras kristallers dimensioner ger en felaktig effekt på deras egenskaper; Således är forskare angelägna om att studera och leta efter applikationer på nanopartiklar CUxSoch.
Covelita
Varje mineral- eller kopparsulfid har unika egenskaper. Men av dem alla är Covelita den mest intressanta ur en strukturell och estetisk synvinkel (på grund av dess iriscens och blå toner). Därför nämns några av dess egenskaper nedan.
Molmassa
95 611 g/mol.
Densitet
4,76 g/ml.
Smältpunkt
500ºC; Men det bryter ner.
Vattenlöslighet
3,3 · 10-5 G/100 ml vid 18 ° C.
Ansökningar
Nanopartiklar i medicin
Varierar inte bara storleken på partiklarna förrän räckvidd. Således kan kopparsulfid bilda nanosfärer, stavar, plattor, tunna filmer, burar, kablar eller rör.
Dessa partiklar och deras attraktiva morfologier förvärvar enskilda tillämpningar i olika mediciner.
Till exempel kan nanojaulor eller tomma sfärer tjäna som läkemedelstransportörer i kroppen. Nanosferor har använts, stödd av kolglas och kolananorör, för att tjäna som glukosdetektorer; liksom deras aggregat är känsliga för detektering av biomolekyler såsom DNA.
Det kan tjäna dig: 6 naturliga pH -indikatorer och deras egenskaperCus nanorör överstiger nanosferor vid glukosdetektering. Förutom dessa biomolekyler har immunosensorer utformats av tunna filmer av CU och vissa stöd för patogen detektion.
Nanokristaller och amorfa aggregat av CU kan till och med orsaka cancercellapoptos, utan att orsaka skador på friska celler.
Nanovetenskap
I den främre underavsnittet sades det att deras nanopartiklar har varit en del av biosensorer och elektroder. Förutom sådana användningar har forskare och tekniker också utnyttjat sina egenskaper för att utforma solceller, kondensatorer, litiumbatterier och katalysatorer för mycket specifika organiska reaktioner; oumbärliga element i nanovetenskap.
Det är också värt att nämna att när de stöds på aktivt kol visade sig NPCUS-CA-uppsättningen (CA: aktivt kol och NP: nanopartiklar) tjäna som en remover av skadliga färgämnen för människor och därför fungerar som en renare av Källor från källor till vatten som absorberar oönskade molekyler.
Referenser
- Shiver & Atkins. (2008). Oorganisk kemi. (Fjärde upplagan). MC Graw Hill.
- Wikipedia. (2019). Kopparsulfid. Hämtad från: i.Wikipedia.org
- Ivan Grozdanov och Methodija Najdoski. (nittonhundranittiofem). Optiska och elektriska egenskaper hos kopparsulfidfilmer med variabel sammansättning. Journal of Solid State Chemistry Volym 114, nummer 2, 1 februari 1995, sidorna 469-475. doi.org/10.1006/JSSC.nittonhundranittiofem.1070
- Nationellt centrum för bioteknikinformation. (2019). Kopparsulfid (CUS). Pubchemdatabas. CID = 14831. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- Peter a. Ajibade och nandipha l. Bot. (2017). Syntes, optiska och strukturella egenskaper
- av kopparsulfid -nanokristaller från enstaka molekylprekursorer. Institutionen för kemi, University of Fort Hare, Private Bag X1314, Alice 5700, Sydafrika. Nanomaterial, 7, 32.
- Samarbete: Författare och redaktörer av volymerna III/17E-17F-41C (S.F.). Kopparsulfider (Cu2S, Cu (2-X) S) kristallstruktur, laticeparametrar. I: Madelung eller., Rössler u., Schulz m. (eds) Icke-tetrahedralt bundna element och binära föreningar i. Landolt-Börnstein-Group III kondenserad materia (numeriska data och funktionella relationer inom vetenskap och teknik), Vol 41C. Springer, Berlin, Heidelberg.
- Momtan, f., Vafaei, a., Ghaedi, m. et al. Koreanska J. Kem. Göra. (2018). Applicering av kopparsulfid Nanopartiklar Laddat aktivt kol för samtidig adsorption av terminfärgämnen: Svarytmetodik. 35: 1108. doi.org/10.1007/S11814-018-0012-1
- Goel, s., Chen, f., & Cai, W. (2014). Syntes och biomedicinska tillämpningar av kopparsulfid Nanopartiklar: Från sensorer till theranostik. Small (Weinheim an der Bergstrasse, Tyskland), 10 (4), 631-645. Doi: 10.1002/smll.201301174

