Ytspänningsorsaker, exempel, applikationer och experiment

- 734
- 100
- Prof. Erik Johansson
De ytspänning Det är en fysisk egenskap som alla vätskor närvarande och kännetecknas av motståndet att deras ytor motsätter sig någon ökning i deras område. Detta är detsamma som att säga att denna yta kommer att leta efter minst möjliga område. Detta fenomen sammanflätas flera kemiska koncept, såsom sammanhållning, vidhäftning och intermolekylära krafter.
Ytspänningen är ansvarig för bildandet av krökningarna på ytan på vätskorna i rörformiga behållare (graderade cylindrar, kolumner, provrör etc.). Dessa kan vara konkava (dal krökt) eller konvex (krökt kupol). Många fysiska fenomen kan förklaras med tanke på de förändringar som lidit av ytspänningen på en vätska.
 De sfäriska formerna som antagits av vattendroppar på bladen beror delvis på deras ytspänning. Källa: Foto taget av Flickr -användaren Tanakawho [CC av (https: // CreativeCommons.Org/licenser/av/2.0)]
De sfäriska formerna som antagits av vattendroppar på bladen beror delvis på deras ytspänning. Källa: Foto taget av Flickr -användaren Tanakawho [CC av (https: // CreativeCommons.Org/licenser/av/2.0)] Ett av dessa fenomen är den trend som vätskemolekylerna måste agglomerat i form av droppar, när de vilar på ytor som avvisar dem. Till exempel kan vattendropparna som vi ser ovanför bladen inte våta det på grund av dess kulle, hydrofob yta.
Det kommer emellertid en tid då tyngdkraften utövar sin roll och droppen spillas som en vattenspelare. Liknande fenomen förekommer i Mercurys sfäriska droppar när en termometer spillas.
Å andra sidan är ytvattenspänningen den viktigaste av alla, eftersom det bidrar och organiserar statusen för mikroskopiska kroppar i vattenhaltiga medier, såsom celler och deras lipidmembran. Dessutom är denna spänning ansvarig för vatten för att avdunsta långsamt, och några tätaste kroppar som kan flyta på ytan.
[TOC]
Orsaker till ytspänning
Förklaringen av ytspänningsfenomenet är på molekylnivå. Molekylerna i en vätska interagerar med varandra, så att de är sammanhängande i sina oberäknade rörelser. En molekyl interagerar med sina grannar bredvid och de som är över eller under den.
Detta händer emellertid inte samma sak med molekylerna på vätskans yta, som är i kontakt med luften (eller någon annan gas), eller med ett fast ämne. Ytmolekylerna kan inte sammanhålla med de yttre miljön.
Som ett resultat upplever de inte någon kraft som lockar dem; Bara ner, från dess grannar till det flytande mediet. För att motverka denna obalans "pressas ytmolekylerna", för först då lyckas de övervinna kraften som skjuter ner dem.
Kan tjäna dig: natriumsilikat (Na2Sio3): Struktur, egenskaper, användningar, riskerEn yta skapas sedan där molekylerna är i en mer spänd bortskaffande. Om en partikel vill penetrera vätskan måste den först korsa denna molekylära barriär proportionell mot ytspänningen hos nämnda vätska. Detsamma gäller för en partikel som vill fly till den yttre miljön från vätskedjupet.
Därför uppträder ytan som om det var en elastisk film som visar motstånd mot deformer.
Enheter
Ytspänningen representeras vanligtvis med y -symbolen och uttrycks i N/M -enheter, kraft efter längd. Men för det mesta är din enhet dyn/cm. Den ena kan bli den andra genom nästa konverteringsfaktor:
1 dyn/cm = 0,001 N/m
Ytvattenspänning
Vatten är väst och mest överraskande av alla vätskor. Dess ytspänning, liksom flera av dess egenskaper, har ett ovanligt högt värde: 72 dyn/cm vid rumstemperatur. Detta värde kan öka till 75,64 dyn/cm, vid en temperatur av 0 ºC; eller minska till 58,85 ºC, vid en temperatur av 100 ºC.
Dessa observationer är vettiga om det anses att molekylbarriären är spänd ännu mer vid temperaturer nära fryspunkten, eller "lossa" lite mer runt kokpunkten.
Vatten har stor ytspänning efter vätebroar. Om dessa är ökända i vätskan är de ännu mer på ytan. Vattenmolekyler sammanflätas starkt genom att bilda dipol-dipolo-interaktioner av typ H2Åh åh.
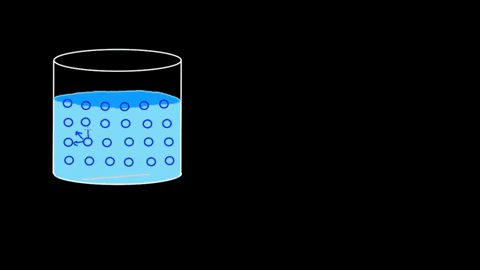 Vattenmolekyler lockar varandra; De är kopplade av vätebroar
Vattenmolekyler lockar varandra; De är kopplade av vätebroar Effektiviteten hos dess interaktioner är sådan att den vattenhaltiga molekylära barriären till och med kan upprätthålla vissa kroppar innan de sjunker. I avsnitten av applikationer och experiment kommer denna punkt att återupptas.
Andra exempel
Alla vätskor har ytspänningar, antingen i mindre eller högre grad än vatten, eller om de är rena ämnen eller lösningar. Hur starka och spända är de molekylära barriärerna för deras ytliga, det kommer att bero direkt på dess intermolekylära interaktioner, utöver strukturella och energifaktorer.
Kondenserade gaser
Till exempel interagerar gasmolekyler i flytande tillstånd endast med varandra genom spridande krafter i London. Detta överensstämmer med att deras ytliga spänningar har låga värden:
-Flytande helium, 0,37 dyn/cm a -273 ºC
Det kan tjäna dig: ammoniumklorid (NH4CL)-Flytande kväve, 8,85 dyn/cm a -196 ºC
-Flytande syre, 13,2 dyn/cm a -182 ºC
Ytspänningen av flytande syre är större än heliumets eftersom dess molekyler har större massa.
Apolära vätskor
Från apolära och organiska vätskor förväntas de ha högre ytspänningar än dessa kondenserade gaser. Bland några av dem har vi följande:
-Dietileter, 17 dyn/cm vid 20 ºC
-n-Hexano, 18,40 dyn/cm vid 20 ºC
-n-Oktan, 21,80 dyn/cm vid 20 ºC
-Toluen, 27,73 dyn/cm vid 25 ºC
En liknande trend observeras för dessa vätskor: ytspänningen ökas när dess molekylmassor ökar. Men n-Octane bör enligt detta ha den största ytspänningen och inte toluenen. Här spelar molekylstrukturerna och geometrierna.
Toluen, plan och anillares molekyler har effektivare interaktioner än de i n-oktan. Därför är toluenens yta "spänd" än ytan på n-oktan.
Polära vätskor
Att vara starkare dipol-dipol. Men det är inte alltid fallet. Bland några exempel vi har:
-Ättiksyra, 27,60 dyn/cm vid 20 ºC
-Aceton, 23,70 dyn/cm vid 20 ºC
-Blod, 55,89 dyn/cm vid 22 ° C
-Etanol, 22,27 dyn/cm vid 20 ºC
-Glycerol, 63 dyn/cm vid 20 ºC
-Smält natriumklorid, 163 dyn/cm vid 650 ºC
-NaCl 6 M -lösning, 82,55 dyn/cm vid 20 ºC
Molten natriumklorid förväntas ha enorm ytspänning: det är en viskös och jonisk vätska.
Å andra sidan är kvicksilver en av vätskorna med den högsta ytspänningen: 487 dyn/cm. I den består dess yta av starkt sammanhängande kvicksilveratomer, mycket mer än vattenmolekylerna kan vara.
Ansökningar
 Vissa insekter använder ytspänningen i vattnet för att gå på det. Källa: Pixabay.
Vissa insekter använder ytspänningen i vattnet för att gå på det. Källa: Pixabay. Enbart ytlig spänning saknar applikationer. Detta betyder emellertid inte att det inte är involverat i flera dagliga fenomen, att om det inte fanns det, skulle de inte hända.
Till exempel kan myggor och andra insekter gå genom vatten. Detta beror på att deras hydrofoba ben avvisar vattnet, samtidigt som deras lilla massa tillåter dem.

Ytlig spänning uppfyller också en roll i vätskevetning. Ju större dess ytliga spänning, desto mindre är dess tendens att läckta genom ett materials porer eller kycklingar. Utöver detta är de lite användbara vätskor för att rengöra ytor.
Kan tjäna dig: neutraliseringsreaktionTvättmedel
Det är här där tvättmedlen verkar, minska ytspänningen i vattnet och hjälpa den att täcka större ytor; När du förbättrar din avfettningsåtgärd. Genom att minska sin ytliga spänning rymmer den luftmolekyler, med vilka bubblor bildas.
Emulsioner
Å andra sidan är låga högre spänningar kopplade till stabiliseringen av emulsioner, mycket viktigt i formuleringen av olika produkter sortiment.
Enkla experiment
 Metallklämma som flyter på grund av ytvattenspänning. Källa: Alvesgaspar [CC BY-S (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]
Metallklämma som flyter på grund av ytvattenspänning. Källa: Alvesgaspar [CC BY-S (https: // CreativeCommons.Org/licenser/BY-SA/3.0)] Slutligen kommer vissa experiment som kan göras i alla inhemska utrymmen att citeras.
Klippexperiment
I ett glas med kallt vatten placeras ett metallklämma på ytan. Som framgår av den övre bilden kommer klippet att förbli flytande tack vare ytspänningen i vattnet. Men om en liten lava Loza läggs till i glaset kommer ytspänningen att minska dramatiskt och klippet plötsligt sjunker.

Pappersbåt
Om vi har ett pappersfartyg eller en träpalett, och om du tvättar det lilla eller tvättmedlet, läggs det till i huvudet på en vattpinne, kommer ett intressant fenomen att inträffa: det kommer att finnas en avvisande som kommer att sprida dem mot kanterna av glaset. Pappersfartyget och träpaletten kommer att röra sig bort från vattpinnen med tvättmedel.

Ett annat liknande och mer grafiskt experiment är att upprepa samma operation, men i en hink med vatten sprutad med svartpeppar. Black Pepper -partiklarna kommer att röra sig bort och ytan kommer från peppar för att vara kristallin, med kanterna vid kanterna.
Referenser
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Wikipedia. (2020). Ytspänning. Hämtad från: i.Wikipedia.org
- USGS. (s.F.). Ytspänning och vatten. Hämtad från: USGS.Gov
- Jones, Andrew Zimmerman. (12 februari 2020). Ytspänning - definition och experiment. Återhämtat sig från: tankco.com
- Susanna lauren. (15 november 2017). Varför är ytspänningen viktig? Biolin Scientific. Återhämtat sig från: blogg.Biolinscientific.com
- Nybörjare. (7 november 2019). Vad är ytspänning | Cool Science Experiment. Återhämtad från: rookieparenting.com
- Jessica mock. (2020). Ytspänningsexperiment. Studie. Återhämtat sig från: studie.com
- Barnet ska se detta. (2020). Sju ytspänningsexperiment - fysikflicka. Återhämtat sig från: thekidenhouldeethis.com

