Valina -egenskaper, funktioner, rika livsmedel, fördelar
- 4563
- 410
- Johan Eriksson
De Valina Det tillhör de 22 aminosyrorna som identifierats som de "grundläggande" komponenterna i proteiner; Det identifieras med förkortningen "Val" och med bokstaven "V". Denna aminosyran kan inte syntetiseras av människokroppen, därför katalogiseras den i gruppen av nio essentiella aminosyror för människor.
Många globulära proteiner har en inre rik på valin och leucinavfall, eftersom båda är associerade med hydrofoba interaktioner och är nödvändiga för vikningen av strukturen och den tre dimensionella konformationen av proteiner.
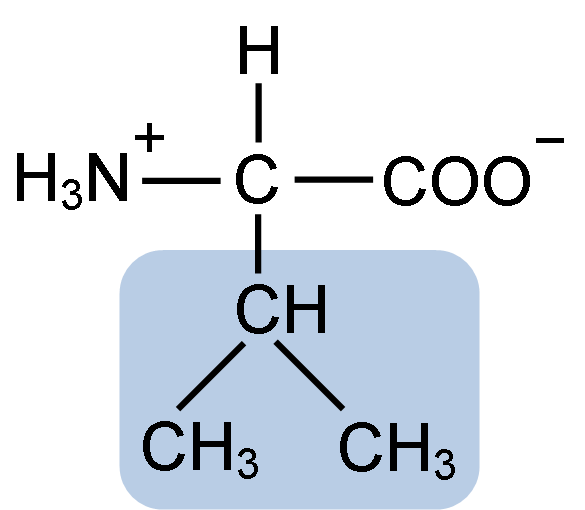
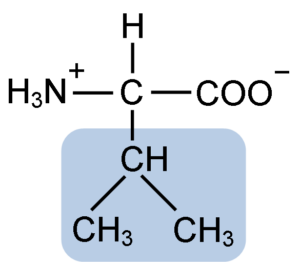 Kemisk struktur av aminosyravalin (källa: Clavecin [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)] via Wikimedia Commons)
Kemisk struktur av aminosyravalin (källa: Clavecin [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)] via Wikimedia Commons) La Valina renades för första gången 1856 av V. Grup-Besanez från ett vattenhaltigt extrakt av bukspottkörteln. Namnet "Valina" myntades dock av E. Fisher 1906, när han lyckades syntetisera det konstgjorda och observerade att dess struktur var mycket lik den för den värdefulla syran, som finns i växter som ofta kallas "Valerianas".
Valinen är en av aminosyrorna som finns i positioner som bevaras i vissa proteiner som delas av ryggradsdjur, till exempel i 80 -positionen för cytokrom C av ryggradsdjur är leucin, valin, isoleucin och metod i samma ordning i samma ordning.
I vävnader eller biomaterial med resistenta, hårda och elastiska egenskaper som ligament, senor, blodkärl, trådar eller webb, finns det stora mängder valin, som ger flexibilitet och resistens tack vare dess hydrofoba interaktioner med andra aminosyror.
En ersättning av en glutamatrest med en av valin i p -kedjan av hemoglobin, proteinet som ansvarar för transport av syre med blod orsakar dålig bildning i proteinstrukturen, vilket orsakar hemoglobin "S".
Denna mutation producerar falciform anemi eller drepanocytos, ett patologiskt tillstånd där röda blodkroppar förvärvar en form av halvmåne eller karakteristiska HOZ, som skiljer dem från normalt, rundat och plattat utseende.
Några av de mest använda herbiciderna har för närvarande aktiva föreningar till sulfonylurea och metylsulfometuron, som orsakar skador på enzymet acetolaktatsyntas, nödvändigt för det första syntessteget av valin, leucin och isoleucin. Skadorna som orsakas av dessa bekämpningsmedel förhindrar örter och ogräs kan normalt utvecklas.
[TOC]
Egenskaper
Valina är en aminosyra med ett fem -kolskelett och tillhör aminosyragruppen med alifatiska sidokedjor. Dess hydrofoba karaktär är sådan att den kan jämföras med fenylalanin, leucin och den hos isoleucin.
Aminosyror som har kolvätekedjor i sina r- eller sidokedjor är ofta kända i bibliografi som grenade eller grenade kedjaminosyror. I denna grupp finns valin, fenylalanin, leucin och isoleucin.
I allmänhet används aminosyrorna i denna grupp som inre strukturella element i proteinsyntes, eftersom dessa kan associeras med varandra genom hydrofoba interaktioner, "fly" från vatten och etablerar den karakteristiska strukturella vikningen av många proteiner.
Dess molekylvikt är cirka 117 g/mol och eftersom dess R- eller sidokedjegrupp är ett grenat kolväte har den ingen belastning och dess relativa överflöd i proteinstrukturer är lite större än 6%.
Strukturera
La Valina delar den allmänna strukturen och de tre typiska kemiska grupperna i alla aminosyror: karboxylgruppen (COOH), aminogruppen (NH2) och en väteatom (-H). I sin R- eller sidokedjegrupp har den tre kolatomer som ger den mycket hydrofoba egenskaper.
Kan tjäna dig: inerta varelser: egenskaper, exempel, skillnader med levande varelserSom är sant för alla kemiska föreningar som klassificeras som "aminosyror", har valinen en central kolatom som är chiral och som kallas α -kol, till vilka de fyra kemiska grupperna nämns.
Valinens IUPAC är 2-3-amino-3-butanóic.
Alla aminosyror finns i D- eller L -formen och valinen är inget undantag. L-värdeformen är emellertid mycket mer riklig än D-valleinformen och dessutom är den spektroskopiskt mer aktiv än formen D.
L-värde är den form som används för bildning av cellproteiner och är därför, av de två, den biologiskt aktiva formen. Det uppfyller funktioner som nutraceutical, mikronäringsämne för växter, metabolit för människor, alger, jäst och bakterier, bland många andra funktioner.
Funktioner
Valina, trots att den är en av de nio essentiella aminosyrorna, spelar inte en ytterligare roll i sitt deltagande i proteinsyntes och som en metabolit i sin egen nedbrytningsväg.
Men skrymmande aminosyror som valin och tyrosin är ansvariga för flexibiliteten i fibroin, huvudproteinkomponenten i sidentrådar som produceras av arten av arten Bombyx Mori, Vanligtvis känd som silke eller mullbärsträd maskar.
Vävnader som arteriellt blodligament och glas består av ett fibröst protein som kallas elastin. Detta består av polypeptidkedjor med upprepade sekvenser av glycin-, alanin- och valinaminosyror, den viktigaste återstoden med protein.
Valina deltar i de viktigaste syntesvägarna för de föreningar som är ansvariga för den karakteristiska lukten av frukt. Valina -molekyler omvandlas till metylerade och grenade derivat av estrar och alkoholer.
I livsmedelsindustrin
Det finns många kemiska tillsatser som använder valin i kombination med glukos för att få aptitretande lukt i vissa kulinariska beredningar.
Vid en temperatur av 100 ° C har dessa tillsatser en karakteristisk lukt av råg och mer än 170 ° C lukt i varm choklad, så de är populära inom livsmedelsproduktion inom Baker och konditorivaror (bakverk).
Dessa kemiska tillsatser använder artificiellt syntetiserad L-Valin.
Biosyntes
Alla grenade aminosyror som valin, leucin och isoleucin syntetiseras huvudsakligen i växter och bakterier. Vilket innebär att djur som människa och andra däggdjur behöver äta livsmedel som är rika på dessa aminosyror för att kunna uppfylla deras näringskrav.
Vanligtvis börjar biosyntesen av valinen med överföring av två kolatomer från hydroxetyl -typaminpyrofosfat till pyruvatet genom verkan av enzymet ocetohydroxi -isomer -syrareduktas syra.
De två kolatomerna härstammar från en andra pyruvatmolekyl genom en TPP-beroende reaktion som är mycket lik den katalyserade av enzymdiskenpyylaspyruvatet, men som katalyseras av dihydroxy-syra-dehydratas.
Enzymet Valina aminotransferas innehåller slutligen en aminogrupp till ketoacidföreningen till följd av den främre dekarboxyleringen, som bildar L-Valin. Leucin-, isoleucin- och valinaminosyror har en stor strukturell likhet, och det beror på att många mellanhänder och enzymer delar på sina biosyntetiska rutter.
Det kan tjäna dig: Flora och Fauna de Salta: Mer representativa arterKetoaciden som producerats under biosyntesen av L-valin reglerar några enzymatiska steg genom negativ feedback eller alosterisk reglering på den biosyntetiska vägen för leucin och andra relaterade aminosyror.
Detta innebär att biosyntetiska rutter hämmas av en metabolit som genereras i dem som, när de ackumuleras, ger celler en specifik signal som säger dem att en viss aminosyra är överdrivet och därför kan dess syntes stoppa.
Degradering
De tre första nedbrytningsstegen i valinen delas på nedbrytningsvägen för alla grenade kedjaminosyror.
Valina kan komma in i Krebs citronsyrcykel för att förvandlas till succinyl-CoA. Nedbrytningsvägen består av en initial transaminering, katalyserad av ett enzym som kallas aminotransferas av grenade kedjaminosyror (BCAT).
Detta enzym katalyserar en reversibel transamination som lyckas omvandla de grenade kedjaminosyrorna till deras motsvarande grenade kedja a-zo-stoats.
I denna reaktion är deltagandet av glutamat/2-zotoglutaratmomentet viktigt, eftersom 2-zotoglutaraten får aminogruppen som tas bort från aminosyran som metaboliseras och blir glutamat.
Detta första reaktionssteg i katabolismen i valinen producerar 2-cetoisavaleratet och åtföljs av omvandlingen av pyridoxal 5'-fosfat (PLP) i pyridoxamin 5'-fosfat (PMP).
Därefter används det 2-cetoisvaleratet som ett substrat i ett mitokondriellt enzymatiskt komplex, känt som a-a-zo-stoats i grenad kedja, som tillför en coash-del och bildar isobutiril-CoA, som därefter dehydrogenerad och förvandlas till metakrililiil -COA.
Metakrylil-CoA bearbetas nedströms i ytterligare 5 enzymatiska steg som involverar hydrering, eliminering av coash-delen, oxidation, tillsats av en annan coash-del och molekylär omorganisation, som slutar med produktionen av succinyl-CoA, som omedelbart går in i krebscykeln.
Livsmedel rika på Valina
Proteinerna i sesam- eller sesamfrön är rika på Valina, med nästan 60 mg aminosyran för varje gram protein. Av denna anledning rekommenderas kakor, kex och sesamstänger eller nougat för barn med bristfälliga dieter av denna aminosyra.
Soya -korn är i allmänhet rika på alla essentiella aminosyror, även i Valina. De är emellertid dåliga i metionin och cystein. Proteinet eller sojastrukturen har mycket komplexa kvartära strukturer, men som är lätta att lösa upp och separera i mindre underenheter i närvaro av gastriska juicer.
Casein, som vanligtvis är i mjölk och dess derivat, är rika på upprepade sekvenser av Valina. Liksom sojabönor försämras detta protein lätt och absorberas i tarmkanalen hos däggdjur.
Det har uppskattats att för varje 100 gram sojaprotein intas cirka 4,9 gram valin; Medan för varje 100 ml mjölk intas cirka 4,6 ml Valina.
Andra livsmedel som är rika på nämnda aminosyra är nötkött, fisk och olika typer av grönsaker och grönsaker.
Fördelar med ditt intag
Valin, som en stor del av aminosyror, är en glykogen aminosyra, det vill säga den kan införlivas i den glukoneogena vägen, och många neurologer bekräftar att deras intag hjälper till att upprätthålla mental hälsa, muskulös samordning och minska stress.
Kan tjäna dig: de 5 grenarna i huvudbioteknikenMånga idrottare konsumerar komprimerad i Valina, eftersom de hjälper regenerering av vävnader, särskilt muskelvävnader. Att vara en aminosyran som kan gå med i glukoneogenes hjälper energiproduktion, vilket inte bara är viktigt för fysisk aktivitet utan för nervfunktion.
Valina Foods hjälper till att upprätthålla balansen mellan kväveföreningar i kroppen. Denna balans är avgörande för generering av energi från de intagna proteinerna för kroppstillväxt och läkning.
Dess konsumtion förhindrar skador på levern och gallblåsan, samt bidrar till optimering av många kroppsfunktioner.
En av de mest populära kosttillskott mellan idrottare för att öka muskelvolymen och muskelåtervinningen är BCAA.
Dessa typer av tabletter består av tabletter med blandningar av olika aminosyror bland vilka vanligtvis ingår aminosyror såsom L-Valin, L-isoleucin och L-leucina; De är också rika på vitamin B12 och andra vitaminer.
Vissa experiment med grisar har visat att valinkraven är mycket högre och mer begränsande för mödrar under amningsstadiet, eftersom denna aminosyran hjälper till att utsöndra mjölk och ger förbättringar i tillväxthastigheten för spädbarnsnöster.
Brist
Dagligt valinintag som rekommenderas för spädbarn är cirka 35 mg för varje gram protein som konsumeras, medan för vuxna är mängden lite lägre (cirka 13 mg).
Den vanligaste sjukdomen relaterad till valinen och andra grenade aminosyror kallas "urinsjukdom med arce sirap" eller "ketoaciduria".
Detta är ett ärftligt tillstånd orsakat av en defekt i generna som kodar för dehydrogena enzymerna från a-zo-syrorna härrörande från leucin, isoleucin och valin, som är nödvändiga för att metabolisera dem.
I denna sjukdom kan organismen inte assimilera någon av dessa tre aminosyror när de erhålls från kosten, därför härledda ketoacider ackumuleras och utvisas i urinen (de kan också detekteras i blodserumet och i cerebrospinalvätskan).
Å andra sidan har en dålig diet i Valina varit relaterad till neurologiska patologier som epilepsi. Det kan också orsaka viktminskning, Huntingtons sjukdom och kan till och med hamna i utvecklingen av vissa typer av cancer, eftersom vävnadsreparationssystemet och syntesen av biomolekyler äventyras.
Referenser
- Abu-baker, s. (2015). Granskning av biokemi: koncept och anslutningar
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger principer för biokemi. Macmillan.
- PLIMMER, R. H. TILL., & Phillips, h. (1924). Analys av proteiner. Iii. Uppskattning av histidin och tyrosin genom bominering. Biochemical Journal, 18 (2), 312
- PLIMMER, R. H. TILL. (1912). Proteins kemiska konstitution (Vol. 1). Longmans, grönt.
- Torii, k. TILL. Z. ELLER. ANTINGEN., & Iitaka och. (1970). Kristallstrukturen i L-valin. Crystallographica Avsnitt B: Strukturell kristallografi och kristallkemi, 26 (9), 1317-1326.
- Tosti, v., Bertozzi, b., & Fontana, L. (2017). Hälsofördelar med Medelhavsdieten: Metaboliska och molekylära mekanismer. The Journals of Gerontology: Series A, 73 (3), 318-326.

