Chrome Oxide (III) Struktur, nomenklatur, egenskaper, användningar

- 2676
- 318
- Johan Olsson
han Kromoxid (iii) U -kromoxid är ett oorganiskt grönt fast ämne som bildas genom att bränna krommetall (CR) i syre (eller2), lämnar krom med oxidationstillstånd 3+. Dess kemiska formel är cr2ANTINGEN3. I naturen finns det i Eskolaíta mineral. Naturliga avlagringar av kromoxid (iii) är inte kända.
Det kan beredas bland annat genom att värma cr2ANTINGEN3 hydratiserad (cr2ANTINGEN3.Nh2O) för att ta bort vatten helt. Det erhålls också som en produkt av kromoxidkalkinering (VI) (CRO3).
 Kromoxidpigment (III). FK1954 [Public Domain]. Källa: Wikipedia Commons
Kromoxidpigment (III). FK1954 [Public Domain]. Källa: Wikipedia Commons Men det bästa sättet att få det rent är genom nedbrytning av ammoniumdikromaten (NH4)2Cr2ANTINGEN7 vid 200 ºC. Industriellt produceras genom reduktion av natriumdikromat (NA2Cr2ANTINGEN7) fast med svavel.
När det är fint uppdelat presenterar det en ljusgrön färg med gulaktig nyans. Men om partiklarna är större visar det ett blåaktigt färgämne. Kromoxid är det mest stabila gröna pigmentet som är känt. Dess termiska och kemiska motstånd gör det till ett värdefullt keramiskt färgämne.
Det används i industriella beläggningar, lack, i byggbranschen, i smycken, som en färg i kosmetika eller i läkemedelsprodukter, bland andra applikationer.
[TOC]
Strukturera
A-Croxid2ANTINGEN3 Den har Corindon -typstrukturen. Dess kristallina system är rhomboonic hexagonalt. Är isomorf med α-alumina och a-Fe2ANTINGEN3.
Eskolaíta, naturligt mineral av kromoxid (III), presenterar strukturen som visas nedan:
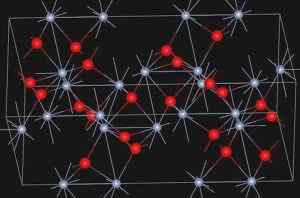 Crystal Structure of Eskolaíta Mineral. https: // ladda upp.Wikimedia.org/wikipedia/commons/e/ee/eskolaite_structure.Jpg. Källa: Wikipedia Commons
Crystal Structure of Eskolaíta Mineral. https: // ladda upp.Wikimedia.org/wikipedia/commons/e/ee/eskolaite_structure.Jpg. Källa: Wikipedia Commons Nomenklatur
- Kromoxid (iii).
- Grön kromoxid.
- Dikromtrioxid.
- Kromhavsquioxid.
- Kromi.
- Eskolaíta: Chrome Oxide Mineral (III).
- Hydrat: Cr2ANTINGEN3.Nh2Eller (där n ≅ 2) kallas kromoxidhydrat (iii) eller Guignet Green.
 Kromoxidhydrat (III). W. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikipedia Commons
Kromoxidhydrat (III). W. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikipedia Commons Egenskaper
Fysiskt tillstånd
Kristallt fast.
Mohs hårdhet
9 (deras kristaller är extremt hårda).
Molekylvikt
151,99 g/mol.
Kan tjäna dig: kvartära föreningar: egenskaper, träning, exempelSmältpunkt
Smälter vid 2435 ºC, men det börjar avdunsta till 2000 ºC bildar moln av grön rök.
Densitet
5.22 g/cm3
Löslighet
När den har värmts vid höga temperaturer är den praktiskt taget olöslig i vatten (3 mikrogram/L vid 20 ° C); olöslig i alkoholer och aceton; något lösligt i syror och alkalier; Perklorsyra SSSOLUBLE (HCLO4) till 70%, där det bryter ner.
pH
6.
Brytningsindex
2,551.
Andra egenskaper
- Om det är starkt kalcinerat blir det inert mot syror och baser. Annars cr2ANTINGEN3 och dess hydratiserade form cr2ANTINGEN3.Nh2O De är amfoteriska, lätt upplöses i syra för att ge aqua -ioner [Cr (h2ANTINGEN)6]3+, och i koncentrerad alkali för att bilda "Chromitos".
- När det har kalcerats är den kemiskt resistent mot syror, alkalier och höga temperaturer. Är extremt stabilt för så2.
- Det har ett enastående motstånd mot ljus eftersom dess kristaller har opacitet, hög UV -dämpning och transparens till synligt ljus.
- Det är ett extremt hårt material, du kan skrapa kvarts, tapacio och zirkonio.
- Dess hydrat cr2ANTINGEN3.Nh2Eller (där n ≅ 2) inte har termisk stabilitet begränsar dess hydratiseringsvatten dess tillämpbarhet till mindre än 260 ºC. Det ger låg färgningskapacitet och begränsad nyans av nyanser.
- Men detta hydrat har en mycket ren och ljus grönblå nyans. Det är halvtransparent, presenterar låg opacitet, utmärkt motstånd mot ljus och motstånd mot alkalis.
- Cr2ANTINGEN3 Det klassificeras inte som farligt material och anses vara ett inert fint pulver. Det är inte föremål för internationella transportregler.
- Irriterar inte huden eller slemhinnan.
Ansökningar
I keramik- och glasindustrin
På grund av dess höga motstånd mot värme och kemisk motstånd, CR2ANTINGEN3 Kalkinerad används som färgfärg eller vitrifierbart pigment i keramisk tillverkning, i porslinemaljer och blandningar för glas.
I industribeläggningar
Keramik med kromoxid (III) ger utmärkt motstånd mot de flesta frätande miljöer. Allt detta genom mekanismen för uteslutning av det omgivande underlaget.
Av denna anledning används den i beläggningar för att förhindra korrosion av många material, appliceras av termisk spray (atomisering eller varm dagg).
Kan tjäna dig: kemisk process: principer, typer, exempelDet används också som skydd mot slitande slitage (när avlägsnande av materialet orsakas av partiklar som rör sig genom en yta).
I dessa fall är appliceringen av en CR -beläggning2ANTINGEN3 Genom avsättning med plasma genererar den hög nötningsresistens.
De två föregående fallen har till exempel användbarhet i gas turbaciala turbinmotorer.
I den eldfasta branschen
Det används i termiskt och kemiskt resistenta tegelstenar, beläggningsmaterial och aluminiumoxidbaserad eldfast betong.
Under konstruktion
Eftersom det är extremt resistent mot atmosfäriska förhållanden, ljus och värme, appliceras det som ett granulerat bergfärg för asfalttak, betongcement, högkvalitativa industribeläggningar för yttre, stålkonstruktioner och fasaderbeläggningar (emulsionbara färger).
Som pigment i olika applikationer
Det kan stödja vulkaniseringsförhållanden och försämras inte, så det används vid gummipigmentering.
Eftersom de är icke-tekniska används det som ett pigment för leksaker, kosmetika (särskilt dess hydrat), plast, tryckfärger, målningar som kommer i kontakt med mat och läkemedelsprodukter.
I pigmentindustrin används den som råmaterial för att producera penetrerande färgämnen som innehåller krom och pigment baserade på faser av blandade metalloxider. Det används också som en färgning av målningar för spolbeläggning.
Dess hydrat har en transparens som möjliggör formulering av polykromatiska ytbehandlingar inom bilindustrin (metallbilsfinish).
På grund av dess unika egenskap för att reflektera infraröd strålning (IR) som liknar växter Klorofyll, under infraröd ljus verkar det bladverk. Av denna anledning är dess användning i kamouflagemålningar eller beläggningar för militära tillämpningar mycket utbredd.
I smycken
Det används som ett färgämne av syntetiska ädelstenar. När CR introduceras2ANTINGEN3 som orenhet i det kristallina nätverket av a-al2ANTINGEN3, Liksom i det halvkänsliga rubinmineralet är färgen röd istället för grön.
Det används också som slipmedel och polerat för hög hårdhet och slipande egenskaper.
Vid kemiska reaktioner
Stöds i aluminiumoxid (till2ANTINGEN3) eller andra oxider, används i organisk kemi som en katalysator, till exempel i hydreringen av estrar eller aldehyder för att bilda alkoholer och i kolvätercyklisering. Katalyserar reaktionen av kväve (n2) med väte (h2) Att bilda ammoniak (NH3).
Det kan tjäna dig: litium: historia, struktur, egenskaper, risker och användningarFör sin oxidreduktionskapacitet som verkar tillsammans med kromoxid (VI) spelar en viktig roll i dehydrogeneringen av alkaner2 För att producera propen och isobuten, eftersom katalysator-deaktiveringsreaktiveringscykeln är lätt körbar. Det används också som en katalysator i oorganisk kemi.
I kromtillverkning
Det används i ren krommetall aluminotermisk produktion. För att göra detta måste det värmas till 1000 ºC för att öka sin kornstorlek.
 Krommetallberedning genom aluminoterm reduktion av kromoxid (III). Rando Tuikene [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Källa: Wikipedia Commons
Krommetallberedning genom aluminoterm reduktion av kromoxid (III). Rando Tuikene [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Källa: Wikipedia Commons I magnetiska material
Det har lagts till i små mängder till magnetiska material av ljud- och videoband genom att lära en självuttryckande effekt till sunda huvuden.
Nya innovationer
Det har erhållits pigment som har förbättrat reflektansen av att gå till Dopar CR Nanoparticles2ANTINGEN3 med salter av element som tillhör den sällsynta jordgruppen, till exempel Lantano och Praseodimio.
Ökning av koncentrationen av dessa element ökar solreflektansen för den nära infraröda utan att påverka den gröna färgen på CR -grisen2ANTINGEN3.
Detta gör det möjligt att klassificera CR2ANTINGEN3 doping som "kallt" pigment, eftersom det är lämpligt för att kontrollera värmeansamling.
Tillämpas på tak, bilar och klädsel, bland andra applikationer, uppnår hög reflektion av IR -solljus, vilket gör att vi kan minska värmeökningen i miljöer avsevärt i.
Referenser
- Bomull, f. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Kirk-THERMER (1994). Encyclopedia of Chemical Technology. Volym 19. Fjärde upplagan. John Wiley & Sons.
- Ullmanns Encyclopedia of Industrial Chemistry. (1990). Femte upplagan. Volym A7 och A20. VCH Verlagsgellschaft MBH.
- Amerikanska element. (2019). Krom (iii) oxid. Återhämtat sig från amerikanerna.com.
- National Library of Medicine. (2019). Krom (iii) oxid. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov.
- Dorfman, Mitchell R. (2012). Termisk spraybeläggningar. I handbok för miljöförstöring av material. Kapitel 19. Återhämtat sig från Scientedirect.com.
- Takehira, K. et al. (2004). Co2 Dehydrogenering av propan över CR-MCM-41-katalysator. I studier i ytvetenskap och katalys 153. Återhämtat sig från Scientedirect.com.
- Selvam sangeetha et al. (2012). Funktionella pigment från krom (iii) nanopartikeloxid. Färgämnen och pigment 94 (2012) 548-552. Återhämtat sig från Scientedirect.com.

