Grundläggande oxider

- 1512
- 216
- Johan Eriksson
Vi förklarar vad de grundläggande oxiderna är, hur deras egenskaper, nomenklatur och ger flera exempel bildas,
 Många grundläggande oxider har slående, karakteristiska för metallfärger
Många grundläggande oxider har slående, karakteristiska för metallfärger Vad är grundläggande oxider?
De grundläggande oxider De är oorganiska föreningar som bildas av föreningen mellan syre och en metall. De kallas basiska oxider eftersom de producerar alkaliska eller grundläggande lösningar när de löses i vatten. Även för att de reagerar med syror för att bilda ett salt och vatten genom en syra-basneutraliseringsreaktion.
Grundläggande oxider är mycket vanliga. Faktum är att de flesta metaller i naturen finns i oxider jordar, så de brukade kallas land.
Grundläggande oxider är av stor betydelse för branschen. Många färgade pigment som används i branschen är oxider. Andra oxider används som bas för målningar, särskilt titan-, bly- och zinkoxider.
Grundläggande oxideregenskaper
De är binära föreningar
Dessa föreningar bildas endast av två element: syre och en metall. Därför är de binära föreningar.
Dess empiriska formel är m2ANTINGENX eller moX/2
Syreens valens i oxider är alltid -2, så de empiriska formlerna för oxiderna förenklas när metallen Valencia är ett vridmomentantal. Detsamma händer dock inte när det är konstigt.
Till exempel är den empiriska formeln av natriumoxid NA2Eller för att natrium har Valencia +1 (udda). Istället är den empiriska formeln för kalciumoxid CAO, eftersom kalcium har Valencia +2.
De är oorganiska föreningar, nästan alltid joniska
De flesta grundläggande oxider är kristallina joniska föreningar. Detta inkluderar oxiderna i alla alkaliska metaller, av alla alkaliners (med undantag för beryllium) och den första serien av övergångsmetaller.
Kan tjäna dig: kemisk bindningDe har mycket höga fusions- och kokpunkter
Den joniska bindningen håller alla joner som bildar grundläggande oxider starkt förenade. Detta gör dem svåra att smälta och ännu svårare att förånga. Av denna anledning har de mycket höga fusions- och kokpunkter.
De är solida vid rumstemperatur
På grund av samma faktum att ha höga fusionspunkter är alla grundläggande oxider solida vid rumstemperatur.
De är grundläggande föreningar
Anledningen till att de kallas basiska oxider är just på grund av dess syrabasegenskaper. Oxider med större jonisk karaktär producerar grundläggande lösningar när de löses i vatten och reagerar också med syror, neutraliserar dem.
Det bör dock noteras att inte alla metalloxider är grundläggande. Vissa är neutrala, andra syror och andra amfotor.
De flesta är lite lösliga eller olösliga i vatten
Alla grundläggande oxider är olösliga i vatten, med undantag av alkaliska och bariummetalloxider. De är emellertid lösliga i syralösningar.
Hur är grundläggande oxider?
Grundoxider kan bildas spontant när metaller utsätts för luftsyre. I själva verket består korrosionslager som bildas på ytan av metaller av olika basoxider.
Metallen är i allmänhet en alkalisk, alkalisk metall eller en övergångsmetall.
Du kan skriva tre allmänna reaktioner för bildning av oxider, beroende på om metallen Valencia är jämn eller udda:
För metaller med udda valenser:
När metallen har udda valens är den allmänna reaktionen av oxidbildning:

Till exempel för bildning av natriumoxid, där natrium har Valencia +1, är reaktionen:
Det kan tjäna dig: fosfor: historia, egenskaper, struktur, erhållning, användning
Ett annat exempel är bildningen av järnoxid, där järn har oxidation eller Valencia +3. I detta fall är reaktionen:

För metaller med Valencia +2:
När metallen har Valencia +2 är den allmänna reaktionen av oxidbildning:

Till exempel, när det gäller bildning av kalciumoxid, där kalcium har Valencia +2, är reaktionen:

För metaller med andra par:
När metallen har till och med valenser utöver +2 är den allmänna reaktionen av oxidbildning:
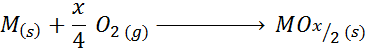
Ett exempel på detta fall är titanoxidbildningsreaktionen (IV):

Grundläggande oxider nomenklatur
Det finns tre nomenklatursystem för de grundläggande oxiderna som är: den traditionella nomenklaturen, beståndet och det systematiska.
För att namnge en oxid enligt de två första nomenklatursystemen är det nödvändigt att känna till Metal Valencia, medan för det sista.
Traditionell nomenklatur
Enligt den traditionella nomenklaturen heter Basic Oxides från och med ordet antingenXido följt av katjonnamnet. Detta efternamn är byggt genom att placera roten till metallnamnet och ett system med prefix och suffix som indikeras av Metal Valencia:
Oxid + Prefix-raí-sufijo
Reglerna för att tilldela prefix och suffix sammanfattas i följande tabell:
Antal möjliga valenser | Valencia | Prefix | Ändelse |
1 Single Valencia | |||
Endast | --- | ___ico | |
2 Valencias | |||
Äldre | --- | ___ico | |
Mindre | --- | ___Björn | |
3 valenser | |||
Äldre | --- | ___ico | |
Mellanliggande | --- | ___Björn | |
Mindre | Hicka___ | ___Björn | |
4 valenser | |||
Äldre | Per___ | ___ico | |
Stora mellanliggande | --- | ___ico | |
Mindre mellanliggande | --- | ___ico | |
Mindre | Hicka___ | ___ico |
Exempel:
han Tro2ANTINGEN3 Det är en järnoxid med Valencia +3. Järn har bara två valenser som är +2 och +3, så i detta oxid har järnet den äldsta av två valenser. Av denna anledning läggs suffixet till ___ico vid roten till namnet på järnmetallen som är Ferr-.
Det kan tjäna dig: inga elektrolyter: egenskaper och exempelDärför det traditionella namnet på Tro2ANTINGEN3 är: Järnoxid.
Beståndsnomenklatur
I det här systemet byggs namnet från orden oxid av, följt av metallnamn. Slutligen placeras hans Valencia i romerska antal inom parentes:
Metall + namnoxid (Valencia)
Om metallen bara har en valens, utelämnas den.
Exempel:
I cr2ANTINGEN3 Chromium har Valencia +3, så namnet är Kromoxid (iii).
Systematisk nomenklatur
Detta är den enda av de tre nomenklaturerna som inte anger metallen Valencia. Sitematiska namn indikerar hur många syre- och metallatomer som innehåller föreningen med numeriska prefix.
Namnet är byggt med ordet oxid föregående av honom prefix som anger antalet syre, Sedan artikeln av följd av Metallnamn med respektive prefix.
Prefix-oxid + av + prefix-metall
Vissa prefix är:
siffra | Prefix |
1 | Bulle |
2 | Gav av |
3 | Tri |
4 | Tetra |
5 | Penta .. |
Exempel:
I den systematiska nomenklaturen, cr2ANTINGEN3 Det kallas dikromtrioxid, eftersom den har tre syre och två kromos.
Exempel på grundläggande oxider
- Natriumoxid - NA2ANTINGEN
- Järnoxid - tro2ANTINGEN3
- Järnmonoxid - ful
- Cromic Oxide - Cr2ANTINGEN3
- Divanadio pentaoxid - v2ANTINGEN5
- Kaliumoxid - k2ANTINGEN
- Bariumoxid - Bao

