Natriumbensoatstruktur, egenskaper, användningar och risker
- 2037
- 464
- Johan Gustafsson
han natriumbensoat Det är ett organiskt salt vars kemiska formel är c6H5Väg. Det förekommer eller genereras genom neutraliseringsreaktion mellan bensoesyra och natriumhydroxid. Resultatet är ett vitt fast ämne (lägre bild) i vattnet och sönderdelas genom att värma vid 120 ºC.
Detta salt kan hittas naturligt i flera frukter och andra delar av grönsaker, till exempel: blåbär, plommon, russin, kanel, lukt naglar och äpplen. Det är också en metabolit av alger och växter.
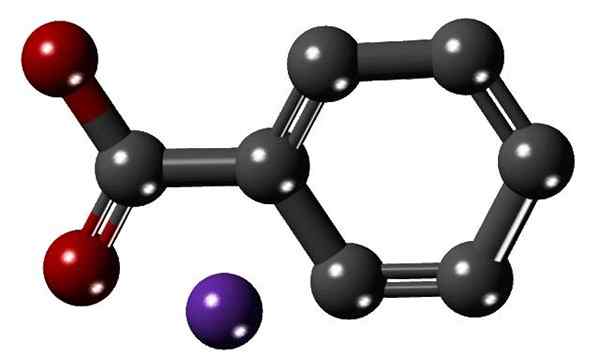
 Natriumbensoat. Källa: Chemik10 på Polish Wikipedia [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]
Natriumbensoat. Källa: Chemik10 på Polish Wikipedia [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)] Natriumbensoat samlas inte i kroppen, eftersom det snabbt kombineras med glycinaminosyra för att bilda hippursyra, som fritt utsöndras i urin.
Denna förening används med livsmedelskonserveringsmedel, dess verkan är mer effektiv för ett surt pH. Detta beror på närvaron av organiska syror som ger mat ett pH som är lämpligt för verkan av natriumbensoat; Det som sådan slutar det med att protonsera i bensoesyra.
Detta salt används också vid behandling av ärftliga metaboliska störningar i ureacykeln, som producerar ackumulering av en mellanliggande metabolit, för vilken enzymet som bearbetar det är dåligt.
Det internationella kemiska säkerhetsprogrammet fann ingen skadlig effekt av natriumbensoat på människor, för konsumtion mellan 647 - 825 mg/kg kroppsmassa.
Det har emellertid rapporterats att natriumbensoat kan producera pseudoallergiska reaktioner och förvärra symtom hos patienter med ofta urticaria -episoder och astma.
[TOC]
Natriumbensoatstruktur
 Natriumbensoatstruktur. Källa: Kamil9243 [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]
Natriumbensoatstruktur. Källa: Kamil9243 [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)] Den övre bilden visar strukturen för natriumbensoat med en modell av sfärer och staplar. Den aromatiska ringen, med karboxylatgruppen, kan märkas med karboxylatet-, kopplad till honom (det för de röda sfärerna); och den senare lockar i sin tur elektrostátiskt till na katjonen+ (lila sfär).
Eftersom skillnaden i storlek mellan båda jonerna är stor (jämför i bilden) är det inte konstigt att natriumbensoatkristallernas retikulära energi är låg. Detta får deras kristaller att ha en naturlig tendens att solubilisera i polära lösningsmedel eller drabbas av en serie kemiska reaktioner.
Kan tjäna dig: Gaseous State: Egenskaper, allmän lag, exempelC6H5Kuttra- Du kan acceptera två vätebroar från två vattenmolekyler, vilket gynnar dess hydrering. Under tiden NA+ Det slutar också solvated av vatten och övervinner de elektrostatiska krafterna som håller det tillsammans med C6H5Kuttra-.
Således består detta salt av cjoner6H5Kuttra- och na+, som är ordnade på ett ordnat sätt att bygga kristaller. I litteraturen uppnås inte information om dess kristallina struktur, så det är okänt vad typen av enhetscell för detta salt är.
[TOC]
Egenskaper
Kemiska namn
-Natriumbensoat
-Natriumsalt av bensoesyra
-Sobenato
-Antimol.
Fysisk beskrivning
Vita granuler eller kristallint damm. Färglöst kristallint pulver.
Lukt
Toalett.
Smak
Bittersöt, sammandragande och obehagliga.
antändningspunkt
> 100 ºC.
Självtändning
> 500 ºC.
Densitet
1,50 g/cm3.
Löslighet
-Lösligt i flytande ammonium och pyridin.
-LITT LOLLUBLE i etanol: 8,22 g/100 g vid 25 ° C.
-I metanol är den mer löslig än i etanol: 8,22 g/100 g vid 15 ° C.
Stabilitet
Det är stabilt under de rekommenderade lagringsförhållandena. Det kan vara känsligt för fukt, hydrolysering till bensoesyra. Oförenlig med starka oxiderande medel, alkalier och mineralsyror.
Sönderfall
När den värms upp till sönderdelning till 120 ºC (248 ºF) avger den en tunnland rök av natriumoxid och andra komponenter som kan vara giftiga och cancerframkallande.
Genom att sönderdela 120 ° C förhindrar det att dess kokning och fusionspunkter bestäms exakt, de rapporterade värdena för dessa teoretiska uppskattningar av parametrarna är.
pH
Nära 8, upplöst i vatten. Det vill säga, det är ett grundläggande salt. Detta beror på att det är hydrolyserat för att frigöra joner OH-.
Ytspänning
72,9 mn/cm vid 20 ºC i en lösning av 1 g/l vatten.
Syntes
Benzoesyran involverad i syntesen av natriumbensoat produceras huvudsakligen med tre metoder:
-Naftalen oxideras med vanadiumpentoxid för att bilda ftálisk anhydrid. Denna förening kan underboxilera för att komma från bensoesyran, eftersom den i dess struktur med två aromatiska ringar verkar ha två grupper -kondensatbil med varandra.
-Toluen oxideras till bensoesyra genom att tillsätta salpetersyra. I denna reaktion oxiderar "helt enkelt" metilo -gruppen karboxylgruppen:
C6H5Ch3 => C6H5Cooh
-Och slutligen hydrolyseras bensotriclorid av verkan av mineralsyror, vilket orsakar bensoesyra.
Kan tjäna dig: keramiska material: egenskaper, typer, exempelErhållen bensoesyra av någon av dessa tre metoder, upplöses sedan i natriumhydroxid. Dessa föreningar upplever en neutraliseringsreaktion som producerar natrium och vattenbensoat.
C6H5COOH +NAOH => C6H5Sökväg +h2ANTINGEN
Reaktionen kan också utföras med natriumkarbonat, även om dess prestanda kan vara mindre än önskat.
Ansökningar
I mat
Natriumbensoat är ett livsmedelskonserveringsmedel som kan hämma eller försena processen för jäsning, försurning eller någon process som ger en försämring av dem. Dessutom har natriumbensoat en fungicidåtgärd.
Detta salt kan eliminera jäst, bakterier och svampar närvarande i mat. Dess konserveringsmedel är effektivare för pH < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Natriumbensoat används också vid bevarande av kolsyrade och läsk, där kolsyra finns. Även i sylt, rik på citronsyra, och i allmänhet, i livsmedel med syror närvarande som upprättar ett surt medium.
Dessutom används det i fodret med en koncentration av natriumbensoat på 0,1 %. Den maximala mängden bensoesyra och natriumbensoat som används, eftersom kondomer i mat, inte överstiger 2.000 mg/kg mat.
Medicinsk vård
Akut hyperamonemi
Natriumfenylaceate och natriumbensoat används, i form av adjuvansbehandling, vid behandling av akut hyperamonemi och en tillhörande flusopati hos patienter med förändringar av ureycykeln.
Dessa föreningar klassificeras som föräldralösa läkemedel. Denna valör gäller läkemedel som inte är lönsamma ur den ekonomiska synvinkeln.
Schizofreni
Natriumbensoat har använts experimentellt vid behandling av schizofreni. Den centrala delen av undersökningen är rollen som hämningen av oxidasenzymer från D-aaminosyrorna, en aktivitet som natriumbensoatet möter behandlingen i behandlingen.
Arginosuccin sur
Natriumbensoat används vid behandling av arginosuccinsyra -syra, en ärftlig metabolisk störning som kan orsaka hos patienter en höjd i ammoniumkoncentration, som kan påverka det centrala nervsystemet.
Kan tjäna dig: Benzyic Acid: Syntes, Transposition and UseInhibitor
-Det är en hämmare av araquidonato-enzymet 15-lipoxigenasa, ett enzym som undersöks av läkemedelsindustrin för att vara involverad i koronaryopatier.
-Hämmar verkan av trihacilglyceridlipasenzymet, ett enzym som verkar som producerar frisättningen av glycerol och fettsyror i tunntarmen, vilket möjliggör absorption av dessa lipider närvarande i mat.
Kanske möjligt användningen av natriumbensoat för att reglera tarmsabsorptionen av lipider såsom triacylglycerider.
Ärftliga störningar
Natriumbensoat används vid behandling av flera ärftliga störningar, relaterade till metabolismen av aminosyror, bland vilka citeras: behandling av hyperarginememi, och behandlingen av bristen på translokasenzymet av ornitin.
Andra
-Det används i alkoholhaltiga sköljningar och i silverpolisen. Dessutom används det vid utarbetandet av pyrotekniska föreningar, som är ansvarig för visselpipan som produceras när de är upplysta.
-Det används som antikorrosiv, vilket är en av de viktigaste kraven i produktionen av detta salt. Det används också i köldmedier, frostskyddsmedel och andra vattenbaserade system.
-I formuleringen av plast som polypropen används den för att förbättra dess motstånd och tydlighet.
-Det fungerar som en stabilisator i badrum och fotografiska processer.
Risker
Natriumbensoat klassificeras av FDA som "generellt säkert", i en dos av 0,1 % av matens vikt. Det anses inte vara irriterande att kontakt med hud och ögon, så det kan sägas att akut toxicitet är låg.
Natriumbensoat kan emellertid producera icke -immunologiska reaktioner (pseudoallergia) genom kontakt. Denna effekt är sällsynt hos normala människor, men hos patienter med episoder av ofta urtikarier eller astmasymtom kan det vara en ökning av frekvensen av dessa symtom.
I studier som utfördes hos råttor och möss hittades inga indikationer på en cancerframkallande verkan av natriumbensoat.
Besväret med dess användning i närvaro av askorbinsyra, som kan ge bensen; Toxisk förening, indikerad som cancerframkallande.
Referenser
- Nettoindustri. (2019). Natriumbensoatproduktion. Återhämtat sig från: vetenskap.skrov.org
- Wikipedia. (2019). Natriumbensoat. Hämtad från: i.Wikipedia.org
- Pub. (2019). Natriumbensoat. Återhämtat sig från: pubchem.Ncbi.Nim.Nih.Gov
- Hanes t. (2019). Fakta på natriumbensoat. Livlig. Återhämtat sig från: livestrong.com
- Kemisk bok. (2017). Natriumbensoat. Återhämtat sig från: Chemicalbook.com
- Spår H. och kål. (2013) Jama Psichiatry. 70 (12): 1267 - 1275.
- Världshälsoorganisationen Genève. (12 april 2005). Bensoesyra och natriumbensoat. [Pdf]. Återhämtat sig från: vem.int
- « Malojillo -fördelar, näringsdata, kontraindikationer
- De 16 farligaste läkemedlen och deras effekter »

