Natriumcitrat (C6H5O7NA3) Struktur, användningar, egenskaper
- 2598
- 425
- Prof. Erik Johansson
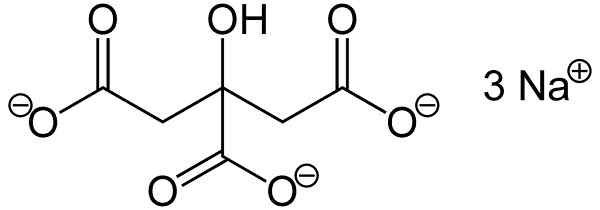
han natriumcitrat Det är natriumsaltet av citronsyra. Den bildas av en anjoncitrat c6H5ANTINGEN73- och tre natrium Na -katjoner+. Dess molekylformel är c6H5ANTINGEN7Na3 eller i sin utökade form: Naooc-ch2-C (agone) (OH) -CH2-Väg. Natriumcitrat är den konjugerade basen för citronsyra, det vill säga det senare erhålls från det senare genom att ersätta varje proton h+ av -cooh för en natriumnod+.
Det kan framställas i anhydra (utan vatten i dess sammansättning) eller i dess hydratiserade form med 2 eller 5 vattenmolekyler. Det är en förening som när vattenfri (utan vatten) tenderar att absorbera vatten från miljön.
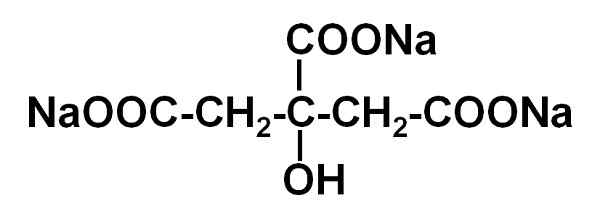 Trisodiumcitratmolekyl. Författare: Marilú Stea.
Trisodiumcitratmolekyl. Författare: Marilú Stea. Natriumcitrat fungerar som en buffert, detta innebär att pH stabiliseras, vilket är ett mått på surhet eller basicitet i en vattenlösning. Det har också egenskapen att bilda en stabil förening med CA -kalciumjoner2+, Kalciumcitrat.
Det används till exempel i livsmedelsindustrin för att undvika att komjölk bildar klumpar svåra att smälta av spädbarn.
I bioanalyslaboratorier används det för att undvika att koagulera blodet som patienter utvinns för vissa tester. Det förhindrar också att det koaguerar blodet som används vid transfusioner. Det används ofta i fosfatfria tvättmedel eftersom det inte är förorenande.
[TOC]
Strukturera
Trisodio citrat består av tre natrium Na -joner+ och en citratjon.
Citratjonen består av en kedja av tre kolatomer till vilka 3 karboxylater är förenade- (en för varje kolatom) och en hydroxyl -OH i det centrala kolet.
Var och en av de 3 Najonerna+ är kopplad till en grupp -coo-.
 Trisodiumcitratstruktur. Jü [allmän domän]. Källa: Wikimedia Commons.
Trisodiumcitratstruktur. Jü [allmän domän]. Källa: Wikimedia Commons. Nomenklatur
- Natriumcitrat
- Trisodiocitrat
- 2-hydroxipan-1,2,3-tricarboxylate trisodium
Egenskaper
Fysiskt tillstånd
Vit eller färglöst kristallint fast ämne.
Molekylvikt
258,07 g/mol
Smältpunkt
300 ºC
Löslighet
Det är mycket lösligt i vatten: 42,5 g/100 ml vid 25 ºC. Det är praktiskt taget olösligt i alkohol.
pH
En vattenlösning på 5% natriumcitrat har ett pH mellan 7,5 och 9,0, det vill säga det är något alkaliskt.
Kemiska egenskaper
Natriumcitrat är en buffert, vilket innebär att stabiliserar pH, vilket är ett mått på surhet eller alkalinitet hos en vattenlösning. Citrat Vid stabilisering av pH tillåter inte lösningen försuras eller alkaliseras över vissa värden.
Kan tjäna dig: kärnelektronisk konfiguration: konstruktion, exempelNär det finns överskott av protoner h+ Jag tar dem för att konvertera sina grupper -coo- I grupper -oH. Vice versa, om det finns många OH -grupper- ger protonerna i deras grupper -Coh och gör dem -coo-.
När den transformeras av kroppen ger den 3 HCO -molekyler3- För varje citratmolekyl.
Andra egenskaper
Hans kristaller är läckra, det vill säga de absorberar luft från luften. Dihydratiserat natriumcitrat är mer stabilt i luften.
Om dihydratet värms upp, när det når 150 ºC blir det vattenfritt (utan vatten).
Som citronsyra har natriumcitrat sur smak.
Erhållande
Natriumcitrat erhålls vanligtvis genom att tillsätta natriumkarbonat till en citronsyralösning tills effekten upphör. Efervescens beror på frigöring av koldioxid2:
Na2Co3 + Citronsyra → natriumcitrat + co2↑
Sedan förångas lösningen för att kristallisera produkten.
Det kan också framställas genom att behandla en natriumsulfatlösning med kalciumcitrat:
Na2Sw4 + Kalciumcitrat → Natriumcitrat + fodral4↓
Lösningen filtreras för att ta bort fallet4 Fast som har fällts ut. Då koncentreras lösningen och kristalliserar således natriumcitrat.
Plats i naturen
Natriumcitrat är den konjugerade basen för citronsyra, som är en naturlig förening som finns i alla levande organismer eftersom det är en del av dess metabolism, som är mekanismen för att utveckla energi i celler.
Ansökningar
I livsmedelsindustrin
Natriumcitrat har olika användningsområden inom livsmedelsindustrin, till exempel som en regulator för surhet, kidnappning, stabilisator, ytaktivt medel eller emulgator.
Det används i drycker, frysta desserter och speciella ostar, bland andra produkter.
Det gör det möjligt att undvika koagulering av mjölken, så den tillsätts till kymjölken som används för utfodring av spädbarn. På detta sätt skapas inga coagles eller hårda -till -digest -lockar av de små magen.
 Du kan lägga till natriumcitrat till mjölk så att klumpar inte bildas i magen. Författare: Couleur. Källa: Pixabay.
Du kan lägga till natriumcitrat till mjölk så att klumpar inte bildas i magen. Författare: Couleur. Källa: Pixabay. Det används för att påskynda färgfixering i fläskkött eller botade vacciner, det vill säga behandlat kött för att undvika dess sönderdelning. Upp till 50% askorbinsyra ersätts i dessa.
Kan tjäna dig: kiselsyra Fläskt botat kött som antagligen innehåller natriumcitrat. Författare: Ben Kerckx. Källa: Pixabay.
Fläskt botat kött som antagligen innehåller natriumcitrat. Författare: Ben Kerckx. Källa: Pixabay. Det tjänar också till att förhindra blodkoagulation i färskt vaccinkött (som biffar).
Inom medicin
Det används som ett alkaliserande medel, eftersom neutraliserar överskottssyra i blod och urin. Det indikeras att behandla metabolisk acidos som uppstår när kroppen producerar för mycket sur.
När citratjonen intas blir det en bikarbonatjon som är ett systemiskt alkaliserande medel (det vill säga hela kroppen) och som en följd av jonerna heutraliserar+, Ökar blodets pH och återgår eller eliminerar acidos.
Natriumcitrat fungerar som ett neutraliserande medel för obehag i magen.
Det används som släckta och svett. Det har diuretiska handlingar. Öka urinens kalciumutsöndring, som används vid hyperkalcemi, vilket är när det finns överskott av kalcium i blodet.
Det tjänar också till att underlätta eliminering av bly när förgiftning med denna metall inträffar.
Om överskott administreras kan alkalos produceras, muskelspasmer förfaller.
Natriumcitrat används i transfusioner. Det läggs till blodet tillsammans med dextros för att undvika dess koagulering.
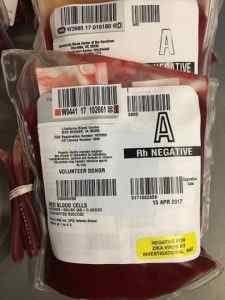 Lagrat blod för transfusioner. Innehåller förmodligen natriumcitrat. Författare: Kshirl02. Källa: Pixabay.
Lagrat blod för transfusioner. Innehåller förmodligen natriumcitrat. Författare: Kshirl02. Källa: Pixabay. Normalt metaboliserar levern snabbt citrat som erhålls i transfusionen, men under transfusioner av stora mängder kan leverkapaciteten överskridas.
I sådana fall eftersom citrat bildar ett komplex med kalcium är det en minskning av CA -kalciumjonen2+ i blodet. Detta kan generera bedövning, skakningar, stickningar, etc. Därför måste transfusioner genomföras långsamt.
I läkemedelsindustrin
Bland många andra användningsområden används för att förhindra mörkare mediciner där det finns järn och tanniner.
I blodanalys
Det används som ett antikoagulant i blodsamlingen eller när det ska lagras, eftersom det fungerar som en kalciumjonkorg CA2+, det vill säga det binder till kalciumjoner som bildar kalciumcitrat som inte är joniserad.
Kan tjäna dig: jonisk länk: egenskaper, hur den bildas och exempelDet används i koagulationstester och för att bestämma sedimentationshastigheten för röda blodkroppar.
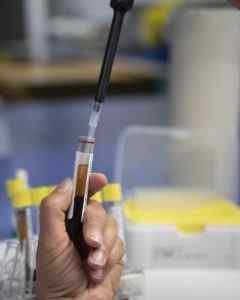 Blodprov. Författare: Bokskopet. Källa: Pixabay.
Blodprov. Författare: Bokskopet. Källa: Pixabay. Det används som ett antikoagulant under plasmaferes, procedur för att extrahera från blodöverskott som är skadliga för kroppen.
I nanopartikelsyntes
Det används som en stabilisator i syntesen av guld -nanopartiklar. Trisodio Citrate Dihydratiserad till kloroahinsyra tillsätts och bildar en rött vinupphängning.
Natriumcitrat fungerar som ett reducerande medel och som ett antiregionsmedel, som det är adsorberat på nanopartiklar.
På grund av den negativa citratbelastningen avvisar partiklarna varandra med varandra och undviker och bildar en stabil spridning. Ju högre den minsta citratkoncentrationen är partiklarna.
Dessa nanopartiklar tjänar till att förbereda medicinska biosensorer.
I miljövänliga tvättmedel
Natriumcitrat används allmänt i fosfatfria vätskefatorer. Detta beror på att dess miljöbeteende är ofarligt eftersom det är en metabolit som finns i alla levande organismer.
Det är lätt biologiskt nedbrytbart och svagt giftigt för vattenlevande liv. Av denna anledning anses det att det är ett rengöringsmedel med ekologiskt gynnsamma egenskaper.
För att förbättra exploateringen av bituminösa sand
Bituminösa sand är sandiga formationer rika på bitumen eller tjära, ett material som liknar olja.
Natriumcitrat har testats framgångsrikt tillsammans med NaOH -natriumhydroxid för att extrahera olja från bituminös sand.
Man tror att när citratet med sandstenen, jonerna -coo- av citrat bildar ett stort antal negativa belastningar på kiseldioxidpartiklar. Detta ger en bättre separering av sanden från bitumen genom den enkla avvisningen av de negativa belastningarna av grus av de negativa belastningarna av bitumen.
I andra applikationer
Det används i fotografering, för att ta bort spårmetaller, i elektrodeposition och för att ta bort SO2 av restgaser.
Referenser
- ELLER.S. National Library of Medicine. (2019). Natriumcitrat. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov.
- McNamara, c. (2017). Insamling och hantering av blod. I Dacie och Lewis praktiska hematologi (tolfte upplagan). Återhämtat sig från Scientedirect.com.
- Steber, J. (2007). Ekotoxiciteten hos rengöring av produktingredienser. I handbok för rengöring/dekontaminering av ytor. Återhämtat sig från Scientedirect.com.
- Xiang, b. et al. (2019). Studie av natriumcitratens roll i Bitumen -befrielse. Energy Fuels 2019, 33, 8271-8278. Återhämtat sig från pubar.ACS.org.
- Hedle, n. och Webert, K.OCH. (2007). Medicinsk transfusion. Inom blodbank och transfusionsmedicin (andra upplagan). Återhämtat sig från Scientedirect.com.
- Sudhakar, s. och Santhosh, s.B. (2017). Guld -nanomaterial. I framsteg i biomembran och lipid själv-ambulant. Återhämtat sig från Scientedirect.com.
- Elsevier (redaktion) (2018). Kapitel 8. Nanometal. I fonder och tillämpningar av Nano -kisel i plasmonik och fulliner. Aktuella och framtida trender mikro- och nanoteknologier. Sidorna 169-203. Återhämtat sig från Scientedirect.com.

