Kromklorid (CRCL3) struktur, egenskaper, användningar

- 5064
- 294
- Hans Olsson
han Kromklorid (CRCL3) Det är ett oorganiskt salt bestående av CR -katjoner3+ och CL -anjoner- i en 1: 3 -proportion; det vill säga för varje cr3+ Det finns tre cl-. Som kommer att ses senare är deras interaktioner inte joniska. Detta salt kan förekomma i två former: anhydra och hexahydrat.
Den vattenfria formen kännetecknas av att presentera en violetta-Reddisk färg; Medan hexahydrat, CRCL3.6h2Eller det är mörkgrönt. Införlivandet av vattenmolekyler modifierar de fysiska egenskaperna hos dessa kristaller; Som kokande och fusionspunkter, tätheter etc.
 Violet-flodkristaller av kromklorid (iii) vattenfri. Källa: Ben Mills [Public Domain]
Violet-flodkristaller av kromklorid (iii) vattenfri. Källa: Ben Mills [Public Domain] Chrome -klorid (III) (enligt beståndet nomenklaturen) sönderdelas vid höga temperaturer och blir kromklorid (II), CRCL2. Det är frätande för metaller, även om det används i krom: proceduren där metaller är täckta med ett tunt kromskikt.
Cr3+, Kommer från respektive klorid har den använts vid behandling av diabetes, särskilt hos patienter med total parenteral näring (TPN), som inte intar mängden krom som krävs. Resultaten är dock mycket bättre (och mer pålitliga) om det levereras som en picolinato.
[TOC]
Kromkloridstruktur
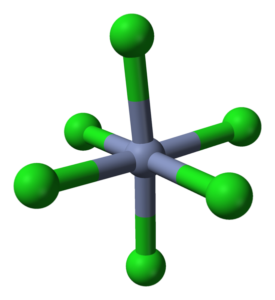 Octaedro -samordning för CRCL3 i dess kristaller. Källa: Ben Mills [Public Domain]
Octaedro -samordning för CRCL3 i dess kristaller. Källa: Ben Mills [Public Domain] Crcl3 Trots att det är ett salt är deras interaktioner inte rent joniska; De har en viss kovalent karaktär, produkt från samordningen mellan CR3+ och cl-, som ger upphov till en deformerad octahedron (överlägsen bild). Kromet ligger i mitten av Octaedro och klorerna vid dess vertikaler.
Octahedron CRCL6 Du kan vid första anblicken motsäga CRCL -formeln3; Denna kompletta oktaedron definierar emellertid inte enhetens enhetscell, utan en kub (även deformerad), som skär de gröna sfärerna eller kloranjonerna i hälften.
Kan tjäna dig: 20 exempel på kemisk sublimering och egenskaperKristallina vattendrag
Således fortsätter den enhetliga cellen med denna octaedro att upprätthålla andelen 1: 3. Återge dessa deformerade kuber i rymden, CRCL -kristallen erhålls3, som representeras i den överlägsna bilden med en tre -dimensionell fyllningsmodell och en modell av sfärer och barer.
 CRCL3 Crystal Structure Layer representerat med en trefimensionell sfär och staplar Model. Källa: Ben Mills [Public Domain]
CRCL3 Crystal Structure Layer representerat med en trefimensionell sfär och staplar Model. Källa: Ben Mills [Public Domain] Detta kristallina skikt är ett av de många som gör3 (Förväxla inte glasets färg, sant, med de gröna sfärerna).
Som man kan se, CL -anjonerna- De upptar ytan, så deras negativa belastningar avvisar de andra kristallina skikten. Följaktligen blir kristallerna bedrägerier och bräckliga; Men lysande, på grund av Chrome.
Om samma lager visualiseras ur ett lateralt perspektiv kommer det att observeras, istället för oktaedra, förvrängda tetraedrar:
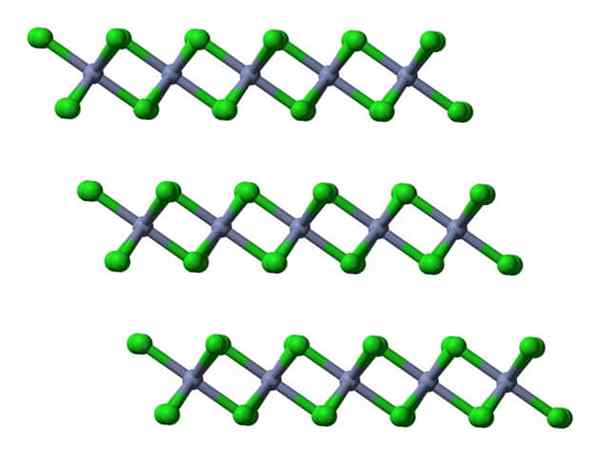 Crcl3 kristallina lager vyer i sidled. Källa: Ben Mills.
Crcl3 kristallina lager vyer i sidled. Källa: Ben Mills. Här underlättas förståelsen för varför skikten avvisas med varandra när CL- av dess ytor.
Egenskaper
Namn
-Kromklorid (III)
-Chrome Trichloride (III)
-Kromklorid (iii) vattenfri.
Kemisk formel
-Crcl3 (vattenfri).
-Crcl3.6h2O (hexahing).
Molekylvikt
-158,36 g/mol (vattenfri).
-266,43 g/mol (hexahydrat).
Fysisk beskrivning
-Solid och violet-redistiska kristaller (vattenfri).
-Mörkgrönt kristallint damm (hexahydrat, lägre bild). I detta hydrat kan det ses som vatten hämmar ljusstyrka, metallkromfunktion.
 Hexahydrat krom krom. Källa: Användare: Walkerma [Public Domain]
Hexahydrat krom krom. Källa: Användare: Walkerma [Public Domain] Smältpunkt
-1.152 ºC (2.106 ºF, 1.425 K) (ANHYDRUM)
-83 ºC (hexahydrat).
Kokpunkt
1300 ºC (2.370 ºF, 1.570) (ANHYDRUM).
Vattenlöslighet
 Vattenlösningar av kromklorid (III). Källa: Leiem [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]
Vattenlösningar av kromklorid (III). Källa: Leiem [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)] -Något lösligt (anhydro).
-585 g/l (hexahydrat).
I den övre bilden visas en serie provrör fyllda med en vattenlösning av CRCL3. Observera att ju mer koncentrerad, desto mer intensiv färgen på komplexet [cr (oh2)6]3+, Grön färgansvarig.
Kan tjäna dig: Putrescina: Struktur, egenskaper, syntes, användningLöslighet i organiska lösningsmedel
Löslig i etanol, men olöslig i eter (vattenfri).
Densitet
-2,87 gr/cm3 (vattenfri).
-2,76 g/cm3 (Hexahydrat).
Förvaringstemperatur
Sönderfall
När de värms upp till sönderdelning avger kromklorid (III) giftiga ångor av föreningar som innehåller klor. Dessa föreningar frigörs också när kromklorid (III) kommer i kontakt med starka syror.
Korrosion
Det är mycket frätande och kan attackera vissa stål.
Reaktioner
Det är oförenligt med starka oxidanter. Det reagerar också starkt med litium och kväve.
När den värms upp i närvaro av väte reduceras den till kromklorid (II), med bildning av väteklorid.
2 CRCL3 + H2 => 2 CRCL2 + 2 hcl
pH
I en vattenlösning och med en koncentration av 0,2 M: 2,4.
Syntes
Kromklorid (iii) hexahydrat produceras, vilket reagerar kromhydroxid med saltsyra och vatten.
Cr (oh)3 + 3 hcl +3 h2O => crcl3.6h2ANTINGEN
För att få anhydra salt värms CRCL3.6h2Eller i närvaro av tionilo -klorid, SoCl2, Saltsyra och värme:
[Cr (h2ANTINGEN)6] Cl3 + 6socl2 + ∆ → CRCL3 + 12 hcl + 6so2
Alternativt CRCL3 Klorgas erhålls på en blandning av krom och koloxid.
Cr2ANTINGEN3 + 3 c +cl2 => 2 CRCL3 + 3 Co
Och slutligen, som den mest använda metoden, är det att värma sin oxid med ett halogenantmedel, såsom koltetraklorid:
Cr2ANTINGEN3 + 3CCL4 + ∆ → 2cl3 + 3COCL2
Ansökningar
Industriister
Kromklorid ingriper i på -platsens framställning av kromklorid (II); reagens som ingriper i reduktionen av alkylhalider och i syntesen av haluro från (e) -salquenilo.
Kan tjäna dig: natriumoxalat (Na2C2O4): struktur, egenskaper, användningar, risker-Det används i den kromade tekniken. Detta består av deponering, genom galvanoplastik, ett fint skikt av krom på metallföremål eller annat material med ett dekorativt mål, vilket ökar korrosionsmotståndet och även ythårdhet.
-Det används som en textilmordant och fungerar som en länk mellan färgningsmaterialet och tygerna som ska färgas. Dessutom används den som en katalysator för produktion av olefiner och vattentätande medel.
Terapeutik
Användningen av UP -kromkloridtillskott rekommenderas hos patienter som endast får intravenösa lösningar, administrerade för Total Parenteral Nutrition (TPN). Därför, bara när dessa patienter inte får alla sina näringskrav.
Krom (iii) är en del av glukostoleransfaktorn, en aktivator av de reaktioner som främjas av insulin. Man tror att krom (iii) aktiverar metabolismen av glukos, proteiner och lipider, vilket underlättar insulinets verkan hos människor och djur.
Krom finns i många livsmedel. Men dess koncentration överstiger inte 2 genom ration, varvid broccolin är maten med det största bidraget (11 μg). Dessutom är tarmsabsorptionen av krom låg, med ett värde av 0,4 till 2,5% av det intagna beloppet.
Detta gör det svårt att skapa en diet för kromförsörjning. 1989 rekommenderade National Academy of Sciences mellan 50 och 200 μg/dag som ett adekvat kromintag.
Risker
Bland de möjliga riskerna för konsumtionen av detta salt som ett kromtillskott är:
-Starka magsmärtor.
-Onormal blödning, som kan variera från svårigheter att läka ett sår, röda faraste blåmärken eller mörkare av fekalpallprodukten av inre blödningar.
-Irritationer i matsmältningssystemet, orsakar magsår eller tarmar.
-Dermatit
Referenser
- Shiver & Atkins. (2008). Oorganisk kemi. (Fjärde upplagan). MC Graw Hill.
- Wikipedia. (2019). Krom (iii) klorid. Hämtad från: i.Wikipedia.org
- Krom (iii) klorid [PDF]. Återhämtat sig från: alfa.Kem.Umg.Edu
- Pub. (2019). Kromklorid hexahydrat. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- National Institute of Health. (21 september 2018). Krom: faktablad för kosttillskott. Hämtad från: SDG.Va.Nih.Gov
- Tomlinson Carole a. (2019). Kromkloridbiverkningar. Leaf Group Ltd. Återhämtat sig från: hälsosamt.com
- « Varför är det viktigt att läsa? 10 fördelar med läsning
- Boraxhistoria, struktur, egenskaper, användningar, syntes, risker »

