Difenylamin
- 835
- 231
- Prof. Erik Johansson
Vad är förvaren?
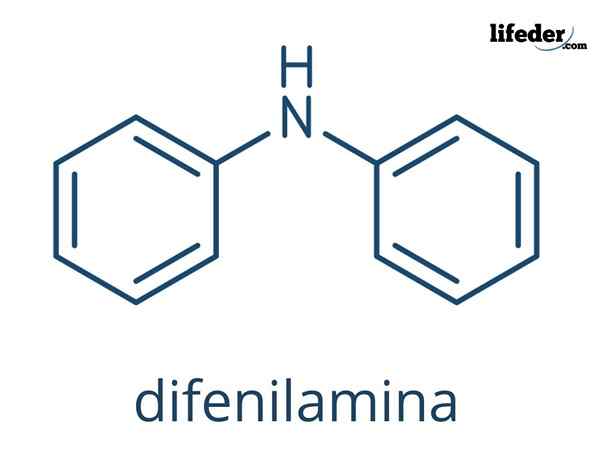
De Difenylamin Det är en organisk förening vars kemiska formel är (c6H5)2Nh. Namnet indikerar att det är en amin, liksom dess formel (-NH2). Å andra sidan avser termen "diffenil" närvaron av två aromatiska ringar kopplade till kväve. Följaktligen är defilamin en aromatisk amin.
Inom världen av organiska föreningar är det aromatiska ordet inte nödvändigtvis relaterat till förekomsten av dess lukt, utan till egenskaper som definierar deras kemiska beteenden mot vissa arter.
När det gäller difenylamin sammanfaller dess aromatisitet och det faktum att deras solida utgör en distinkt arom. Emellertid kan grunden eller mekanismerna som styr dess kemiska reaktioner förklaras av dess aromatiska karaktär, men inte på grund av dess trevliga arom.
Dess kemiska struktur, basicitet, aromatisitet och intermolekylära interaktioner är variablerna som är ansvariga för dess egenskaper: från färgen på dess kristaller till dess användbarhet som antioxidantmedel.
Kemisk struktur av förvar

I de överlägsna bilderna representeras de kemiska strukturerna i diffenilamin. De svarta sfärerna motsvarar kolatomer, vita till väteatomer och blått till kväveatomen.
Skillnaden mellan båda bilderna är modellen för hur de representerar molekylen grafiskt. I den lägre belyser den aromatiken på ringarna med linjerna prickade i svart och även den platta geometrien för dessa ringar bevisas.
Ingen av de två bilderna visar det ensamma elektronparet som inte delas på kväveatomen. Dessa elektroner "går" genom det konjugerade π -systemet för dubbelbindningarna i ringarna. Detta system bildar ett slags cirkulerande moln som möjliggör intermolekylära interaktioner; det vill säga med andra ringar från en annan molekyl.
Det kan tjäna dig: Laboratorietermometer: Egenskaper, vad är det för, användning, exempelOvanstående innebär att det icke -delade kväve vridmomentet går genom båda ringarna, distribuerar i dessa sin elektroniska densitet och sedan återvänder de till kväve för att upprepa cykeln igen.
I denna process minskar tillgängligheten av dessa elektroner, vilket resulterar i en minskning av basiciteten för dipelamin (dess tendens att donera elektroner som en Lewis -bas).
Dipenylaminanvändningar/applikationer
Diphenylamin är ett oxidationsmedel som kan uppfylla en serie funktioner, och bland dem är följande:
- Under deras förvaring upplever äpplen och päron en fysiologisk process som kallas skosse. Dipenylaminverkan gör det möjligt att öka lagringsperioden, vilket minskar fruktskador på 10 % av vad som observeras i deras frånvaro.
- När man bekämpar oxidation utvidgar difenylamin och dess derivat funktionen av motorer genom att undvika förtjockning av begagnad olja.
- Difenylamin används för att begränsa ozonverkan i gummitillverkning.
- Diphenylamin används i analytisk kemi för nitratdetektering (nej3-), Klorater (CLO3-) och andra oxiderande medel.
- Det är en indikator som används i nitratförgiftningstest.
- När RNA är hydrolyserad i en timme, reagerar det med defilamin; Detta tillåter dess kvantifiering.
- I veterinärmedicin används dipe -pilamin topiskt i förebyggande och behandling av manifestationerna av boreridmasken hos uppfödningsdjur.
- Några av duuelaminderivaten tillhör kategorin icke-steroida antiinflammatoriska läkemedel. De kan också ha farmakologiska och terapeutiska effekter såsom antimikrobiella, smärtstillande medel, antikonvulsiva medel och anti -canceraktivitet.
Dipenylaminberedning
Naturligtvis produceras defilamin i löken, i koriantros, i bladen av grönt och svart te och i skalens frukter. Syntetiskt sett finns det många rutter som leder till denna förening, till exempel:
Termisk deamination av anilin
Den är beredd genom termisk deaminering av anilin (c6H5Nh2) I närvaro av oxiderande katalysatorer.
Om anilin i denna reaktion inte innehåller en syreatom till dess struktur, varför oxiderar du? Eftersom den aromatiska ringen är en elektronattraktorgrupp, till skillnad från H -atomen, som donerar sin låga elektroniska kvävetäthet i molekylen.
2 c6H5Nh2 => (C5H5)2 NH+NH3
Anilin kan också reagera med anilinhydrokloridsalt (C6H5Nh3+Kli-) under en uppvärmning av 230 ºC i tjugo timmar.
C6H5Nh2 + C6H5Nh3+Kli- => (C5H5)2 Nh
Fenotiazinreaktion
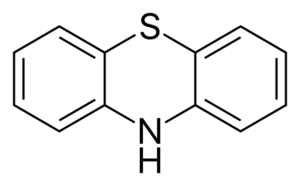
Dipenylamin har sitt ursprung i flera härledda i kombination med olika reagens. En av dessa är fenotiazin, som syntetiserar med svavel är en föregångare till derivat med farmaceutisk verkan.
(C6H5)2Nh +2s => s (c6H4) NH +H2S

Dipenylaminegenskaper
Dipenylamin är ett vitt kristallint fast ämne som, beroende på dess föroreningar, kan förvärva bronkneal, bärnsten eller gula toner. Den har en trevlig blommaarom, den har en molekylvikt 169,23 g/mol och en densitet av 1,2 g/ml.
Molekylerna i dessa fasta ämnen interagerar av van der Waals-krafter, bland vilka är vätebroar som bildas av kväveatomer (NH-NH) och stapling av aromatiska ringar, vilar sina "elektroniska moln" på andra sidan.
Kan tjäna dig: Zink Sulfide (ZnS)Som aromatiska ringar upptar mycket. Ovanstående får det fasta ämnet att inte ha en mycket hög fusionspunkt (53 ºC).
I flytande tillstånd är emellertid molekylerna mer separata och effektiviteten hos vätebroar förbättras. Likaså är defilamin relativt tung och behöver mycket värme för att flytta till en gasfas (302 ºC, dess kokpunkt). Detta beror också delvis på vikten och interaktioner mellan de aromatiska ringarna.
Löslighet och basicitet
Det är mycket olösligt i vatten (0,03 g/100 g vatten) på grund av den hydrofoba karaktären hos dess aromatiska ringar. Istället är det mycket lösligt i organiska lösningsmedel som bensen, koltetraklorid (CCL4), aceton, etanol, pyridin, ättiksyra, etc.
Dess surhetskonstant (PKA) är 0,79, vilket hänvisar till surheten i dess konjugerade syra (C6H5Nh3+). Protonen som läggs till kväve har en tendens att dela, eftersom paret av elektroner som den är kopplad kan gå genom de aromatiska ringarna. Således hög instabilitet c6H5Nh3+ Det återspeglar den låga basiciteten i diffenilamin.
Referenser
- Lubrizol Corporation. (2018). Difenylaminantioxidanter. Återhämtat sig från lubrizol.com
- Arun Kumar Mishra, Arvind Kumar. (2017). Farmakologiska tillämpningar av difenylamin och dess derivat som potent bioaktiv förening: en översyn. Aktuella bioaktiva föreningar, volym 13.
- Förskolning. (2015-2016). Beredning av difenylamin. Återhämtat sig från prepchem.com
- Pub. (2018). Difenylamin. Återhämtat sig från pubchem.Ncbi.Nlm.Nih.Gov.
- Wikipedia. (2018). Difenylamin. Hämtas från.Wikipedia.org

