Dimetylamin ((CH3) 2NH) struktur, egenskaper, användningar, risker
- 2809
- 350
- Johan Johansson
De dimetylamin Det är en organisk förening som bildas av två metylgrupper -ch3 Förenad till en -NH -grupp. Dess kemiska formel är (Cho3)2Nh. Det är en färglös gas. När en lukt av fisk uppfattas i luften i låga koncentrationer. Men om det är i hög koncentration har den en lukt av ammoniak NH3.
Dimetylamin finns i växter och djur. Det tros att hos människan kommer från nedbrytningen av vissa enzymer men också från intag av vissa livsmedel som fisk. Om dimetylamingas upplöses i vatten, bildar den mycket alkaliska och frätande lösningar.
 Dimetylamin. Ring0 [allmän domän]. Källa: Wikimedia Commons.
Dimetylamin. Ring0 [allmän domän]. Källa: Wikimedia Commons. Den har olika industriella användningsområden, så att de producerar lösningsmedel för att påskynda vulkaniseringen av gummi.
Dimetilamin är en mycket brandfarlig gas. Behållarna som innehåller den bör inte utsättas för värme eller eld eftersom de kan utnyttja. Dessutom är deras ångor irriterande ögon, hud och luftvägar.
Det är en förening som kan vara en del av atmosfäriska aerosoler, det vill säga av mycket tunna droppar som finns i atmosfären.
[TOC]
Strukturera
Dimetilamin är en sekundär alifatisk amin. Detta innebär att kvävesubstituenter (n) är alifatiska (-ch3), vilket innebär att de inte är aromatiska och att de är två. Därför finns det två metyl -ch3 United kväve, som också har ett väte (H).
I dimetylaminmolekylen har kväve (N) ett par fria elektroner, det vill säga ett par elektroner som inte är förenade med någon annan atom.
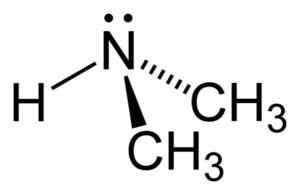 Dimetylamin. Författare: Benjah-Bmm27. Källa: Wikimedia Commons.
Dimetylamin. Författare: Benjah-Bmm27. Källa: Wikimedia Commons. Nomenklatur
- Dimetylamin
- N, N-dimetylamin
- N-metylmetanamin
- DMA (akronym för di-metyl-amin).
Egenskaper
Fysiskt tillstånd
Färglös gas.
Molekylvikt
45,08 g/mol
Smältpunkt
-93 ºC
Kokpunkt
7,3 ºC
Flampunkt
-6.69 ºC (stängd koppmetod).
Självriktningstemperatur
400 ° C
Kan tjäna dig: lag om flera proportionerDensitet
Vätska = 0,6804 g/cm3 A 0 ºC.
Ånga = 1,6 (relativ densitet med avseende på luft, luft = 1).
Löslighet
Mycket lösligt i vatten: 163 g/100 g vatten vid 40 ° C. Löslig i etanol och etyleter.
pH
Vattenhaltiga dimetylaminlösningar är starkt alkaliska.
Dissociationskonstant
Kb = 5,4 x 10-4
Pktill konjugerad syra = 10 732 till 25 ° C. Konjugatsyra är dimetylamoniumjonen: (Cho3) NH2+
Kemiska egenskaper
Flytande dimetylamin kan attackera vissa plast, däck och beläggningar.
Vid upplösning i vatten tar kväve -fria elektronparet (n) en proton (h+) vatten, lämnar en oh gratis-, Så det bildar mycket alkaliska och frätande lösningar:
Dimetylamin + vatten → dimetylamoniumjon + hydroxyljon
(Ch3)2NH + H2O → (Välj3)2Nh2+ + Åh-
Med salpetersyra erhålls ett nitratsalt, det vill säga dimetyla amotylamoniumnitrat:
Dimetylamin + salpetersyra → dimetylamoniumnitrat
(Ch3)2Nh +hno3 → (ch3)2Nh2+NEJ3-
Andra egenskaper
När det är i låg luftkoncentration har en lukt som liknar fisk, medan det i höga koncentrationer luktar som ammoniak (NH3).
Biokemiska reaktioner
I organismen kan dimetylamin drabbas av nitrillär under svagt sura förhållanden för att ge dimetylnitrosamin en cancerframkallande förening (CH3)2Nr.
Dimetlnitrosaminbildning sker från dimetylamin och nitrit (natriumnitrit) i magen (ett pH 5-6) genom verkan av bakterierna som finns i mag-tarmkanalen. Natriumnitrit finns i vissa livsmedel.
Dimetylamin + natriumnitrit → dimetylnitrosamin + natriumhydroxid
(Ch3)2Nh + nano2 → (ch3)2N-no + naoh
Erhållande
Dimetilamin framställs kommersiellt genom att reagera metanol (välj3OH) med ammoniak (NH3) vid 350-450 ° C i närvaro av en kiseldioxidkatalysator (SIO2/Till2ANTINGEN3).
2 ch3Oh + nh3 → (ch3)2NH + 2 H2ANTINGEN
Eftersom monometylamin och trimetylamin också produceras utförs en rening i en serie på fyra till fem destillationskolumner.
Närvaro
Dimetylamin finns i växter och djur. Det finns också naturligt och rikligt i mänsklig urin.
Det kan tjäna dig: epoxid: nomenklatur, erhållning, applikationer, exempelDet uppskattas att dess närvaro hos människor beror på att vissa typer av tarmbakterier produceras från vissa föreningar som finns i maten.
Några av dessa föreningar är kullen (förening som är associerad med vitamingruppen B) och trimetylaminoxid. Det tros också att det kommer från en enzymhämmare av kväveoxid (NO) som bildas i kroppen.
Vissa informationskällor indikerar att ökningen av dimetylamin i urinen orsakas av intag av fisk och frukt av havet, där huvudvärden erhålls när de äter bläckfisk, kullar, sardiner, svärdfisk, torsk, fisk och linje.
 Att äta fisk kan öka dimetylaminnivåerna i urin. Författare: Anna Sulencha. Källa: Pixabay.
Att äta fisk kan öka dimetylaminnivåerna i urin. Författare: Anna Sulencha. Källa: Pixabay. Patienter med överskott av dimetylamin
Det anses att dimetylamin är ett uremiskt toxin, det vill säga ett ämne som kan orsaka skador om dess koncentration i urin höjs. I själva verket har mycket höga nivåer av dimetylamin observerats hos patienter med njursjukdom vid terminalstadiet.
Det antas att hos dessa patienter kan det finnas överbefolkning av tarmbakterier som kan producera det.
Ansökningar
DMA eller DMA används för:
- Beredning av andra föreningar.
- Produktion av dimetylformamid och dimetylacetamidlösningsmedel.
- Påskynda vulkaniseringen av vissa tandkött.
- Eliminera hårhår under garvning.
- Agera som en antioxidant för lösningsmedel.
- Tjäna som en mineralflotationsmedel.
- Hämta korrosion och som ett anti -Sniff -medel.
- Funktion som ytaktivt medel.
- Göra tvålar och tvättmedel.
- Agera som kemist i textilier.
- Funktion som ett antidatingmedel i bränslen och som en gasstabilisator.
- Förbereda färgämnen.
- Absorbera syragaser.
- Tjäna som bekämpningsmedel och raketer.
- Vara en del av medel för vattenbehandling.
- Handla som en fungicid i jordbruksprodukter.
- Redan upphörande användningar som att attrahera och utrota gorgjos eller insekter som attackerar bomull.
 Bomullsväxt. Författare: Isaa KC. Källa: Pixabay.
Bomullsväxt. Författare: Isaa KC. Källa: Pixabay.  Tidigare eliminerades insekterna som attackerar bomullsväxter med dimetylamin. Marvinbikolano [CC BY-SA (https: // Creativecommons.Org/licenser/BY-SA/4.0)]. Källa: Wikimedia Commons.
Tidigare eliminerades insekterna som attackerar bomullsväxter med dimetylamin. Marvinbikolano [CC BY-SA (https: // Creativecommons.Org/licenser/BY-SA/4.0)]. Källa: Wikimedia Commons. Risker
Dimetilaminångor är irriterande hud, ögon och luftvägar.
Kan tjäna dig: oorganiska föreningarOm du kommer i kontakt med huden i flytande form kan orsaka frysning och kemisk brännskada. Dess inandning har negativa hälsoeffekter.
DMA -gas är frätande och kan bilda frätande vattenhaltiga lösningar. Dina vattenhaltiga lösningar kan bli brandfarliga om de inte är ganska utspädda.
Gasformad dimetylamin inflammeras lätt genom att producera toxiska ångor av kväveoxider (nejx).
Om behållaren som innehåller denna gas utsätts för intensiv värme eller värme kan den explodera.
DMA -påverkan i atmosfären
Atmosfärisk aerosol (mycket små droppar av blandning av naturliga föreningar och/eller föroreningar i atmosfären) har en djup inverkan på global klimat och luftkvalitet i de olika regionerna i världen.
Bildningen av nya aerosolpartiklar är ännu inte helt förstått.
Det uppskattas att dimetylamin deltar tillsammans med andra föreningar i bildningen av dessa partiklar, vilket verkar bero på området för starka DMA -utsläpp.
Till exempel i industriområden finns det större koncentration än i jordbruksområden, och detta kan påverka hur DMA deltar.
Det bör noteras att enligt vissa forskare kan förbränning av växtmaterial som innehåller glyfosat (en av de herbicider som används mest i världen) leda till dimetylaminbildning.
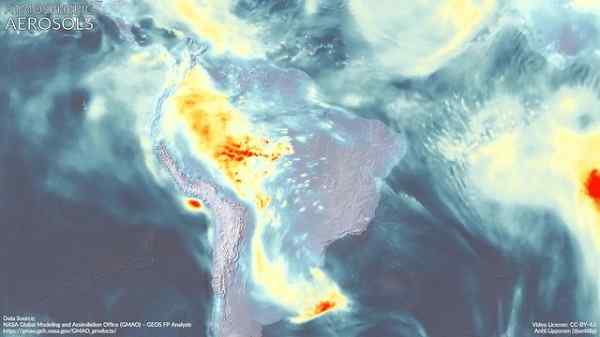 Atmosfäriska aerosoler i Sydamerika. Dimetilamin kan bidra till dess bildning. Marvinbikolano [CC BY-SA (https: // Creativecommons.Org/licenser/BY-SA/4.0)]. Källa: Wikimedia Commons.
Atmosfäriska aerosoler i Sydamerika. Dimetilamin kan bidra till dess bildning. Marvinbikolano [CC BY-SA (https: // Creativecommons.Org/licenser/BY-SA/4.0)]. Källa: Wikimedia Commons. Referenser
- ELLER.S. National Library of Medicine. (2019). Dimetylamin. Återhämtat sig från pubchem.Ncbi.Nlm.Nih.Gov.
- Kirk-THERMER (1994). Encyclopedia of Chemical Technology. Fjärde upplagan. John Wiley & Sons.
- Morrison, r.T. och Boyd, r.N. (2002). Organisk kemi. Sjätte upplagan. Prentice-hall.
- Windholz, m. et al. (redaktörer) (1983). Merck -indexet. En enyklopedi av kemikalier, droger och biologiska. Tionde upplagan. Merck & Co., Inkl.
- Abramowitz, m.K. et al. (2010). Uremiens patofysiologi. Alifatiska aminer. Vid kronisk njursjukdom, dialys och transplantation (tredje upplagan). Återhämtat sig från Scientedirect.com.
- Li, h. et al. (2019). Påverkan av atmosfäriska förhållanden på svavelsyra-dimetylamin-Ammoni-baserad ny partikelbildning. Chospher 2019; 245: 125554. NCBI återhämtade sig.Nlm.Nih.Gov.
- Mackie, J.C. och Kennedy, och.M. (2019). Pyrolys av glyfosat och låtar giftiga produkter. Miljö. Sci. Teknol. 2019: 53 (23): 13742-13747. NCBI återhämtade sig.Nlm.Nih.Gov.

