Hydroxylgrupp

- 2729
- 573
- Prof. Erik Johansson
Vi förklarar vad en hydroxylgrupp, dess egenskaper, struktur och flera exempel är
 Hydroxylgruppens kemiska struktur
Hydroxylgruppens kemiska struktur Vad är en hydroxylgrupp?
En Hydroxylgrupp Det är en funktionell grupp eller en del av andra funktionella grupper som finns i många organiska och oorganiska föreningar. Det bildas av en väteatom och en av syre (därmed dess namn).
Hydroxylgrupper är vanligtvis kopplade till en kolatom eller ett annat icke -metalliskt element såsom svavel eller fosfor, och är en av de viktigaste funktionella grupperna i organisk kemi.
Denna grupp atomer finns i organiska funktionella grupper såsom alkoholer, fenoler och karboxylsyror och är den som ger var och en av dessa funktionella grupper sina kemiska egenskaper egenskaper Karakteristiska egenskaper. I olika strukturer kan det representeras som -oh eller ho-
Egenskaper hos hydroxylgrupper
- Den består av en syreatom och en av väte kopplad till varandra och kopplas till en annan atom i en molekyl genom kovalenta bindningar.
- Kopplingen mellan väte och syreatom är en polär bindning där syre har en negativ partiell belastning och positiv partiell belastningsväte, vilket gör hydroxylgruppen till en polär funktionell grupp.
- Den har en struktur som liknar den för vatten. Av denna anledning är många av de föreningar som innehåller det vanligtvis lösliga i nämnda lösningsmedel.
- Den har ett väte som är direkt kopplat till syreatomen, så att hydroxylgruppen kan bilda en vätebindning där den deltar som en donatorvätegrupp.
- Med två fria elektroner på syreatomen kan hydroxylgruppen bilda ytterligare två vätebindningar som fungerar som en acceptor av väteatomer.
- Du kan fungera som en syra genom att ge en proton till en bas. Beroende på den funktionella gruppen som den är en del av och den atom som den är direkt kopplad, kan hydroxylgruppen visa olika surhetsnivåer. Till exempel, i alkoholer, har den en PKA på 15 eller mer (hård syra än vatten), i fenoler varierar det mellan 7 och 10 medan i karboxylsyror är det vanligtvis mellan 4 och 5.
- Du kan också fungera som en Lewis -bas och donera ett av dess elektronpar för att länka till en annan proton eller någon annan Lewis -syra.
Hydroxylgruppsstruktur
Som nämnts bland egenskaperna bildar syre- och väteatomer i hydroxylgruppen en polär kovalent bindning.
Dessutom bildar syreatomen en andra kovalent bindning med en annan atom som är en del av en molekyl som en alkohol, fenol till någon annan sammansättning. Lewis -strukturen i denna grupp presenteras nedan:
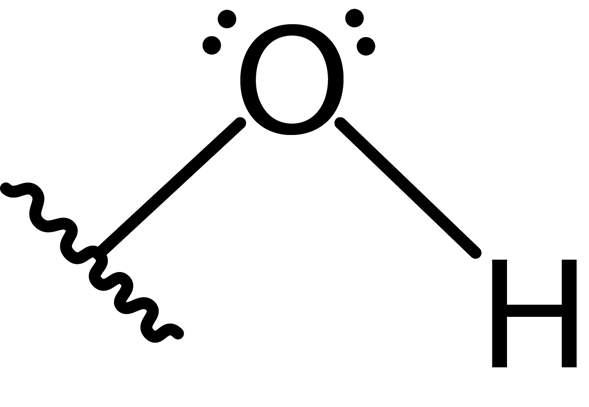
På grund av närvaron av de två paren av fria elektroner på syreatomen och de två kovalenta bindningarna har hydroxylgruppen vinkelgeometri med en vinkel på cirka 104 °, något lägre än den tetraedrala vinkeln. Längden på syre-hydrogenbindningen är cirka 0.97 Angstroms.
Hydroxylgrupp, hydroxylradikal och hydroxidjon
Det är mycket vanligt att förvirra hydroxylgruppen med hydroxylradikal och hydroxidanjon, eftersom alla bildas av samma två atomer, men dessa termer hänvisar inte till samma.
Å ena sidan skiljer sig hydroxylradikalen från hydroxylgruppen där den är en fri radikal med ett udda antal valenselektroner, och är inte heller kopplad till någon annan atom eller grupp atomer (varför det berättas gratis).
Trots dessa skillnader använder många felaktigt den hydroxylradikala termen för att hänvisa till hydroxylgruppen när de finns i en molekyl.
Hydroxidanjon är å andra sidan en jon med en negativ belastning bildad av väte och syre, medan hydroxylgruppen är en neutral grupp.
Även om hydroxylgruppen alltid är kopplad till en molekyl med hjälp av en kovalent bindning, har föreningar som innehåller hydroxidjoner jonbindning mellan detta och en del metall, såsom natrium, litium eller kalium.
Kan tjäna dig: vad är anoden och katoden?Hydroxylgruppsexempel
Alkohol
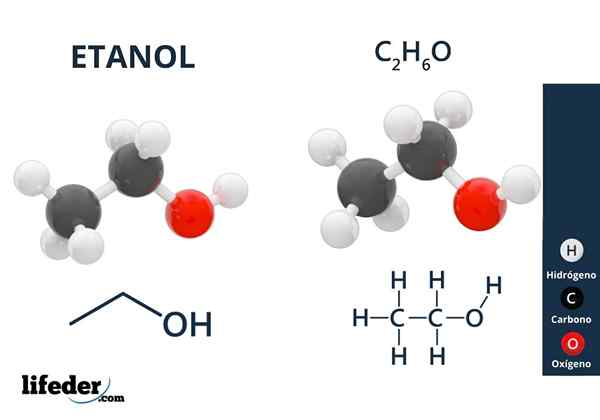 Etanol
Etanol Alkoholer har hydroxylgrupper kopplade till ett alifatiskt kol. Exempel på alkoholer är:
- Metylalkohol.
- Etanol.
- Isopropylalkohol.
Fenoler
Fenolerna kännetecknas av att ha en hydroxylgrupp direkt kopplad till en aromatisk ring. Några exempel på vanliga fenoler är:
- Fenol.
- Alfa och beta-naftol.
- Ortho, mål och för Cresol.
Kolhydrater
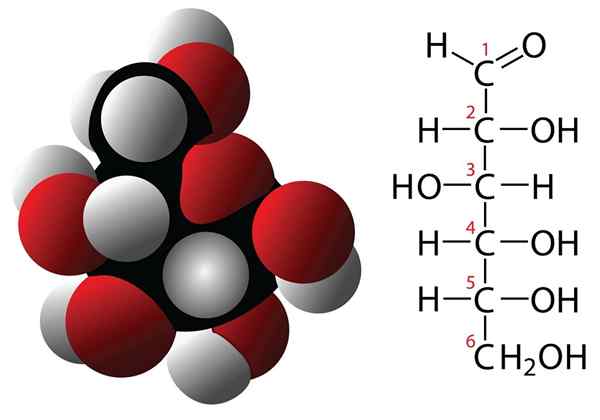 Glukos- och molekylformelmolekyl
Glukos- och molekylformelmolekyl Kolhydrater är föreningar med 3 eller fler kolatomer som kännetecknas av att ha en empirisk formel bildad av kol och vattenmolekyler. Dessa föreningar har ofta flera hydroxillogrupper som gör dem mycket lösliga i vatten. Några exempel på kolhydrater är:
- Glukos.
- Fruktos.
- Sackaros.
Karboxylsyror
Den karboxylfunktionella gruppen som finns i karboxylsyror motsvarar en av de mest sura funktionella grupperna som en organisk molekyl kan ha. Dessa föreningar är vanligtvis svaga syror när de jämför dem med vissa mineralsyror, men de kan bli betydligt sura beroende på deras struktur.
Syran av karboxylgruppen beror på närvaron av en hydroxylgrupp kopplad till en karbonylgrupp, som stabiliserar den negativa belastningen på anjonen som bildas när hydroxylen ger dess proton. Några exempel på karboxylsyror är:
- Ättiksyra.
- Bensoesyra.
- Trifluorättiksyra.
Sulfonsyror
Sulfonsyror är organiska föreningar som bildas av reaktionen mellan vissa organiska föreningar och svavelsyra eller svaveldioxid. Dessa typer av föreningar har en hydroxylgrupp och är i allmänhet ganska starka syror, jämförbara med svavelsyra.
Några exempel på sulfonsyror är:
- Pentosulfonsyra.
- Orto, mål och toluensulfonsyraisomerer.
- Bensulfonsyra.
Oorganiska syror
Hydroxylgrupper visas inte bara i organiska föreningar. Många oorganiska föreningar har också dem, i synnerhet oxacidsyror. I dessa fall är hydroxylgruppen direkt kopplad till en icke -metall, vanligtvis annorlunda än kol.
Några exempel på oorganiska syror som har hydroxylgrupper tillsammans med den icke -metall som den är kopplad till är:
- Hypoklorsyra, där hydroxylgruppen är kopplad till en kloratom.
- Svavelsyra, som har två hydroxylgrupper kopplade till en svavelatom.
- Fosforsyra, där de tre hydroxylgrupperna är kopplade till en fosforatom.

