Kopparhydroxid (II) Struktur, egenskaper, nomenklatur, användningar

- 4531
- 502
- Prof. Erik Johansson
han Kopparhydroxid (II) O CUPRIC Hydroxid är ett grönaktigt blått eller blått kristallint oorganiskt fast ämne vars kemiska formel är Cu (OH)2. Det erhålls som blå voluminös fällning genom att tillsätta en alkalisk hydroxid till cupric -lösningar (det betyder att de innehåller joner CU2+). Det är en instabil förening.
För att öka dess stabilitet är den beredd i närvaro av ammoniak (NH3) eller fosfater.Om du förbereder sig i närvaro av ammoniak finns ett material med god stabilitet och stor partikelstorlek.
 CUPRIC Hydroxide Prov, Cu (OH)2. Samzane på italienska Wikipedia [Public Domain] Källa: Wikipedia Commons
CUPRIC Hydroxide Prov, Cu (OH)2. Samzane på italienska Wikipedia [Public Domain] Källa: Wikipedia Commons När du förbereder sig med kopparfosfat (ii), CU3(PO4)2, En finare partikelstorlek och större ytarea erhålls. Kuprisk hydroxid används ofta som fungicid och baktericid i jordbruket och för att behandla trä, förlänga dess livslängd.
Det används också som animaliskt mattillskott. Det används som råmaterial för att erhålla andra koppar (ii) salter och i galvanoplastik för att täcka ytor.
Studier genomförs för att uppskatta deras potential att bekämpa bakterie- och svampinfektioner hos människan.
[TOC]
Strukturera
Kopparhydroxid (ii) innehåller oändliga kopparjoner (CU2+) United för hydroxylgrupper (OH-).
Kedjorna är så förpackade att två syreatomer från andra kedjor är över och under varje kopparatom och sedan antar en förvrängd oktaedrisk konfiguration, som är vanligt i de flesta kopparföreningar (ii).
I sin struktur är fyra syreatomer på ett avstånd av 1,93 A; Två syreatomer är 2,63 A; Och Cu-Cu-avståndet är 2,95 till.
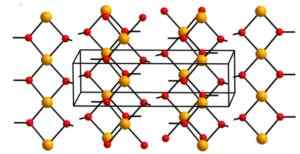 Kristallin struktur av cupric hydroxid. Aleksandar Kondinski [CC BY-SA.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Källa: Wikipedia Commons
Kristallin struktur av cupric hydroxid. Aleksandar Kondinski [CC BY-SA.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Källa: Wikipedia Commons Nomenklatur
- Kopparhydroxid (II).
- Kopparhydroxid.
- Koppardihydroxid.
Egenskaper
Fysiskt tillstånd
Kristallt fast.
Molekylvikt
99,58 g/mol.
Smältpunkt
Det bryts ner innan du smälter. Nedbrytningspunkt 229 ºC.
Kan tjäna dig: 25 exempel på löslighet i vardagenDensitet
3,37 g/cm3
Löslighet
Det är praktiskt taget olösligt i vatten: 2,9 mikrogram/L A 25 ºC. Snabbt lösligt i syror, i koncentrerade alkaliska lösningar och ammoniumhydroxid. Olöslig i organiska lösningsmedel. I varmt vatten sönderdelas det att generera kopparoxid (ii), vilket är mer stabilt.
Andra egenskaper
Det är lätt lösligt i starka syror och även i alkaliska koncentrerade lösningar av hydroxider, för att ge djupblå anjoner, förmodligen typen [Cun(ÅH)2n+2]2-.
Dess stabilitet beror på beredningsmetoden.
Det kan brytas ner genom att ge kopparoxid (ii) svart (CuO) om det förblir i vila några dagar eller låg uppvärmning.
I närvaro av ett överskott av alkali bryts det över 50 ° C.
Ansökningar
I jordbruket
Kopparhydroxid (ii) har bred tillämpning som fungicid och antibakteriell i jordbruksgrödor. Här är några exempel:
- Det tjänar mot bakteriefläckar ( Erwinia) I sallad, tillämpas som en bladbehandling.
- Mot bakteriefläckar (av Xanthomonas Pruni) I persikor, för vilka en latent och bladbehandling tillämpas.
- Det används mot blåkärens ark och stam genom latenta applikationer.
- Mot råtta under lagring av blåbär orsakade av Monilinia oxikokier, efter latent tillämpning.
För tillämpningen inom jordbruket används kopparhydroxid (II) som framställs i närvaro av fosfater på grund av dess lilla partikelstorlek.
 Salladodling. Källa: Pixabay
Salladodling. Källa: Pixabay Vid bevarande av trä
Trä, på grund av organisk natur, är känslig för attack av insekter och mikroorganismer. Kopparhydroxid (II) används som biocid för svampar som attackerar trä.
Det används vanligtvis bredvid en kvartär ammoniumförening (NH4+). Kopparhydroxid fungerar som en fungicid och den kvartära ammoniumföreningen fungerar som en insekticid.
På detta sätt håller behandlade trä eller motstår serviceförhållandena och når användarens nödvändiga prestationsnivå. Det trä som behandlas med dessa föreningar har emellertid en hög kopparnivå och är mycket frätande för vanligt stål, så en typ av rostfritt stål krävs som kan uthärda bearbetningen av behandlat trä.
Kan tjäna dig: reversibel reaktion: egenskaper och exempelTrots dess användbarhet anses kopparhydroxid (II) som en något farlig biocid.
Av denna anledning är det en oro för att det frigörs från det trä som behandlas på miljön i mängder som kan vara skadliga för mikroorganismerna som naturligtvis finns i vattnet (floder, sjöar, våtmarker och hav) eller jorden.
I Rayóns tillverkning
Sedan 1800 -talet har ammoniaklösningar av kopparhydroxid (II) använts för att lösa cellulosa. Detta är ett av de första stegen för att få fibern som heter Rayón genom tekniken utvecklad av Bemberg i Tyskland.
Kopparhydroxid (II) upplöses i en ammoniaklösning (NH3), bildar ett komplext salt.
Korta raffinerade bomullsfibrer tillsätts till ammonisk kopparlösning som innehåller kopparhydroxid (ii) i form av fällningsfast fast.
Bomullscellulosa bildar ett komplex med tetra-ammonium kopparhydroxid som upplöses i lösningen.
Därefter är denna lösning koagula när den passerar genom en extruderingsanordning.
På grund av dess höga kostnader har denna teknik redan övervunnits av Viscosa. Bembergs teknik används för närvarande endast i Japan.
Inom djurmatbranschen
Det används som spår i djurfoder, eftersom det är ett av de ämnen som krävs som mikronäringsämnen för den fullständiga näringen av djur.
 Koncentrerad mat till nötkreatur. Thamizhpparithi Maari [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikipedia Commons
Koncentrerad mat till nötkreatur. Thamizhpparithi Maari [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikipedia Commons Detta beror på att koppar i högre levande varelser är ett viktigt element som krävs för aktiviteten hos olika enzymer som innehåller koppar.
Till exempel finns det i enzymet som deltar i produktionen av kollagen och enzymet som krävs för melaninsyntes, bland andra.
Kan tjäna dig: aminerDet är en förening som allmänt erkänds som försäkring när den läggs till nivåer i överensstämmelse med god matpraxis.
 Mjölkiga kor. Källa: Pixabay
Mjölkiga kor. Källa: Pixabay Vid tillverkning av andra kopparföreningar (ii)
Föregångare aktiv i produktionen av följande kopparföreningar (II): Koppar (II), 2-Otylhexanoat koppar (II) och koppar tvålar och koppar tvålar. I dessa fall används kopparhydroxid (II) som syntetiseras i närvaro av ammoniak.
Andra användningsområden
Det används vid nylonstabilisering, i batterielektroder; som färgfixer i färgningsoperationer; som pigment; i insekticider; vid pappersbehandling och färgning; i katalysatorer, som en katalysator i vulkaniseringen av polysulfidgummi; som anti -sniffing pigment; och i elektrolys, i galvanoplastik.
Framtida medicinska tillämpningar
Kopparhydroxid (II) är en del av kopparföreningar som studeras i form av nanopartiklar för eliminering av bakterier, såsom OCH. coli, K. pneumoniae, s. Aeruginosa, Salmonella spp., bland andra orsaker till sjukdomar hos människor.
Det har också visat sig att koppar -nanopartiklar kan vara effektiva mot Candida albicans, En svamp som är vanlig orsak till mänskliga patologier.
Detta indikerar att koppar -nanoteknologi kan spela en viktig roll mot bakterier och svampar som orsakar mänskliga infektioner, och kopparhydroxid (II) kan vara mycket användbar inom dessa fält.
Referenser
- Bomull, f. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Kirk-THERMER (1994). Encyclopedia of Chemical Technology. Volym 7. Fjärde upplagan. John Wiley & Sons.
- Ullmanns Encyclopedia of Industrial Chemistry. (1990). Femte upplagan. Volym A7. VCH Verlagsgellschaft MBH.
- Dans, j.C.; Emeléus, h.J.; Sir Ronald Nyholm och Trotman-Deckenson, till.F. (1973). Omfattande oorganisk kemi. Volym 3. Pergamonpress.
- National Library of Medicine. (2019). Koppar (ii) hydroxyde. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- Schiopu, n. och Tiruta-Brana, L. (2012). Träbevarande. I toxicitet hos buffertmaterial. Kapitel 6. Återhämtat sig från Scientedirect.com.
- Mordorski, b. och Friedman, till. (2017). Metallnanopartiklar för mikrobiell infektion. I funktionaliserade nanomaterial för hantering av mikrobiell infektion. kapitel 4. Återhämtat sig från Scientedirect.com.
- Takashi tsurumi. (1994). Lösningssnurrning. I avancerad fibernurningsteknik. Kapitel 3. Återhämtat sig från Scientedirect.com.
- « Histochemistry Foundation, bearbetning, färgning
- Cerio Oxide (IV) Struktur, egenskaper, användningar »

