Kaliumhydroxidstruktur, egenskaper, användningar

- 2098
- 495
- PhD. Emil Svensson
han kaliumhydroxid Det är ett vitt kristallint oorganiskt fast ämne. Dess kemiska formel är KOH. Dess kristaller absorberar lätt luft från luften, så det sägs att det är en hygroskopisk förening. Det är en stark bas och absorberar koldioxid (CO2) i miljön.
Industriellt förekommer genom elektrolys av kaliumklorid (KCL). Av skäl för energibesparing och produktrenhet används kvicksilverceller (HG) i denna metod.
 Kaliumhydroxidpärlor (KOH). Ingen maskinläsbar författare tillhandahållen. Walkerma antas (baserat på upphovsrättsanspråk). [Public Domain] Källa: Wikipedia Commons
Kaliumhydroxidpärlor (KOH). Ingen maskinläsbar författare tillhandahållen. Walkerma antas (baserat på upphovsrättsanspråk). [Public Domain] Källa: Wikipedia Commons Men under många år har det varit oro över föroreningen av kvicksilver som genererar denna process. I själva verket är utsläpp till avfallsloppare som innehåller kvicksilver strikt förbjudna. Det finns andra processer som membran och membran.
Det finns också icke-elektrokemiska processer såsom sönderdelning av kaliumnitrit (KNO2) I närvaro av järnoxid (tro2ANTINGEN3).
KOH-lösningar erhållna i industriella processer förångas för att uppnå KOH vid 90-95%. 5-10% vattenrester är kopplat till KOH i form av kaliumhydroxidmonohydrat (KOH.H2ANTINGEN).
På grund av dess kaustiska egenskaper och dess starka basicitet har den mycket varierande tillämpningar. Det fungerar som råmaterial i tvålar och tvättmedel, tryck eller kosmetikfärger, bland andra användningsområden. Det används också för att tvätta industriella gaser, i detekteringen av svampar med mikroskop och har applicering inom livsmedelsindustrin.
Även om det är en mycket stabil förening klassificeras den som frätande. Det måste manipuleras noggrant, eftersom det kan orsaka brännskador i ögon, hud och slemhinnor.
[TOC]
Strukturera
KOH -kristallen vid vanliga temperaturer är monoklinisk, varvid varje kaliumatom (K) omgiven av en octaedro förvrängd från syreatomer (O). I sin tur bildar hydroxyl (OH) -grupper en sicksackformad kedja kopplad av hydrogener, där O-O-avstånd är 3,35 A, vilket kasserar någon betydande vätebindning.
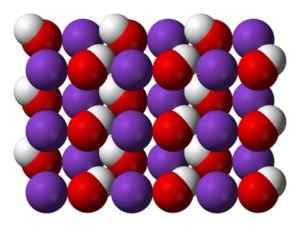 KOH: s kristallina struktur vid vanliga temperaturer. Blått: kalium, röd: syre, vit: väte. Benjah-Bmm27 [Public Domain]. Källa: Wikipedia Commons
KOH: s kristallina struktur vid vanliga temperaturer. Blått: kalium, röd: syre, vit: väte. Benjah-Bmm27 [Public Domain]. Källa: Wikipedia Commons Vid höga temperaturer har Koh en kubisk kristallin form.
Det kan tjäna dig: Cruise for Crucible: Egenskaper, funktioner, använda exempelNomenklatur
- Kaliumhydroxid.
- Kaustisk potas.
- Kaliumhydrat.
- Kaliumblekmedel.
Egenskaper
Fysiskt tillstånd
Vit kristallint fast.
Molekylvikt
56,106 g/mol.
Smältpunkt
380 ºC; 406 ºC har också rapporterats (det varierar beroende på vatteninnehållet). Den tekniska examen (90-92% KOH) smälter ungefär 250 ºC.
Kokpunkt
1327 ºC.
Densitet
2,044 g/cm3
Löslighet
Lösligt i kallt vatten (107 g/100 ml vid 15 ºC) och varmt vatten (178 g/100 ml vid 100 ° C). Dess upplösning i vatten är en mycket exoterm process, detta innebär att en stor mängd värme genereras.
Löslig i alkohol. Lösligt i glycerin. Olöslig i eter.
pH
13.5 (i 0,1 molär vattenlösning).
Andra egenskaper
Dess kristaller är delikat eller hygroskopiska, vilket innebär att den absorberar luft från luften. Absorbera också CO2 från luften.
Dess kemiska reaktioner är egenskaperna hos en stark bas. I vattenlösning reagerar den med någon svag syra för att bilda kaliumsaltet av syra. Till exempel reagerar den med kolsyra (h2Co3) eller med koldioxid (CO2) Att bilda bikarbonat- eller kaliumkarbonat.
Reagerar med alkoholer för att bilda kaliumalcoxider, eller med vätesulfid H2S för att bilda sulfid eller kaliumbisulfid.
I vattenhaltiga system bildar KOH flera hydrater: mono-, di- och tetra-hydrater.
Koh vattenhaltiga lösningar är färglösa, starkt grundläggande, tvål och kaustiska. Det är ett frätande material, både fast och i lösning.
Det är inte brandfarligt, men när det värms upp tills dess sönderdelning avger giftiga och frätande röker av k2ANTINGEN.
Orsakar svåra brännskador i ögon, hud och slemhinnor och i kontakt med metaller, såsom aluminium, tenn, bly eller zink, kan generera utvecklingen av vätgas (h2), vilket är mycket brandfarligt.
Värmen som produceras när den kommer i kontakt med fukt eller andra ämnen kan orsaka tillräckligt med värme för att slå på brännbara material.
Ansökningar
Vid produktion av andra kaliumföreningar
Kaliumhydroxid används som råmaterial för kemisk och farmaceutisk industri. Det tjänar till att producera kaliumkarbonat (K2Co3), Kaliumpermanganat (KMNO4), kaliumfosfat (k3Po4), kaliumsilikat (k2Sio3) och kaliumcyanid (KCN), bland andra föreningar.
Kan tjäna dig: linjära alkaner: struktur, egenskaper, nomenklatur, exempelI flera applikationer
Den höga renheten KOH har tillämpning inom tillverkning av bekämpningsmedel, bläck och färgämnen syntes, kemikalier för gummi eller galvanoplastik, litografi, etc.
Den tekniska graden KOH används som råmaterial inom tvättmedel och tvålindustrin; vid tillverkning av kosmetika, glas och textilier; att avvivla råolja; som torkmedel och vid borttagning av målningar och lack, bland andra applikationer.
Det är också användbart som ett kaustiskt medel inom träindustrin, i bomulls mercerisering, i analytisk kemi för alkalimetriska titlar, organisk och vattenbehandling.
I medicinska tillämpningar
I medicin används den i våt montering under framställningen av kliniska prover för mikroskopisk visualisering av svampar och andra svampelement i läder, hår, naglar, bland andra.
KOH -beredning används för att klargöra det kliniska materialet så att svampelementen lättare kan ses.
Ett kliniskt provfragment tillsätts till en 10% KOH -lösning på en glasskiva. Täck sedan med ett täckningsobjekt och låt stå vid rumstemperatur för att tillåta matsmältning av värdceller. Slutligen observeras det med mikroskopet.
 Mikroskop. Kontantin Kolosov Bild. Källa: Pixabay
Mikroskop. Kontantin Kolosov Bild. Källa: Pixabay Å andra sidan är KOH i form av aktuell lösning effektiv vid behandling av vårtor.
I den kosmetiska industrin
Det används i vissa nagelrengöringsprodukter, rakkräm och tvålar, eftersom dess frätande egenskap gör det mycket effektivt vid nedbrytning eller borttagning av mjukvävnad och hårborttagning.
 Tvålar. Ritualbild. Källa: Pixabay
Tvålar. Ritualbild. Källa: Pixabay I jordbruket
Det används i gödselmedel och andra jordbruksprodukter som herbicider och bekämpningsmedel.
I industrikemiska processer
KOH är användbart vid rengöring och rening av industriella gaser, särskilt när det krävs att ta bort syror.
Kan tjäna dig: Henderson-Haselbalch-ekvation: Förklaring, exempel, träningTill exempel för att det är lätt att reagera med CO2, Den används för att absorbera denna gas. Dessutom är det idealiskt att reagera med syror, så det tjänar till att avlägsna sulfhydronsyra (h2S). Och på liknande sätt för att ta bort kväveoxider.
 Industriell process. Michael Gaida -bild. Källa: Pixabay
Industriell process. Michael Gaida -bild. Källa: Pixabay I livsmedelsindustrin
Det används för att justera pH, som en stabilisator och som en förtjockningsmedel i livsmedelsindustrin.
Det har beaktats av US Food and Drug Administration, eller FDA (för dess förkortning för engelska Food and Drug Administration), Som en direkt ingrediens hos människor, förutsatt att den används under förhållanden relaterade till god tillverkningspraxis.
För att få biodiesel
Biodiesel är en diesel- eller dieselersättningsförbränbar vätska. Det erhålls från vegetabiliska oljor eller djurfetter. KOH har använts som katalysator i biodieselproduktion.
Nyliga studier
Under flera år ägnas uppmärksamhet åt föroreningen av hav.
Av denna anledning försöker vi hitta metoder som tillåter bearbetning av matsmältningskanalprover av djur, upplösning av det organiska materialet men utan att lösa upp plasten som intas av proverna.
I denna mening har det visat sig att användningen av KOH -lösningar för att separera plast från organiskt material är en praktisk och effektiv metod, som kan vara mycket användbar i kvantitativa studier av plastintag av djurlivet.
Referenser
- Mahmoud a. Ghanoum och Nancy C. Iseham. (2009). Dermatofyter och dermatofytos. I klinisk mykologi. Andra upplagan. Återhämtat sig från Scientedirect.com.
- Kühn, s. et al. (2016). Användningen av kaliumhydroxid (KOH) som ett lämpligt tillvägagångssätt för att isolera plast som intas av marina organismer. I marinföroreningsbulletin. Återhämtat sig från Scientedirect.com.
- Bomull, f. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Kirk-THERMER (1994). Encyclopedia of Chemical Technology. Volym 19. Fjärde upplagan. John Wiley & Sons.
- Ullmanns Encyclopedia of Industrial Chemistry. (1990). Femte upplagan. Volym A22. VCH Verlagsgellschaft MBH.
- National Library of Medicine. (2019). Kaliumhydroxyd. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- Krisada Nooiroj, et al. (2009). I jämförande studie av Koh/Al2ANTINGEN3 och KOH/NAY -katalysatorer för biodieselproduktion via transcesserifiering från palmolja. I förnybar energi. Återhämtat sig från Scientedirect.com.
- « Organisatoriska värden egenskaper, betydelse, exempel
- Alsacia och Lorena territorium, bakgrund, världskrig »

