Tillväxthormon (somatotropin) struktur, funktioner
- 3468
- 595
- Johan Johansson
De Somatotropin (STH) U Growth Hormon (GH) är ett relativt litet protein som produceras på nivån av adenohypofys och involverad i utvecklingsprocesser, längsgående tillväxt av organismen och i kontrollen av flera metaboliska processer.
Det är ett icke -glaro -hormon. Gandotropas hormoner i hypofysen samlas.
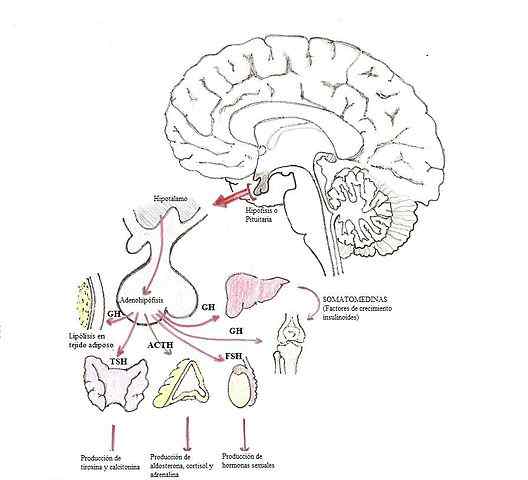
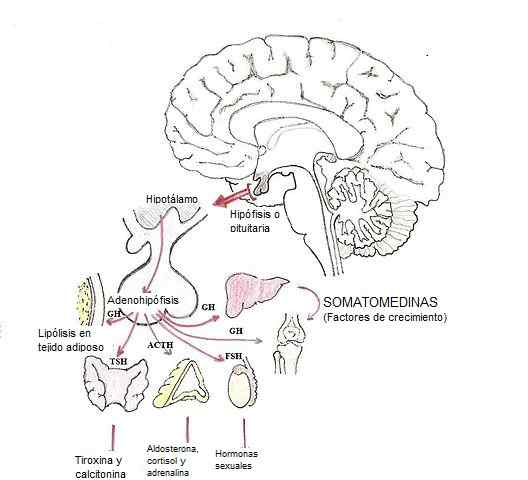 Modifiering av hormoner i hypofysen (Källa: Dubaele / Public Domain, via Wikimedia Commons)
Modifiering av hormoner i hypofysen (Källa: Dubaele / Public Domain, via Wikimedia Commons) Glandotropas hormoner är till exempel adrenokortopin (ACTH), gonadotropiner (FSH och LH) och sköldkörtelstimulerande hormon (TSH).
Icke -Glandropas hormoner, å andra sidan, och bland vilka prolaktin och tillväxthormon ingår, agerar utan tävling från någon annan endokrin körtel, eftersom de utövar sina handlingar direkt på de vita cellerna vars aktiviteter reglerar.
[TOC]
Strukturera
Tillväxthormon är ett relativt litet protein som förekommer i flera isoformer. Den huvudsakliga isoformen består av cirka 191 aminosyror, har en 22 kDa molekylvikt och kommer från en längre föregångspeptid (pre-GH) på 28 kDa, som också utsöndras men som saknar fysiologiska funktioner.
I sin struktur verkar somatotropin vara homologerat till prolaktin och korioniskt somatomamototropin (CS), producerade det senare i moderkakan. Sådan är likheten, som anses att de tre bildar en hormonell familj.
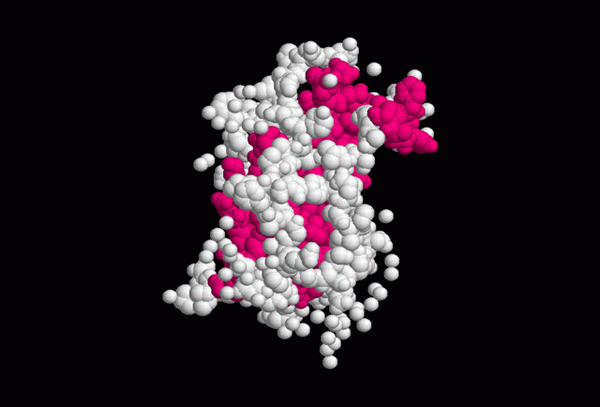 Ungefärlig struktur för tillväxthormonet (källa: роан бекер, via Wikimedia Commons)
Ungefärlig struktur för tillväxthormonet (källa: роан бекер, via Wikimedia Commons) Den sekundära strukturen för somatotropin visar 4 alfa -propeller stabiliserade med två disulfidbroar, vars konfiguration är nödvändig för interaktionen mellan hormonet med dess mottagare.
Ett faktum i relation till strukturen och värdig att bli markerad representerar det faktum att trots att tillväxthormonerna hos olika arter har anmärkningsvärda likheter med människan, endast den senare och primater, utövar effekter som är betydande hos människor.
Funktioner
Somatotropinfunktioner beskrivs vanligtvis som de som är förknippade med utvecklingen och tillväxten av organismen. Även de som är förknippade med metabolism, som inkluderar modifieringar i lipidmetabolism och glukos som främjas av hormon.
Tillväxtfunktioner kan emellertid också betraktas som metaboliskt, eftersom de antyder anabola funktioner associerade med proteinsyntes, som inte utesluter vissa andra funktioner utan direkt associering med metabolism såsom cellproliferation.
Några av de funktioner eller åtgärder som används av somatotropin utövas av detta hormon direkt över dess vita vävnader, men många av dem utförs av vissa andra ämnen vars syntes och frisättning stimuleras av tillväxthormonet.
IGF -syntes
Den första raden av somatotropinverkan är just syntesen av dessa ämnen som kallas tillväxtfaktorer som liknar insulin (IGF), varav typ 1 och 2 har identifierats. De utses till IGF1 (de viktigaste) och IGF2, enligt dess förkortning på engelska.
Dessa faktorer var ursprungligen kända och betecknas fortfarande, som mediatorer av somatotropin eller somatomediner C (IgF1) och A (IgF2) eller också som en aktivitet som liknar icke -suppressibel insulin (NSILA). De syntetiseras av många celltyper, men förekommer främst i levern.
STH och IGF1: s åtgärder är mycket olika. Vissa utövar var och en av dessa ämnen oberoende, ibland i samband och synergistiskt och andra gånger agerar de antagoniskt.
Kan tjäna dig: elektrofores: foundation, teknik, vad är det för, exempelTillväxtinduktion
Detta är en av de viktigaste åtgärderna som främjas av somatotropin, men utförda i samband med IGF1. Även om båda inducerar tillväxten av många kroppsvävnader utförs deras mest framträdande effekt på skeletttillväxt.
Detta slutliga resultat produceras av flera effekter inducerade av hormonet och IGF1. De inkluderar ökningen av proteinavlagring av kondrocytiska och osteogena celler, den högsta reproduktionshastigheten för dessa celler och omvandlingen av kondrocyter till osteogena celler; Som alla leder till den nya benavsättningen.
Under tillväxten och utvecklingen av organismen, och före stängningen av benepifyser, avsätts ny brosk i epifyser följt av dess omvandling till ett nytt ben, som förlänger diaphysen och epifyserna är separerade.
Den progressiva konsumtionen av epifyseal brosk avlägsnar den och benet kan inte fortsätta växa. I slutet av tonåren bromsas diafysen och epifyserna och tillväxten i lång benlängd till varje ände och slutar slutligen.
En andra mekanism kan förklara ökningen av bentjockleken. Osteoblasterna i periosteium deponerar nytt ben på det gamla, och osteoklasterna eliminerar det gamla benet. Om avsättningshastigheten överstiger eliminationen ökar tjockleken.
När tillväxthormonet utövar intensiv stimulering på osteoblaster, kan under dess effekt tjockleken på benen fortsätta, även om dess längd inte längre modifieras på grund av stängningen av epifyser.
Främjande av proteinavlagring i vävnader
Denna effekt kan uppnås genom olika mekanismer: ökningen av transport av aminosyror genom cellmembran, ökningen av RNA -översättning på ribosomnivån, ökningen av transkription av DNA till RNA i kärnan och en minskning av protein- och aminosyran katabolism.
Andra metaboliska åtgärder
I fettvävnad främjar tillväxthormon lipolys och frisättning av fettsyror till cirkulationstorrenten, vilket ökar dess koncentration i kroppsvätskor. Samtidigt gynnar det i alla vävnader omvandlingen av fettsyror i acetylkoenzym A och dess användning som en energikälla.
Stimuleringen av användningen av fetter, tillsammans med ackumulering av proteiner på grund av deras anabola effekt, leder till en ökning av mager vävnad.
Ökningen av mobiliseringen av fetter kan vara så hög att levern producerar stora mängder acetoättiksyra som leder till ketos och en fet lever kan genereras.
I förhållande till metabolismen av kolhydrater inkluderar effekterna av somatotropin minskningen av glukosuppsamlingen i fett och muskulös muskelvävnad, ökad glukosleverproduktion och ökad insulinsekretion.
Alla dessa effekter kallas diabetogener, och hormonutsöndring med hög tillväxt kan reproducera metaboliska förändringar som följer icke -insulinberoende typ II -diabetes.
Andra funktioner
De anabola och mitogena verkningarna från GH och IGF1 manifesteras också i tillväxt och funktion av hjärtat, levern, mjälten, sköldkörteln, tymus och tungan och tungan. Hormonet kan bidra till att hudens förtjockning, till stimulering av svettkörtlarna och hårväxten.
I njurarna ökar den glomerulära filtreringshastigheten och syntesen av calcitriol, vilket gynnar inte bara tillväxt, utan också benmineralisering. Det främjar också erytropoies och fibrinogensyntes och immunsvar genom stimulering av T -lymfocyter och makrofager.
Kan tjäna dig: epitelvävnad: egenskaper, beskrivning, funktioner, typerReceptorer för somatotropin
Somatotropinåtgärder, inklusive främjande av syntes av tillväxtfaktorer som liknar insulin, förmedlas genom deras förening med specifika receptorer uttryckta i vita cellmembran.
Det finns två former av dessa receptorer, varav den andra är en kort (trunkerad) variant av den första; Trunkerad form som hämmar funktionen hos den långa mottagaren, och att om överuttryckt skulle ge vävnadskänslighet för hormonet.
Den långa mottagaren består av 638 aminosyror och har en extracellulär domän på 250, en alfa -transmembraal domän på cirka 38 och en intracellulär domän på 350 aminosyror. Varje somatotropinmolekyl hamnar i två mottagarmolekyler och producerar det som kallas receptordimeriseringen.
Denna dimerisering aktiverar ett JAK2 -kinasprotein beläget på de intracellulära ändarna av varje monomer i mottagaren och dessa aktiva kinasfosforylat Andra substrat såsom STAT5 och somatotropinreceptorn själv.
De fosforylerade STAT5 -molekylerna lider också av en dimerisering som gör dem mycket exakta regulatorer för genuttryck och proteinsyntes.
Produktion
Somatotropin syntetiseras på nivån av adenohypofysen Somatotropas -celler. Dessa celler färgas intensivt med sura ämnen så att de också kallas acidofiler. De är tillsammans den vanligaste cellgruppen i körtlarna eftersom de representerar 50% av totalt 5 olika typer.
Det finns ett genetiskt komplex av 5 gener i den långa armen av den mänskliga kromosomen 17 som kodar för de olika isoformerna av tillväxthormonet och det humana korioniska somatomamototropinet (HCS).
En av dem är den normala HGH-N, som kodar för den vanligaste formen av mänskligt tillväxthormon som är ovannämnda av 22 kDa och representerar 75% av det totala cirkulerande tillväxthormonet.
Hans messenger RNA utsätts för "Klipp och skarvning" För att producera en mindre form av hormonet, på 20 kDa, som saknar aminosyravfall från 32 till 46 och representerar 10%.
En andra gen (HGH-V) uttrycks huvudsakligen i moderkakan och kodar en variant form av HGH av vilken endast betydande mängder förekommer i cirkulationen under graviditeten. De andra 3 generna kodar isoformer av somatomamototropin människa.
Släpp
Både syntes och utsöndring eller frisättning av tillväxthormon regleras av stimulerande och hämmande faktorer i sådana funktioner.
Stimulerande influenser
Bland de huvudsakliga humoristiska påverkningarna som stimulerar syntes och somatotropinsekretion är GHRH -peptider (tillväxthormon som frigör hormon) och ghrelin.
Tillväxthormonet som frigör hormonet (GHRH) är en hypotalamisk peptid som finns i två varianter av 40 respektive 44 aminosyror. Den leder i somatotropasceller till syntesen av AMPC och till aktiveringen av den specifika PIT1 -transkriptionsfaktorn för tillväxthormonet.
Ghrelin är ett endogen av tillväxthormon av tillväxthormon. Det är en peptid av cirka 28 aminosyror syntetiserade vid hypotalamus och magnivå. Det fungerar synergistiskt med GHRH vars frisläppande främjar, samtidigt som det hämmar somatostatin. Handlar genom receptorer som aktiverar fosfolipas C.
Vissa metaboliska parametrar såsom hypoglykemi, låga nivåer av fria fettsyror i blod och höga aminosyrakoncentrationer är viktiga stimuli för utsöndring av tillväxthormon.
Kan tjäna dig: De 12 stadierna av mänsklig utveckling och dess egenskaperAndra stimulerande faktorer som räknas är akut stress, överbelastning av kroppen, smärta, könssteroider (pubertet), dopamin, stimulering av a2-receptorer, acetylkolin, galanin, serotonin och p-endorfin.
Hämmande influenser
Bland dessa är somatostatin eller hormoninhibitor för frisättning av tillväxthormon (GHRIH) och negativ återkoppling.
Somatostatin är en hypotalamisk peptid av 14 aminosyror som hämmar utsöndring, men inte syntes, av tillväxthormon. En lång variant, 28 aminosyror, syntetiseras i mag -tarmkanalen. Båda varianterna binder till samma mottagare och hämmar cyklisk AMP -syntes.
När det gäller negativ feedback, frigör GH, genom en självsocial handling, hämmar sin egen ytterligare utsläpp. IGF1 hämmar hypotalamus till tillväxthormonet i tillväxthormon och stimulerar somatostatin, medan han hämmar GH -syntes i hypofysen.
Vissa metaboliska parametrar såsom hyperglykemi, höga plasmanivåer av fria fettsyror och låga aminosyranivåer är somatotropinsekretionshämmare.
Hämmare är också kalla, kronisk stress, fett, progesteron, sköldkörtelhormoner, underskott eller kortisolöverskott och stimulering av adrenerga receptorer ß2 ß2.
Dos
Den terapeutiska användningen av biosyntetiserat tillväxthormon indikeras för behandling av de lidande där en brist i sin utsöndring har avslöjats, i hypofysen dvärg och i lågt sized barn av Turners syndrom.
Administrationen är gjord i form av en injicerbar lösning som byggs om från en väg som innehåller en lyofiliserad med 40 u.Yo. av det biosyntetiska hormonet, och till vilket de 2 ml följeslagarna med 0,9 % natriumkloridlösning läggs till.
Vid tillväxthormonbrist hos barn rekommenderas det mellan 0,07 och 0,1 U.Yo./kg kroppsvikt per dag. I turnersyndrom 0,14 u.Yo./kg kroppsvikt per dag. För tillväxthormonbrist hos vuxna: 0,018 till 0,036 U.Yo./kg kroppsvikt per dag.
Effekter
Den terapeutiska administrationen av tillväxthormon kan åtföljas av vissa negativa säkerhetseffekter såsom manifest överkänslighet genom generaliserad urtikaria, fasta hypoglykemi, inflammation på injektionsstället och passagerarhuvudvärk.
Utvecklingen av en viss godartad intrakraniell hypertoni har beskrivits, mer frekvent hos barn och mindre hos vuxna.
Beträffande kolhydratmetabolism har utvecklingen av diabetes mellitus rapporterats hos patienter som fick behandling med tillväxthormon.
I förhållande till skelettmuskelsystemet finns bevis på inflammatorisk myosit med myalgi och muskelsvaghet, producerad inte av hormonet, utan kanske av metakresol som används som konservativ i formeln.
Fall av gynekomasti, anemi och akut pankreatit har rapporterats.
Referenser
- Ganong WF: Hypofysen, 25: e upplagan. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: hypofyshormoner och deras kontroll av hypotalamus, i Lärobok för medicinsk fysiologi, 13: e upplagan, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lang F, Verrey F: Hormon, i Physiologie des Menschen Mite Pathophysiologie, 31 ED, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010
- Voigt K: Endokrines System, i Physiologie, 6: e upplagan; R KLINKE et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H och Strang KT: The Endocrine System. Hypotalamus och hypofysen, i Vanders mänskliga fysiologi: Mekanismerna för kroppsfunktion, 13: e upplagan; EP Windmaier et al (eds). New York, McGraw-Hill, 2014.

