Heisenberg atommodell
- 4290
- 691
- Johan Eriksson
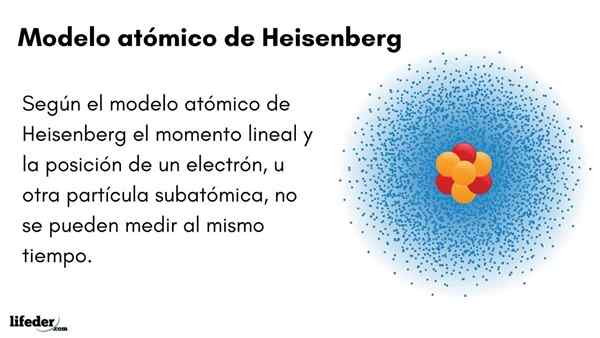
Vad är Heisenbergs atommodell?
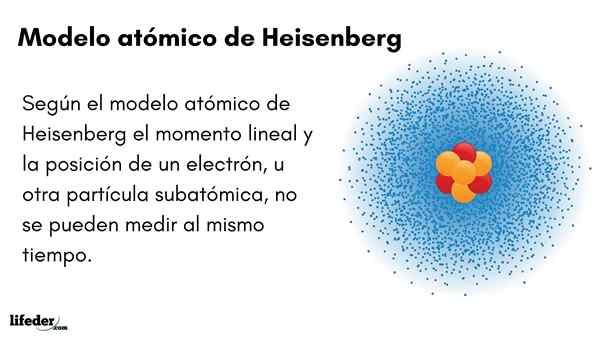
han Heisenberg atommodell (1927) introducerar osäkerhetsprincipen i elektronorbitaler som omger atomkärnan. Den enastående tyska fysikern etablerade grunden för kvantmekanik för att uppskatta beteendet hos subatomära partiklar som utgör en atom.
Osäkerhetsprincipen för Werner Heisenberg indikerar att det inte är möjligt att med säkerhet veta den linjära positionen för en elektron samtidigt. Samma princip gäller för tids- och energivariabler; Det vill säga, om vi har en indikation på elektronens position, kommer vi att ignorera elektronens linjära ögonblick och vice versa.
Kort sagt är det inte möjligt att samtidigt förutsäga värdet på båda variablerna. Ovanstående innebär inte att någon av de tidigare nämnda storleken inte kan kännas med precision. Närhelst det är separat finns det inget hinder för att få värdet av intresse.
Osäkerhet sker emellertid när det gäller att samtidigt känna till två konjugerade storlekar, som är fallet med den linjära positionen och ögonblicket.
Denna princip uppstår på grund av strikt teoretiskt resonemang, som den enda genomförbara förklaringen som ger anledning till vetenskapliga observationer.
Egenskaper för Heisenberg Atomic Model
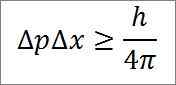 Werner Heisenberg
Werner Heisenberg I mars 1927 publicerade Heisenberg sitt arbete På det perceptuella innehållet i film och kvantmekanik, Där han detaljerade principen om osäkerhet eller obestämdhet.
Denna princip, grundläggande i den atomiska modellen som föreslagits av Heisenberg, kännetecknas av följande:
- Osäkerhetsprincipen uppstår som en förklaring som kompletterar de nya atomteorierna om elektronbeteende. Trots att man använder mätinstrument med hög precision och känslighet är obestämdhet fortfarande närvarande i någon experimentell studie.
- På grund av osäkerhetsprincipen, när du analyserar två relaterade variabler, kommer du att öka om du har en exakt kunskap om en av dessa, att ökar obestämningen om värdet på den andra variabeln.
- Det linjära ögonblicket och positionen för en elektron, eller en annan subatomisk partikel, kan inte mätas samtidigt.
- Förhållandet mellan båda variablerna ges av en ojämlikhet. Enligt Heisenberg, produkten av variationerna i det linjära ögonblicket -3. 4 Jules x sekunder) och 4π, som beskrivs i följande matematiska uttryck:
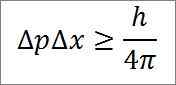
Legenden som motsvarar detta uttryck är som följer:
∆P: Obestämmelse av linjärt ögonblick.
∆x: obestämningen av positionen.
H: Plankkonstant.
π: PI 3.14 -nummer.
- Med tanke på ovanstående har produkten av osäkerheter som sitt lägre stopp förhållandet h/4π, vilket är ett konstant värde. Därför, om en av storleken tenderar att noll, måste den andra öka i samma andel.
- Detta förhållande är giltigt för alla par konjugerade kanoniska storlekar. Till exempel: Heisenbergs osäkerhetsprincip är perfekt tillämplig på energitidsduon, såsom beskrivs nedan:
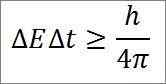
I detta uttryck:
∆E: Energi obestämdhet.
∆t: obestämd tid.
H: Plankkonstant.
π: PI 3.14 -nummer.
- Från denna modell följer det att absolut kausal determinism i konjugat kanoniska variabler är omöjlig, eftersom för att fastställa detta förhållande bör kunskapen om de initiala värdena för studievariablerna fastställas.
- Följaktligen är Heisenberg -modellen baserad på sannolikhetsformuleringar på grund av slumpmässigheten som finns mellan variablerna till subatomiska nivåer.
Experimentella tester
Heisenbergs osäkerhetsprincip uppstår som den enda möjliga förklaringen till de experimentella testerna som ägde rum under de första tre decennierna av 2000 -talet.
Innan Heisenberg uttalade då osäkerhetsprincipen föreslog de föreskrifterna som i kraft genom att de linjära momentumvariablerna, vinkelmoment, tid, energi, bland andra, för de subatomära partiklarna som de var operativt definierade.
Detta innebar att de behandlades som om de var klassisk fysik; Det vill säga ett initialvärde mättes och det slutliga värdet uppskattades enligt den förutbestämda proceduren.
Kan tjäna dig: vektorstorlekOvanstående innebar att definiera ett referenssystem för mätningar, mätinstrumentet och formen för användning av nämnda instrument, enligt den vetenskapliga metoden.
Enligt detta var de variabler som beskrivs av subatomära partiklar att bete sig avgörande. Det vill säga dess beteende bör förutsägas exakt och exakt.
Men varje gång en uppsats av denna art utfördes var det omöjligt att få i mätningen det uppskattade värdet teoretiskt.
Åtgärderna var felaktiga på grund av de naturliga förhållandena i experimentet, och resultatet som erhållits var inte användbart för att berika atomteorin.
Exempel
Till exempel: Om det handlar om att mäta hastigheten och positionen för en elektron, måste experimentets montering fundera över kollisionen mellan en foton av ljus med elektronen.
Denna kollision inducerar en variation i elektronens inre hastighet och position, så att mätningsobjektet förändras av experimentella förhållanden.
Därför uppmuntrar forskaren förekomsten av ett oundvikligt experimentellt fel, trots noggrannheten och precisionen för de instrument som används.
Kvantmekanik annan än klassisk mekanik
Utöver ovanstående anger Heisenberg obestämd princip att kvantmekanik per definition fungerar annorlunda med avseende på klassisk mekanik.
Följaktligen antas det att den exakta kunskapen om de subatomiska åtgärderna begränsas av den tunna linjen som skiljer klassisk och kvantmekanik.
Heisenberg -modellbegränsningar
Trots att han förklarar obestämda partiklar och sitter skillnaderna mellan klassisk och kvantmekanik, upprättar Heisenbergs atommodell inte en unik ekvation för att förklara slumpmässigheten i denna typ av fenomen.
Kan tjäna dig: gravitationsenergi: formler, egenskaper, applikationer, övningarDessutom innebär det faktum att förhållandet är etablerat genom en ojämlikhet att utbudet av möjligheter för produkten av två konjugerade kanoniska variabler är obestämd. Följaktligen är osäkerheten som är inneboende i subatomiska processer betydande.
Intresseartiklar
Schrödinger Atomic Model.
Bros.
Chadwick atommodell.
Perrin atommodell.
Thomson Atomic Model.
Dalton Atomic Model.
Dirac Jordan Atomic Model.
Demokritusatommodell.
Leucipo Atomic Model.
Bohr atommodell.
Sommerfeld Atomic Model.
Nuvarande atommodell.
Referenser
- Beyler, r. (1998). Werner Heisenberg. Encyclopædia Britannica, Inc. Återhämtat sig från: Britannica.com
- Heisenbergs osäkerhetsprincip (s.F.). Återhämtat sig från: hiru.Eus
- Garcia, J. (2012). Heisenberg osäkerhetsprincip. Återhämtat sig från: hiberus.com
- Atommodeller (s.F.). National Autonomous University of Mexico. Mexico City, Mexiko. Återhämtat sig från: rådgivning.Cuautitlan2.Unk.mx
- Werner Heisenberg (s.F.).Hämtad från: The History-off-theatom.Wikispaces.com
- Wikipedia, Free Encyclopedia (2018). Plankkonstant. Återhämtad från: är.Wikipedia.org
- Wikipedia, Free Encyclopedia (2018). Heisenberg obestämd relation. Återhämtad från: är.Wikipedia.org

