Markovnikov -regel
- 968
- 89
- Hans Olsson
Vad är Markovnikovs regel?
De Markovnikov -regel Det är en empirisk regel, formulerad 1869 av den ryska kemisten Vladimir Markovnikov, som används för att förutsäga regioselektiviteten hos produkterna från ett elektrofilt tillägg. Till och med idag är det fortfarande i kraft, vilket avslöjar sin enkelhet i hur mekanismen för flera organiska reaktioner kommer.
Denna regel gäller särskilt alkener i deras hydrohalogeneringsreaktioner. Således tillåter det att förutsäga vad majoritetsprodukterna kommer att vara när Alkenes och Alkynes reagerar med HX (HF, HCL, HBR och HI).
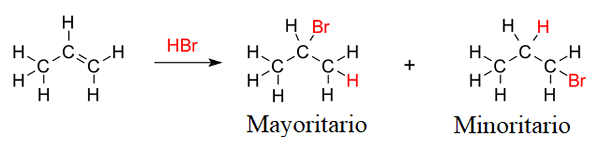 Uppskattning av Markovnikov -regeln i hydrohalogeneringen av propen. Källa: V8Rik, CC BY-SA 3.0, via Wikimedia Commons
Uppskattning av Markovnikov -regeln i hydrohalogeneringen av propen. Källa: V8Rik, CC BY-SA 3.0, via Wikimedia Commons Anta till exempel hydrobromationen av propen eller propylen (överlägsen bild). Markovnikovs regel förutspår att majoritetsprodukten kommer att vara den där bromatomen är kopplad till centrumets kol; När du är i den mindre produkten hamnar bromen till dubbelbindningen kol.
Observera att majoritetsprodukten har väteatomen kopplad till terminal kol. Denna sista punkt är den enklaste att memorera: HX-väte går till kolbindningen som har mer väte- eller C-H-bindningar.
Principer för den Markovnikov -regel
Elektrofil tillägg
Till dubbelbindningarna av alkener eller alkiner. HX har en dålig elektronatom, som är H, och en atom som är rik på elektroner, vilket är x.
Därför kan Hx representeras som hΔ+-XΔ-, är regionen hΔ+ mottaglig för att ta emot elektroner av, i detta fall, dubbelbindning av en alken, som äger rum den elektrofylattacken (se bild nedan).
Kan tjäna dig: fenylättiksyra: struktur, egenskaper, användningar, effekterCarbocation Stability
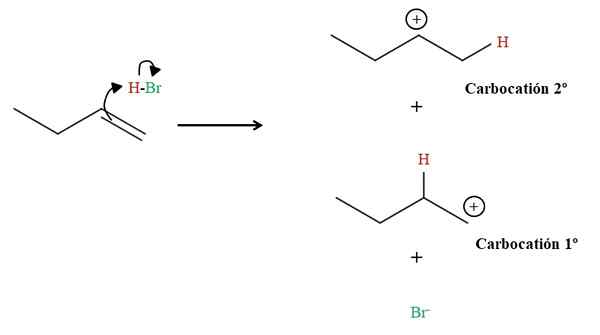
 Bildning av de två Carbocations i Hidrobromation av 1-buten. Källa: Gabriel Bolívar via Molview.
Bildning av de två Carbocations i Hidrobromation av 1-buten. Källa: Gabriel Bolívar via Molview. Som kan ses ovan attackerar 1-buten dubbelbindningen HBO-väte. På så sätt "öppnar elektronerna i H-BR-bindningen" mot bromatomen och bildar en Carbococation och anjonen BR-. Det finns emellertid möjligheten att bilda två karbocationer: en primär (1: a) och den andra sekundären (2: a).
Varje Carbocation är en mellanliggande förening från vilken slutprodukten kommer att härleda. När det finns två carbocations kommer vi då att ha två produkter: 2-bromobutano och 1-bromobutano. Br- Det fungerar som en nukleofil som attackerar någon av de två karbocationerna:
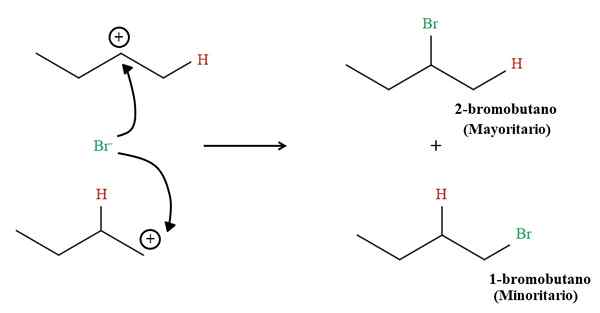 1-buten hydrobromationsprodukter. Källa: Gabriel Bolívar via Molview.
1-buten hydrobromationsprodukter. Källa: Gabriel Bolívar via Molview. Men andelen av båda produkterna är inte 50%; 2-bromobutano förekommer mycket större än 1-bromobutanen.
Anledningen är att 2: a Carbocation är mer stabil än 1: a Carbocation, eftersom dess positiva belastning är bättre stabiliserad av angränsande kolatomer; I Carbocation 1 bidrar inte väteatomen nästan någon elektronisk densitet till den positiva belastningen (vara för induktion eller hyperkonjugering).
De rika blir rikare
Markovnikovs regel föddes från de slutliga observationerna, och från dem kan de som illustreras ovan övervägas för att förklara dem.
Utan att behöva fånga dessa mekanismer, eller dra av stabiliteten i mellanhandskårdar, används den enkla regeln: I ett elektrofilt tillägg riktas väteatomer mot det dubbla kolet med dubbla med mer väteatomer. Således blir det mest hydrerade kolet ännu mer hydrerat.
Kan tjäna dig: vad är vattenavvikelser?Å andra sidan slutar atomen X, i detta fall BR, i koldioxidbindningen som har fler C-C-bindningar, eller som mer ersätts av andra atomer som inte är väte. För i 1-buten är dess terminala kol = Cho2, Det här är den som får väte för att förvandlas till -ch -gruppen3.
Exempel
Fallet med Markovnikov -regeln som tillämpades i hydrobromationsreaktionen sågs ovan. Det är också giltigt för hydrokloklinering, hydroidation, hydroaminering och hydreringsreaktioner, antingen för alkener eller alkiner.
I följande avsnitt kommer några ytterligare exempel att ses som en övningar.
Löst övningar
Övning 1
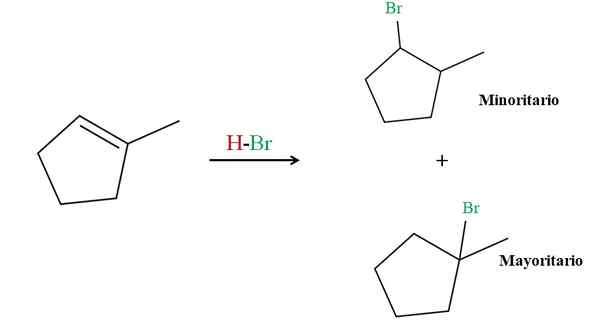 Hydrobromation av 2-metylciclopenten. Källa: Gabriel Bolívar via Molview.
Hydrobromation av 2-metylciclopenten. Källa: Gabriel Bolívar via Molview. Markovnikovs regel säger att HBR H för den övre reaktionen måste gå till dubbelbindningskolet med mer väteatomer. I det här fallet motsvarar det kolet ovan, eftersom kolet till höger, kopplat till Cho3, Det har inte ens väteatomer.
Således går HBR -väte till kolet ovan, medan BR hamnar kopplat till kol till höger (majoritetsprodukt). Å andra sidan, om väte är kopplat till kolet till höger, riktas BR till kolet ovan (mindre produkt).
Observera att majoritetsprodukten består av en tredje halogenid, mer stabil efter definition och stabiliseringseffekter av partiella positiva belastningar; Medan minoritetsprodukten är en 2: a, mindre stabil halogenid.
Båda produkterna, majoriteten och de mindre. Denna typ av minoritetsprodukt, mot Markovnikov -regeln, är känd som Antimarkovnikov -produkt.
Kan tjäna dig: Referenselektrod: Egenskaper, funktion, exempelÖvning 2
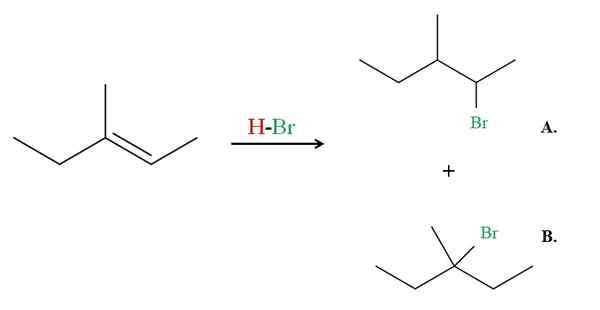 Hydrobromation av 3-metyl-2-penten. Källa: Gabriel Bolívar via Molview.
Hydrobromation av 3-metyl-2-penten. Källa: Gabriel Bolívar via Molview. Se nu exemplet med 3-metyl-2-penten.
Om det observeras har det högra kolet på dubbelbindningen en H, medan den till vänster. Därför kommer HBR: s h till det kolet, kolet måste gå till centrum för att orsaka produkt B. Produkt B är majoriteten, för återigen är det en tredje halid, produkten är en haluro 2: a.
Övning 3
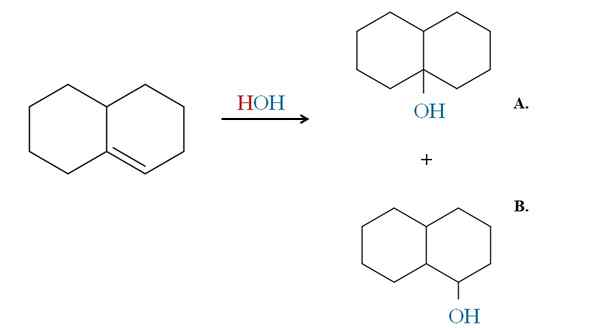 Exempel på Markovnikov -regeln vid hydrering av en cyklisk alken. Källa: Gabriel Bolívar via Molview.
Exempel på Markovnikov -regeln vid hydrering av en cyklisk alken. Källa: Gabriel Bolívar via Molview. De tidigare exemplen skulle ha genererat samma produkter om istället för HBR skulle användas HCl och HI. Detsamma är detsamma som med h2O I en hydreringsreaktion katalyserad av syra och värme. Åh kommer att ersätta HX Atom.
Därför berättar Markovnikovs regel att i det elektrofila tillägget ovan kommer OH att gå till kolet av den mest ersatta dubbelbindningen, med mindre väte.
Således är produkt A majoriteten, och produkt B minoriteten. Observera igen att produkt A är en tredje alkohol, och produkt B A 2: a alkohol.
Referenser
- Morrison, r. T. och Boyd, R, N. (1987). Organisk kemi. Femte upplagan. Redaktör Addison-Wesley Inter-American.
- Carey f. (2008). Organisk kemi. (Sjätte upplagan). MC Graw Hill.
- Graham solomons t.W., Craig b. Fryhle. (2011). Organisk kemi. (10: e upplagan.). Wiley Plus.
- Wikipedia. (2020). Markovnikovs regel. Hämtad från: i.Wikipedia.org
- Steven a. Botekar. (2017). Illustrerad ordlista för organisk kemi: Markovnikovs regel. Återhämtad från: kem.Ucla.Edu
- Gamini Gunawardena. (24 augusti 2020). Markovnikovs regel. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- Redaktörerna för Enyclopaedia Britannica. (17 september 2013). Markovnikovs regel. Återhämtat sig från: Britannica.com
- Doktor. S. Gevorg. (2020). Organisk kemi: Markovnikovs regel med övningsproblem. Återställt från: ChemistroySteps.com

