Haloidförsäljningsegenskaper, nomenklatur, hur bildas de, exempel

- 4078
- 955
- Johan Johansson
De haloidsalter De är binära föreningar som bildas av en metall och en icke -metall, utan något annat element. Dessa salter bildas genom neutraliseringsreaktionen mellan en hydracy -syra med en bas. Till exempel: reaktionen mellan saltsyra (HCl) med natriumhydroxid (NaOH) för att bilda natriumklorid (NaCl).
Haloidala salter bildas också av reaktionen av en hydracy med en metall. Till exempel: magnesiumreaktionen med saltsyra för att bilda magnesiumklorid (MGCL2). Som man ser är klorider de mest representativa haloidsalterna. Men de är inte de enda.
 Halita, natriumklorid i sitt naturliga tillstånd, är det huvudsakliga exemplet på ett haloidsalt. Källa: http: // GL.Wikipedia.org/w/index.Php?Titel = användare: Shinichi / allmän domän
Halita, natriumklorid i sitt naturliga tillstånd, är det huvudsakliga exemplet på ett haloidsalt. Källa: http: // GL.Wikipedia.org/w/index.Php?Titel = användare: Shinichi / allmän domän Haloidsalter förstår enligt vissa definitioner de föreningar de innehåller i sin halogenstruktur; Det vill säga: fluor, klor, brom och jod, så de anses synonyma med halider eller halogenuros.
På samma sätt inkluderas inom haloidsalterna, av vissa författare, föreningar som bildas av föreningen av en metall med ett element som använder dess negativa valens, inklusive: karbider, nitrider, fosfuros, sulfider, seleniuros, arseniuros, etc. Dessa räknas också som haloidsalter när de består av två element bara.
[TOC]
Haloidförsäljningsegenskaper
Haloidsalter är en grupp föreningar vars egenskaper är svåra att fastställa.
Starka jonlänkar
I allmänhet består de av fasta ämnen med starka jonbindningar mellan joner av två element: M+X-, där m+ motsvarar den metalliska katjonen och x- anjonen härrörande från icke -metall.
Höga smältpunkter, kokning och sublimering
De har vanligtvis mycket hög fusion, kokning och sublimeringspunkter, precis på grund av kraften i dess kristallina struktur.
Det kan tjäna dig: DAPI (4 ', 6-diamidino-2-fenylindol): Egenskaper, grund, användningElledning
I fast tillstånd är de dåliga ledare av elektricitet, men i vattenlösning när de joniserar, eller när de smälter samman, blir bra förare.
Utseende
De är kristallina fasta ämnen som när fragmenterat pulveriserat kan bli en vit färg. Många haloidsalter kan dock ha en annan färg. Till exempel är nickelklorid grön, medan järnklorid har en oscillerande färg mellan grönt och rött.
Löslighet
Majoriteten av haluros -salter är lösliga i vatten, med undantag för silver, bly (II) och kvicksilverhalider (I).
Lukt
Eftersom de inte är flyktiga föreningar utgör haloidsalter inte stark lukt. På grund av deras sammansättning kan de också vara av sur, salt, bittera eller söta smaker.
Nomenklatur
Haloidsalterna namnges genom att placera namnet på anjonen med suffixet uroxe, följt av namnet på metallen direkt, föregås av konjunktionen av. I händelse av att metallen har mer än en valens placeras metallen med suffixet björn eller ICO, Beroende på hans Valencia.
Namnet på metallen kan också placeras utan suffix och med antalet oxidation inom parentes.
Till exempel: järnklorid (III) eller järnklorid, FECL3.
Hur bildas haloidsalter?
Haloidsalter bildas huvudsakligen av tre reaktioner: neutralisering, syrareaktion med en metall och reaktionen av en metall med en metall eller en icke -metallverkande med en negativ valens.
Neutraliseringsreaktion
Det är reaktionen av en syra med en bas, producerar salt och en vattenmolekyl. Till exempel:
HCl +NaOH → NaCl +H2ANTINGEN
Detta exempel nämndes för prinsen.
Reaktion av en syra med en metall
En stark syra kan reagera med en metall, med ursprung i ett salt och frisättning av väte (h2). Till exempel: saltsyra reagerar med zink (Zn) för att bilda zinkklorid (ZnCl2):
Kan tjäna dig: analytisk kemiZn +HCl → ZnCl2 + H2
Kombination av en metall med en metall eller en icke -metall
Dessa haloidsalter är resultatet av kombinationen av en metall med en metall eller en icke -metall från halogener. Till exempel: Aluminiumfosfuro kombinerar fosfor med Valencia -3, med aluminium med Valencia +3. Nu beror denna "kombination" på specifika produktionsreaktioner för varje salt.
Användning/applikationer
Halogenuro
Metallhalogenuros används i lampor med hög intensitet, såsom moderna lampor. De används också i växthus eller regnklimat för att komplettera naturligt ljus. Silverhalider används i filmer och fotografiska papper.
Kalciumklorid
 Utseende av kalciumklorid
Utseende av kalciumklorid Kalciumklorid används som en kalciumkälla vid avloppsrening. Det används också som en kalciumkälla genom dess elektrolys. Det används vid behandling av hjärtarytmier och i fall av svår hypokalcemi.
Järnklorid
Järnklorid används vid avloppsrening och vattenrening. Det används också för att spela in eller välja koppar och ingripa som en katalysator i syntesprocessen av vinylklorid.
Klorid och kaliumbromid
Kaliumklorid används som gödningsmedel och vid behandling av hypokalemi eller hypokalemi. Kaliumbromid, å andra sidan, användes som antikonvulsiv och används för närvarande inom läkemedelsindustrin och som en förband.
Klorid och natriumsulfid
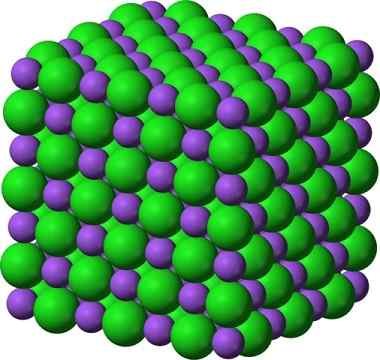
 Den kristallina strukturen hos natriumklorid, NaCl, en typisk jonisk förening. De __ lila sfärerna representerar natriumkatjoner, Na +, och __gröna sfärer representerar Ancies -klorid, Cl−.
Den kristallina strukturen hos natriumklorid, NaCl, en typisk jonisk förening. De __ lila sfärerna representerar natriumkatjoner, Na +, och __gröna sfärer representerar Ancies -klorid, Cl−. Natriumklorid används som en matsmak, i bevarande av kött, som ett antiseptiskt, i svår hyponatremi, etc. Natriumsulfid används i kärnreaktorer i tung vattenproduktion, vid eliminering av skinnhår och i tillverkning av gummi, färgämnen och målningar.
Kan tjäna dig: aluminiumoxid: struktur, egenskaper, användningar, nomenklaturFosfuros och nituro
Aluminiumfosfuro används som en bredbands halvledare och som en insekticid. Under tiden används Gallium nitruro som halvledare.
Exempel på haloidsalter
Bortsett från exemplen som nämns i föregående avsnitt, andra haloidsalter med sina respektive formler och namn:
-NaCl: natriumklorid
-KCL: Kaliumklorid
-CaCl2: Kalciumklorid
-Mgcl2: Magnesiumklorid
-CSCL: Cesiumklorid
-Bacl2: Bariumklorid
-Fecl2: Järnklorid
-Fecl3: Järnklorid
-Nick2: Nickelklorure
-CUCL: Kuprousklorid
-CuCl2: Cupric klorid
-AGCL: Silverklorid
-Zncl2: Zinkklorid
-CDCL2: Kadmiumklorid
-Hgcl2: Kvicksilverklorid
-Alcl3: Aluminiumklorid
-NABR: natriumbromid
-KBR: Kaliumbromid
-CSBR: cesiumbromid
-CDBR: Kadmiumbromid
-Mgbr2: Magnesiumbromid
-Srbr2: Strontium Bromide (II)
-KI: kalium yoduro
-NAI: natriumjodid
-CSI: Cesium Yoduro
-Ali3: Aluminiumjodid
-Bal2: Blyjodid (ii)
-NAF: natriumfluorid
-LIF: Litiumfluorid
-Kaf2: Kalciumfluorid
-Ptf2: Platinfluorid (ii)
-Nas2: Natriumsulfid
-Li4C: litiumkarbid
-Mg2C: magnesiumkarbid
-ALP: aluminiumfosfuro
-Ja3N4: Kisel nitruro
-Tin: Titanium nitruro
Referenser
- Shiver & Atkins. (2008). Oorganisk kemi. (fjärde upplagan). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Julián Pérez Porto och María Merino. (2016). Definition av haloidsalter. Definition.av. Återhämtad från: definition.av
- James P. Björk. (5 juni 2019). Halide Ins. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- Wikipedia. (2020). Halogenid. Hämtad från: i.Wikipedia.org
- « Peroxides egenskaper, nomenklatur, användning, exempel
- Termohigometeregenskaper, funktioner, delar, användningar »

