Transaminering
- 4690
- 24
- PhD. Lennart Johansson
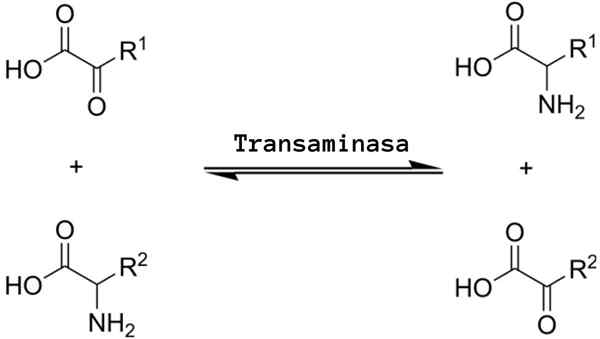 Schema för en aminotransferensreaktion mellan en aminosyra och en alfa-zoacid (källa: Alcibiades via Wikimedia Commons)
Schema för en aminotransferensreaktion mellan en aminosyra och en alfa-zoacid (källa: Alcibiades via Wikimedia Commons) Vad är transaminering?
De transaminering Det är en typ av kemisk reaktion som fungerar i "omfördelningen" av aminosyragrupperna, eftersom den omger reversibla amineringsprocesser (tillsats av en aminogrupp) och hjärtskador (eliminering av en aminogrupp), som katalyseras av specifika enzymer känd som transaminaser eller aminotransferaser.
Den allmänna transaminationsreaktionen innebär utbytet mellan en aminosyra och varje a-ZO-Stoat, där utbytet av ett aminogrupp ger ketoacidversionen av det första substratets aminosyran och aminosyrasversionen av den första a-Zo-Ecotoacid-substratet.
Amino -gruppen som vanligtvis byts ut är amino "alfa", det vill säga den som deltar i bildningen av peptidlänkarna och som definierar strukturen hos aminosyrorna, även om reaktioner som involverar andra aminogrupper närvarande i olika positioner i olika positioner kan förekomma i.
Med undantag av lysin, treonin, prolin och hydroxiprolin deltar alla aminosyror i transaminationsreaktioner, även om för histidin, serin, metod och fenylalanin har beskrivits transaminaser, men deras metaboliska vägar innebär inte denna typ av reaktioner.
Transaminationsreaktionerna mellan aminosyror och a-cetoacider upptäcktes 1937 av Braunstein och Kritzmann, och sedan dess har de varit föremål för intensiva studier, sedan de förekommer i många tyger av olika organismer och med olika ändamål.
Hos människor, till exempel, är transaminaser allmänt fördelade i kroppsvävnader och är särskilt aktiva i hjärtmuskelvävnad, i levern, i skelettmuskelvävnad och i njurarna.
Reaktionsmekanism
Transaminationsreaktioner innebär mer eller mindre samma mekanism. Som nämnts ovan förekommer dessa reaktioner som ett reversibelt utbyte av en aminogrupp mellan en aminosyra och en a-ZO-CID.
Kan tjäna dig: keramiska material: egenskaper, typer, exempelDessa reaktioner beror på en förening känd som fosfatpyridoxal, ett derivat av vitamin B6 som deltar som en amino-grupptransportör och som binder till transaminasenzymer genom bildandet av en schiffbas mellan aldehydruppen i detta molekyl och ε-amino av ett lysinrest på enzymets aktiva ställe.
Föreningen mellan fosfatpyridoxala och lysinresten på det aktiva stället är inte kovalent, men ges genom elektrostatisk interaktion mellan den positiva kvävebelastningen i lysin och den negativa belastningen i fosfatgruppen i pyridoxal.
Under reaktionen förskjuter aminosyran som fungerar som ett substrat ε-amino-gruppen för lysinresten på den aktiva platsen som deltar i Schiff-basen med pyridoxal.
Samtidigt avlägsnas ett par aminosyras alfa-kolelektroner och överförs till pyridinringen som komponerar fosfatpyridoxal (med en positiv laddning) och sedan "levereras" till a-zo-zid som fungerar som ett andra substrat.
På detta sätt deltar det pyridoxala fosfatet inte bara i överföringen eller transporten av aminosyrorna mellan aminosyrorna och a-ekotoaciderna som är substrat för transaminaser, utan också fungerar som ett "sjunkande" av elektroner, underlättar dissociationen av alfa -syran väte.
Sammanfattningsvis överför det första substratet, en aminosyra, sin aminogrupp till fosfatpyridoxal, varifrån den därefter överförs till det andra substratet, en a-zo-ekotoid, bildning, i mellanprodukten, en mellanliggande förening känd som pyridoxamin fosfat.
Kan tjäna dig: kolumnkromatografiTransaminationsfunktion
Transaminasenzymer finns vanligtvis i cytosol och mitokondrier och arbetar i integrationen av olika metaboliska rutter.
Glutamatdehydrogenas i sin omvända reaktion, till exempel, kan förvandla glutamat till ammonium, NADH (eller NADPH) och a-zetoglutarat, som kan komma in i cykeln för tricarboxylsyror och funktion i energiproduktion.
Detta enzym, som är i mitokondriell matris, representerar en grenpunkt som associerar aminosyror med energimetabolism, så att när en cell saknar tillräcklig energi i form av kolhydrater eller fetter för att fungera, kan den växelvis använda vissa aminosyror för samma sak syfte.
Bildningen av enzymet (glutamatdehydrogenas) under hjärnutveckling är avgörande för kontrollen av ammoniumavgiftning, eftersom det har visats att vissa fall av mental retardation har att göra med en låg aktivitet av detta, vilket leder till ackumulering av ammonium, vilket är skadligt för hjärnhälsa.
I vissa leverceller kan transaminationsreaktioner också användas för glukoneogenesis glukossyntes.
Glutamin omvandlas till glutamat och ammonium av glutaminasenzym. Sedan omvandlas glutamat till a-zetoglutarat, som kommer in i Krebs-cykeln och sedan till glukoneogenes. Detta sista steg inträffar tack vare Malo, en av produkterna på rutten, transporteras utanför mitokondrierna med hjälp av en skyttel.
Denna skyttel lämnar a-cethoglutarate över Málica-enzymets nåd, vilket gör att den pyruvat. Två pyruvatmolekyler kan omvandlas, då en glukosmolekyl genom glukoneogenes.
Kan tjäna dig: platt bakgrundskolvExempel
De vanligaste transaminationsreaktionerna är relaterade till alaninaminosyror, glutaminsyra och aspartinsyra.
Vissa aminotransferasenzymer kan, utöver pyridoxalt fosfat, använda pyruvat som "koenzym", som är fallet med transaminas glutamat-piruvat, som katalyserar följande reaktion:
glutamat + pyruvat ↔ alanin + a-cetoglutarat
Muskelceller beror på denna reaktion för att producera alanin från pyruvat och för att få energi genom Krebs-cykeln med hjälp av a-zetoglutorat. I dessa celler beror användningen av alanin som en energikälla på eliminering av aminogrupper som ammoniumjoner i levern, genom ureacykeln.
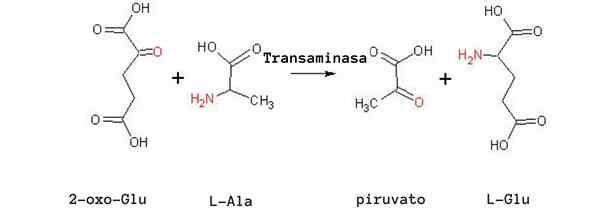 Alanintransamineringsreaktion (källa: Tomas Drab [Public Domain] via Wikimedia Commons)
Alanintransamineringsreaktion (källa: Tomas Drab [Public Domain] via Wikimedia Commons) En annan mycket viktig transaminationsreaktion hos olika arter är den katalyserade av enzymets aspartataminotransferas:
L-spartato + a-ketoglutarat ↔ oxalacetat + l-glutamat
Slutligen, men inte minst, y-aminobutyric acid transamination reaktion (GABA), en icke-proteinaminosyra för det centrala nervsystemet som fungerar som en hämmande neurotransmitter. Reaktionen katalyseras av en y-aminobutirisk transaminasyra och är mer eller mindre enligt följande:
a-ketoglutarat + 4-aminobutansyra ↔ Glutamat + suwcinic semi-bil
Succinic semi -Semi -användningen omvandlas till suwcinic acid genom en oxidationsreaktion och den senare kan komma in i Krebs -cykeln för energiproduktion.

