Aluminiumoxidstruktur, egenskaper, användning, nomenklatur
- 3619
- 603
- Hans Olsson
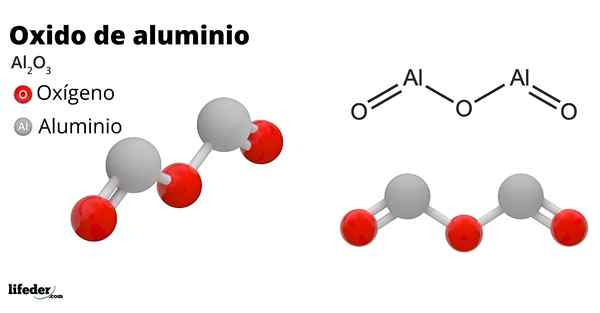
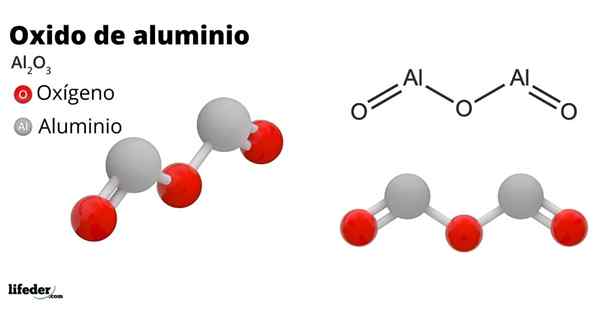
han aluminiumoxid, Även kallad aluminiumoxid, aluminiumoxid, Corindon eller aluminiumtrioxid, det är en oorganisk förening vars kemiska formel är till2ANTINGEN3. Det är en amphotero -oxid, även om den på grund av behandling kan bli en nästan inert förening.
Det har stor hårdhet, korrosionsmotstånd och hög elektrisk motstånd. Dessa egenskaper har bland annat tillåtit aluminiumoxid att ha många tillämpningar, såsom: elektrisk isolering, slipmaterial, ben- och tänderimplantat etc.
Bauxit är den viktigaste källan för att erhålla aluminiumoxid. Corindon är å andra sidan ett mineral av aluminiumoxid som är i fritt tillstånd i form av a-al2ANTINGEN3. Corindon har en hårdhet på 9.0, och på grund av vissa föroreningar producerar det ädelstenar, som Sapphire och Ruby.
Aluminiumoxidelektrolys tjänade som grund för aluminiumisolering av Humphry Davy 1808. Samma metod, med vissa anpassningar, används för närvarande i metallisk aluminiumproduktion.
[TOC]
Strukturera
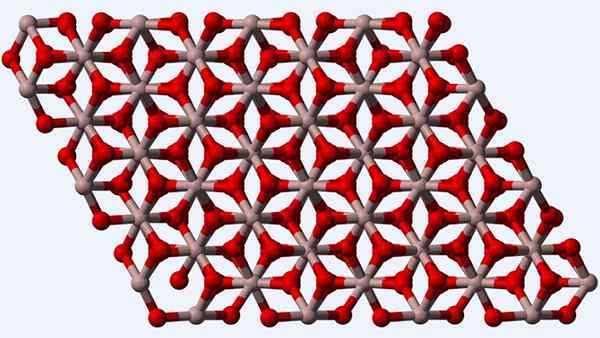 Kristallin struktur i a-Al2O3- eller Corindon-fasen
Kristallin struktur i a-Al2O3- eller Corindon-fasen Corindon eller a-al-fasen2ANTINGEN3, Eftersom det är termodynamiskt mer stabilt polymorf för aluminiumoxid, betraktas dess struktur (överlägsen bild) som den viktigaste vid tidpunkten för dess karaktärisering. Denna struktur är trigonal, med jonerna till3+ omgiven av sex eller2-, och därför etablera octaedros al6 med interaktioner al-o u al-o.
Förutom Corindón, Al2ANTINGEN3 Det finns också som andra metastabla polymorfer, inklusive: y-Al2ANTINGEN3 och η-al2ANTINGEN3 (kubik), θ-at2ANTINGEN3 (monoklinisk), χ-Al2ANTINGEN3 (hexagonal), κ-al2ANTINGEN3 (Ortorrombisk) och 5-al2ANTINGEN3 (Tetragonal eller ortorrombisk).
Som Al2ANTINGEN3, Octahedraen är "bryter" i tetrahedros al4 o Pentaedros alo5. När du har smält och sval igen kan du få en glasögonalumid, det vill säga amorf, med blandningar av Polyhedra ALM5 och alla6.
Det kan tjäna dig: Einstenio (er): Struktur, egenskaper, erhållning, användningAluminiumoxidegenskaper
 Aluminiumoxidbeläggning smält metall aluminiumstycken
Aluminiumoxidbeläggning smält metall aluminiumstycken Fysiskt utseende
Fast eller vitt kristallint pulver
Molmassa
101.96 g/mol
Lukt
Toalett
Densitet
3.798 g/cm3
Smältpunkt
2072 ºC
Kokpunkt
2977 ºC
Löslighet
Olöslig i alla lösningsmedel, inklusive vatten.
Värmeledningsförmåga
30 W · m-1· K-1. Trots dess keramiska användning har den en relativt hög värmeledningsförmåga.
Brytningsindex
1.768-1.760
Hårdhet
Det är en förening som ger en mycket hög hårdhet, med ett värde av 9.0 på Mohs hårdhetsskala i form av a-aluminiumoxid (Corindón).
Elektrisk resistans
Vid 300 ° C: 1.2 x 1013 Ohm · cm. Aluminium eller aluminiumoxidoxid är därför en elektrisk isolator.
Reaktivitet
AL2ANTINGEN3 Trots att de reagerar svagt med alkalier och i större utsträckning med syror anses det vara en kemisk amphoter. Men när det värms upp vid mer än 800 ° C förvärvar det ett nästan inert tillstånd till verkan av syror.
Denna oxid är ansvarig för att skydda aluminium framför miljömässiga medelmodern, eftersom den täcker mätningen av metallen utan smulor eller sprickor.
Nomenklatur
Nomenklaturen för Al2ANTINGEN3 det är enkelt. Systematiskt känd som diauminiumtrioxid. Eftersom denna aluminiumoxid finns, i dess lager nomenklatur anges inte metall valencia (iii). Dessutom är namnet traditionellt sammanfattat till aluminiumoxid genom att bara ha en valens.
Användning/applikationer
Glas
Aluminiumoxid ingriper i utarbetandet av aluminium-silikatlas. Detta eldfasta glas, resistent mot termisk chock, kan användas vid högre temperaturer än bor-silikatglas; Även om det har lägre kemisk resistens.
Tillsatsen av en liten mängd magnesia förvandlar det ogenomskinliga glaset till genomskinligt, att kunna användas som en gasbehållare i natriumånglampor med högt tryck. Det används också vid beredning av beläggningsupphängningar av vissa typer av lysrörslampor.
Kan tjäna dig: Rodio: Historia, egenskaper, struktur, användningar, riskKatalysator
Aktiverad aluminiumoxid har en granulär och porös egenskap som kan ha katalytisk aktivitet, eller tjäna som ett stöd för aktiviteten hos andra katalysatorer. Bland andra processer ingriper aluminiumoxid i katalysen av polymerisation av etenoxid.
Mikrobicidaktivitet
Nano-aluminiumoxidpartiklar följer ytan på bakterier och orsakar deras död. På samma sätt har en liknande effekt på svampen i Candida släkte bevisats.
Elisolator
Aluminiumoxid har en hög elektrisk resistivitet, vilket ger den förmågan att fungera som en elektrisk isolator. Därför används det i integrerade kretspaket. Det används också i superledarenheter och som dielektrisk kondensor eller kondensatorer. Dessutom används den som en isolator i elektriska tändstift.
Skrovlig
 Corindon, den kristallina och tuffare av aluminiumoxid, tjänar till att bygga slipverktyg. Källa: Rob Lavinsky, irocks.com-cc-by-sa-3.0, CC BY-SA 3.0, via Wikimedia Commons
Corindon, den kristallina och tuffare av aluminiumoxid, tjänar till att bygga slipverktyg. Källa: Rob Lavinsky, irocks.com-cc-by-sa-3.0, CC BY-SA 3.0, via Wikimedia Commons Den höga hårdheten hos Corindon Mineral tillåter det att användas som slipmedel, mindre kostnad än diamanter, inom industrin och i oljeborrning.
Corindon förvärvar den ädelstenformen, till exempel den röda rubinen, på grund av kromföroreningar; eller som blå safir, på grund av förorening av järn och titan. Många typer av sandpapper som används i metall och trä har aluminiumoxidkristaller.
Uthållighet eller förmåga att undvika brottet av aluminiumoxid ökar med tillsats av zirkoniume eller kiselkarbid, vilket gör att den kan användas i industriella verktyg för skärning. Dessutom används aluminiumoxid i tandkräm för tänderpolering.
Kan tjäna dig: zinkkromat: struktur, egenskaper, erhållning, användningVissa presentationer av aluminiumoxid används också som slipmedel av hudläkare vid behandling av vissa hudtillstånd.
Gasavfuktare
Aluminiumoxid är en förening med ivrig med vatten, så den kan användas för att extrahera den från gasformiga strömmar.
Brand säkert
Nano-partiklarna i aluminiumoxidhydroxid (Bohemita) fungerar som en värmedissipator, släpper vatten och försenar utseendet på lågor.
Hårdvävnadsimplantat
Aluminiumoxid är en förening av stor hårdhet, kemiskt inert och korrosionsbeständig, förutom att ha en vit färg. För dessa egenskaper används det som en ersättning för hårda vävnader som ben och tänder. På samma sätt har materialet byggt med aluminiumoxid använts vid ledbyte.
Erhållande
 Bauxitprov. Källa: Max.Kit, CC BY-SA 4.0, via Wikimedia Commons
Bauxitprov. Källa: Max.Kit, CC BY-SA 4.0, via Wikimedia Commons Bauxiten är det viktigaste mineralet för att erhålla aluminiumoxid, som bildas av blandningen av tre mineraler: Gibbsite, Laboehmita och Diaspora.
Aluminiumoxid extraheras från dess mineraler genom Bayer -proceduren. Detta består av den heta bauxitreaktionen med natriumhydroxid, en reaktion producerad av natriumaluminat [NAAL (OH)4].
När den tidigare lösningen kyls produceras utfällning av aluminiumhydroxid i fast form. Sedan värms denna hydroxid fram till 1100 ° C, vilket producerar aluminiumoxid.
Referenser
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan.). Cengage Learning.
- Shiver & Atkins. (2008). Oorganisk kemi. (Fjärde upplagan). MC Graw Hill.
- Wikipedia. (2020). Oxidaluminium. Hämtad från: i.Wikipedia.org
- Nationellt centrum för bioteknikinformation. (2020). Oxidaluminium. PubChem Comunund -sammanfattning för CID 9989226. Återhämtat sig från: pubchem.Ncbi.Nlm.Nih.Gov
- Kushagri s. et al. (2019). Antiviral och antimikrobiell potential hos nano -läkemedel: nanopartikelaluminiumoxid. Hämtad från: Scientedirect.com
- Redaktörerna för Enyclopaedia Britannica. (2020). Aluminiumoxid. Återhämtat sig från: Britannica.com
- Lohninger Hans. (15 augusti 2020). Oxidaluminium. Kemi librettexts. Återhämtad från: kem.Librettexts.org
- « Aromatisk elektrofil substitutionsmekanism och exempel
- 30 exempel på etik och moral i det dagliga livet »

