Grundelektrofores, teknik, vad är det för, exempel

- 4439
- 1217
- Anders Svensson
De Elektrofores Det är en teknik som används för att separera molekyler i ett elektriskt fält. Det måste göra specifikt med migrationen av partiklar laddade under påverkan av en elektrisk ström som appliceras mellan två poler, en positiv och en annan negativ.
Elektrofores är för närvarande en av de mest rutinmässiga procedurerna som äger rum under utvecklingen av ett experiment, särskilt inom områden relaterade till analytisk kemi, biokemi och biologiska och medicinska vetenskaper i allmänhet.
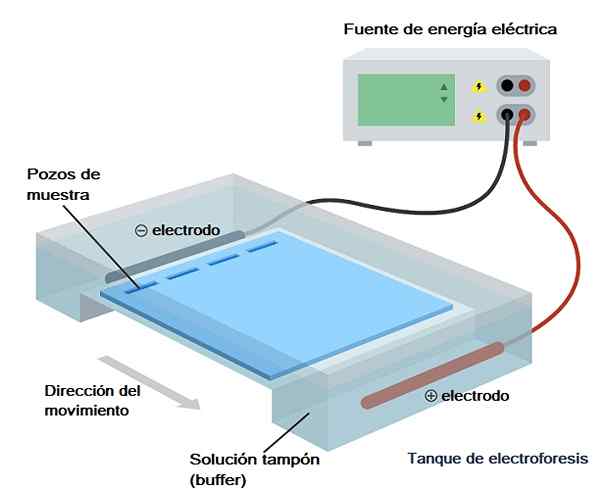
 Elektroforeshink. Källa: Melodygar/CC BY-SA (https: // CreativeCommons.Org/licenser/BY-SA/4.0)
Elektroforeshink. Källa: Melodygar/CC BY-SA (https: // CreativeCommons.Org/licenser/BY-SA/4.0) Det används för att separera protein, peptider, DNA, RNA och andra enligt deras belastning, storlek, densitet och renhet.
De olika kommersiella husen har utformat olika format, med olika applikationer och lämpliga vinster för specifika ändamål, men alla procedurer kräver samma grundelement:
- En energikälla för att generera elektrisk laddning
- Ett medium för stöd för separation
- En buffertlösning (buffert) För att hålla pH -konstanten
[TOC]
Grund
Elektrofores är inget annat än migrationen (separationen) av partiklar eller laddade molekyler (naturligt eller konstgjort) i ett medium eller stöd under påverkan av ett elektriskt fält.
Tekniken är baserad på en av de viktigaste fysiska ekvationerna för elektromagnetism, enligt vilken kraften är lika med den elektriska laddningen multiplicerad av det elektriska fältet som appliceras vid den punkten (F (kraft) = Q (elektrisk laddning) X E (elektriskt fält ).
Enligt denna ekvation kommer två partiklar med samma massa, men med olika belastningar, att flytta till olika hastigheter i samma elektriska fält. Dessutom kommer rörelsens hastighet för dessa partiklar att bero på förhållandet mellan deras belastning och deras massa.
Forskare har utnyttjat dessa egenskaper och last/massförhållanden för att separera komponenterna från biomolekyler i sina minsta delar, samt för att separera olika molekyler i en blandning, bland andra tillämpningar.
Det är viktigt att komma ihåg att biologiska molekyler såsom aminosyror, peptider, proteiner, vissa kolhydrater, nukleotider och nukleinsyror alla har något som vi kallar "joniserbara grupper", så att de kan existera som positiva eller negativt laddade arter under vissa pH -förhållanden.
Metod
Även om det finns olika typer av elektrofores, är gelelektrofores den mest använda i biokemisk analys, molekylärbiologi och bioteknik, så det kommer att vara vad vi kommer att prata om kort i tekniska termer.
Som namnet antyder innebär gelelektrofores användning av ett fast format fast stödmedium, antingen för analys/separering av blandningar av protein eller nukleinsyror (DNA och/eller RNA) under påverkan av ett elektriskt fält.
Systemet eller apparaten som används för att utföra en elektroforetisk "körning" kan vara horisontellt (vanligtvis används för nukleinsyror) eller vertikalt (vanligtvis används för protein).
- Exempel på nukleinsyranelektrofores -tekniken
Nukleinsyror separeras vanligtvis med användning av agarosgeler (galaktospolysackarid) som framställs med en adekvat buffertlösning (Tris/acetat/EDTA eller Tris/Borato/EDTA) och vars koncentration kommer att bestämma "upplösningen" av fragment av olika storlekar.
Kan tjäna dig: Jordens livsmedelskedja: Länkar och exempelProvberedning
Det första steget innan du utför en elektroforetisk körning i en agarosgel är att få provet. Detta kommer att bero på det experimentella änden och proverna kan vara produkten av en enzymatisk matsmältning, på en polymeraskedjereaktion (PCR), en rening av nukleinsyror etc.
 Blandning av provet med lastbuffen.Org/licenser/av/4.0) via Wikimedia Commons)
Blandning av provet med lastbuffen.Org/licenser/av/4.0) via Wikimedia Commons) Efter erhållet blandas detta med en färgad lösning (lastlösning) som möjliggör snabb avsättning av provet i en brunn, eftersom det har glycerol och ett färgämne som tillåter körningen visuellt.
Gelförberedelse
Detta steg består i att blanda den nödvändiga mängden av gelningsunderlaget (agarosen) med buffertlösningen, smälta den med värme och stelna den på ett stöd som fungerar som "mögel".
Under gelifieringen introduceras några "kammar" i gelén placerad i "mögel" för att avgränsa "brunnarna" där proverna kommer att introduceras före körningen.
När gelén har svalnat och stelnat avlägsnas "kammarna" och den införs i en behållare som kallas "hink", som är full av löpande buffertlösning, (Tris/acetate/EDTA eller Tris/Borato/Borato/EDTA).
Denna hink ingår i sin tur i det som kallas ”elektroforetiska kammaren”, som inte är något annat än behållaren genom vilken det elektriska fältet passeras och som har ett utrymme där gelén introduceras och två sektioner som de är fyllda med buffert-lösning (buffert springa).
Denna kamera har två elektroder, en positiv och en negativ, bland vilken jonrörelsen produceras efter applicering av ett elektriskt fält (den är ansluten till en kraftkälla).
Laddningsprover
När proverna har blandats med respektive lastlösning introduceras dessa i de "brunnarna" som tidigare gjorts i gelén.
Eftersom nukleinsyror har en negativ nätbelastning migrerar de från den negativa polen till det positiva, så detta måste beaktas när kameran är ansluten till kraftkällan, vilket säkerställer att den negativa polen motsvarar den mest platsen bredvid platsen där proverna laddades.
Corida -tiden upprättas i strikt beroende av forskaren som ansvarar för experimentet. Spänningen beräknas vanligtvis i ett 5 -volymförhållande per centimeter i gelén som skiljer de två elektroderna.
Visa
När gelén rinner (när proverna har rest gelén från ena änden till den andra) är den nedsänkt i en lösning av etidbromid (ETBR), ett färgämne som är isär mellan kvävehalten och att "varumärket", så De kan visualiseras i en transilumenant med ultraviolett ljus.
Vad är elektrofores för?
Elektrofores har historiskt använts med flera syften. Idag beror emellertid dess användbarhet till stor del på "frågan" som forskaren ställs i förhållande till ett fenomen eller ett visst system, liksom den typ av elektrofores som han vill använda.
Kan tjäna dig: topoisomeras: vad är, egenskaper, funktioner, typerVi kan emellertid få några av de viktigaste funktionerna som denna teknik har, med början med det mest "sällsynta" och slutar av de mest populära och mestadels utnyttjade i biologiska vetenskaper i världen. Elektrofores är användbar:
- För den kvantitativa analysen av komplexa blandningar av makromolekyler och för beräkningen av den potentiella "zeta" (kolloidal egenskap hos en partikel i ett flytande medium under påverkan av ett statiskt elektriskt fält).
- För analys av blodsera för diagnostiska ändamål.
- För separering av glukoproteiner, lipoproteiner och blodhemoglobin.
- För livsmedelsanalys, läkemedelsprodukter och miljöföroreningar.
Elektrofores i agarosgeler
- För separering av DNA -fragment efter matsmältning med restriktionsenzymer.
- För separering av nukleinsyramolekyler före överföring till membran för efterföljande analyser.
- För analys av PCR -produkter (polymeraskedjereaktion) som verifierar om den inträffade eller inte.
- För uppskattningen av storleken på molekylerna i en blandning av DNA eller RNA.
- För uppskattning av mängden och/eller kvaliteten på renade nukleinsyror.
Elektrofores i polyakrylamidgeler under denaturerande eller infödda förhållanden
- För att bestämma storleken på ett protein.
- Att identifiera proteiner.
- För att bestämma renheten hos ett prov efter flera reningssteg.
- För att identifiera närvaron av intramolekylära disulfidlänkar.
- För att bestämma interaktionen mellan proteiner.
- För att bestämma den isoelektriska punkten för ett protein.
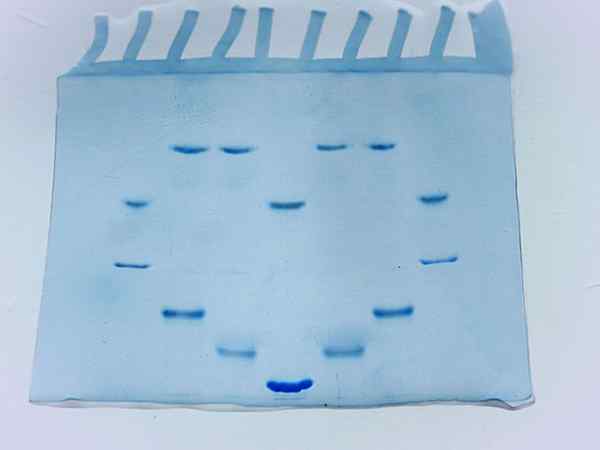 Fotografi av en akrylamidgel efter körningen av flera proteinprover (källa: Larionova.Marina/CC BY-SA (https: // CreativeCommons.Org/licenser/BY-SA/4.0) via Wikimedia Commons)
Fotografi av en akrylamidgel efter körningen av flera proteinprover (källa: Larionova.Marina/CC BY-SA (https: // CreativeCommons.Org/licenser/BY-SA/4.0) via Wikimedia Commons) Faktorer som påverkar elektrofores
Migrationen av en partikel i ett elektriskt fält beror på olika faktorer, bland vilka är:
- Din elektriska laddning
- Dess molekylstorlek
- Dess hydrofobicitet och dess form
- Storleken på det elektriska fältet som appliceras
- Systemtemperaturen och jonkraften för buffertlösningen som används
- Miljöens natur där den ligger
I förhållande till provet
Bland parametrarna relaterade till partiklar (prov) som omfattas av ett elektriskt fält har de viktigaste faktorerna som påverkar denna process att göra med deras belastning, deras storlek och form.
Ju större nettobelastning för en partikel, desto större är migrationshastigheten och denna storlek beror på pH. Förhållandet till storleken är emellertid omvänt proportionell, vilket innebär att ju mer "stora" molekylen, desto långsammare migrerar.
Det kan tjäna dig: lia agar (järnlysin): vad är, grund, förberedelse, användningI förhållande till det elektriska fältet
Hittills har vi talat om vikten av det elektriska fältet för att uppnå rörelse av en partikel genom elektrofores, men vi har inte definierat vad det är: elektrisk kraft per lastenhet eller, i enklare termer, ett område i rymden där det finns en elektrisk kraft.
Parametrarna angående det elektriska fältet som kan påverka migration är spänning, ström och motstånd.
Spänningen påverkar "flygtiden" för molekylerna som är separerade efter applicering av det elektriska fältet. Ju högre det är, desto snabbare rörelse.
De nuvarande (kontinuerliga och enhetliga elektronerna som "skjuts" av spänningskällan) utförs mellan de elektroforetiska systemelektroderna tack vare jonerna som finns i buffertlösningen. Är direkt relaterad till spänning.
I förhållande till buffertlösningen
Kompositionen, jonisk kraft och pH för buffertlösningen är de viktigaste parametrarna som påverkar en elektroforetisk "körning", eftersom de direkt påverkar några av provernas egenskaper, särskilt den elektriska laddningen.
Därför att? Buffertlösningen stabiliserar pH för stödmediet där elektrofores inträffar. Dess sammansättning kan påverka förskjutningen av migreringspartiklarna och den joniska koncentrationen också, eftersom den är direkt relaterad till strömmen.
I förhållande till stödmediet
De olika typerna och formaten för elektrofores presenterar också olika medier på vilka migration inträffar och där det därefter kan "registreras".
Migrationshastigheten för molekylerna som utsätts för elektrofores beror på typen av stödmedium, som vanligtvis bör vara inerta.
Dess absorptionsegenskaper, elektroendo-osmos är viktiga (rörelsens kapacitet för en vätska genom ett membran under påverkan av ett elektriskt fält) och dess molekylsiktkapacitet.
Exempel på användning av elektrofores
Klassiska exempel på elektroforetiska tekniker som används i biologi och bioteknik inkluderar:
- Elektrofores i agarosgeler (engelska Elektroforesgel)
- Elektrofores i akrylamidgeler vid denaturerande förhållanden (SDS-PAGE, engelska Natriumdocylsulfat polyakrylamidgelelektrofores)
- Elektrofores i akrylamidgeler under infödda förhållanden (BN-PAGE, engelska Blå nativ polyakrylamidgelelektrofores)
- Elektrofores i två dimensioner (2d-sida, från engelska Tvådimensionell polyakrylamidgelelektrofores)
- Kapillärelektrofores (från engelska Elektroforeskapillär)
- Isolektroenfoque (engelska Isolektrofokering)
- Pulserad fältelektrofores (engelska Pulserad fältelektrofores)
Referenser
- Beck, Kevin. (2020, 25 maj). Typen av elektrofores. Forskning.com. Hämtad från vetenskapen.com
- Uppsatser, Storbritannien. (November 2018). Elektroforesyper och applikationer. Hämtad från ukessays.com
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger principer för biokemi. Macmillan.
- Parmar, s. (Augusti 2018). Elektrofores: Betydelse, definition och klassificering (med diagram). Bioteknik. Hämtad från bioteknik.com
- Perrett, D. (2010). 200 års elektrofores. Kromatog. Idag 4-7.
- Righetti, s. G. (2005). Elektrofores: The March of Pennies, The March of Dimes. Journal of Chromatography A, 1079 (1-2), 24-40.
- Rilbe, h. (nittonhundranittiofem). Som påminner om elektroforeshistorien. Elektrofores, 16 (1), 1354-1359.
- Vesterberg, eller. (1993). En kort historia av elektroforetiska metoder. Elektrofores, 14 (1), 1243-1249.
- Vinayagam, m. (Inget datum). Faktorer som påverkar elektrofores. Akademi.Edu. Hämtad från akademin.Edu
- « Förklaring av kemisk balans, faktorer, typer, exempel
- Toltec Culture Ursprung, plats, egenskaper, organisation »

