Glykogenstruktur, syntes, nedbrytning, funktioner
- 3629
- 420
- Per Eriksson
han Glykogen Det är lagringskolhydratet hos de flesta däggdjur. Kolhydrater kallas vanligtvis sockerarter och dessa klassificeras enligt antalet avfall orsakade av hydrolys (monosackarider, disackarider, oligosackarider och polysackarider))))).
Monosackarider är de enklaste kolhydraterna som klassificeras enligt antalet kol som finns i deras struktur. Det finns då triosas (3C), tetrosor (4C), Pentosas (5C), hexosous (6C), heptosas (7C) och OctoSA (8C).
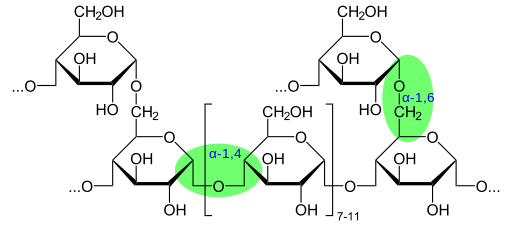
 Kemisk glykogenstruktur som visar glykosidbindningar (källa: Glykogen.SVG: Neurotogerderivatarbete: Marek M [Public Domain] via Wikimedia Commons)
Kemisk glykogenstruktur som visar glykosidbindningar (källa: Glykogen.SVG: Neurotogerderivatarbete: Marek M [Public Domain] via Wikimedia Commons) Enligt närvaron av aldehydgruppen eller Cetona -gruppen klassificeras också dessa monosackarider som aldier respektive ketosas.
Disackarider ger upphov till hydrolys, två enkla monosackarider, medan oligosackarider producerar 2 till 10 enheter monosackarider och polysackarider producerar mer än 10 monosackarider.
Glykogen är, från den biokemiska synvinkeln, en polysackarid som består av grenade kedjor av en sex -kolhöjning, det vill säga en hexos känd som glukos. Grafiskt kan det representeras för glykogen som ett glukosträd. Detta kallas också djurstärkelse.
Glukos i växter lagras som stärkelse och hos djur som glykogen, som främst lagras i levern och muskelvävnaden.
I levern kan glykogen etablera 10% av sin massa och 1% av muskelmassan. Liksom i en 70 kg man väger levern cirka 1800 g och musklerna cirka 35 kg, är den totala mängden muskelglykogen mycket större än lever.
[TOC]
Strukturera
Molekylvikten för glykogen kan nå 108 g/mol, motsvarande 6 × 105 glukosmolekyler. Glykogen består av flera grenade a-D-glycoskedjor. Glukos (C6H12O6) är en aldohexosa som kan representeras på ett linjärt eller cykliskt sätt.
Glykogen har en mycket grenad och kompakt struktur med kedjor av 12 till 14 glukosavfall i form av a-D-glukos som är kopplade till a- (1 → 4) glukosidbindningar. Kedjekomifieringarna bildas av a- (1 → 6) glukosidiska länkar.
Glykogen, som stärkelsen som intas i kosten, ger de flesta kolhydrater som kroppen behöver. I tarmen nedbryts dessa polysackarider genom hydrolys och absorberas sedan mot cirkulationslottet huvudsakligen som glukos.
Tre enzymer: ß-amylas, a-amylas och amylo-a- (1 → 6) -glukosidas är ansvariga för tarmnedbrytningen av både glykogen och stärkelse.
A-amylas hydrolyserar slumpmässigt a-bindningarna (1 → 4) av sidokedjorna av både glykogen och stärkelse och får därför namnet på endoglysidas. Ss-amyla är ett exoglikosidas som släpper ß-maltos dímeros som bryter a- (1 → 4) glykosidlänkar från ändarna på de yttersta kedjorna utan att nå konsekvenserna.
Med tanke på det faktum att varken ß-amylas eller a-amylasnedbrytning av grenar är slutprodukten av dess verkan en mycket grenad struktur på cirka 35 till 40 glukosrester som kallas Limit Dextrine.
Gränsen är dextrin slutligen hydrolyserad vid grenpunkterna som har a- (1 → 6) bindningar genom amyle-a- (1 → 6) -glukosidas, även känt som "ärekränkande" enzym. Kedjorna som släpps av denna defloat är efter nedbrytning av ß-amylas och a-amylas.
När den intagna glykogenen kommer in som glukos, måste den som finns i vävnaderna syntetiseras av organismen från glukos.
Kan tjäna dig: Purines: Egenskaper, struktur, funktionerSyntes
Glykogensyntes kallas glykogenes och äger rum särskilt i muskeln och levern. Glukosen som kommer in i organismen med dieten passerar till cirkulationslottet och därifrån inuti cellerna, där den omedelbart fosforyleras av ett enzym som kallas glycoquinase.
Glukokinasfosforyyl för att glukos i kol 6. ATP ger fosfor och energi för denna reaktion. Som ett resultat bildas glukos 6-fosfat och en ADP släpps. Sedan blir 6-fosfatglukos glukos 1-fosfat genom verkan av ett fosfoglukomutas som ler fosfor från position 6 till position 1.
1-fosfatglukosen aktiveras för glykogensyntes, vilket innebär deltagande av en uppsättning av tre andra enzymer: UDP-glykospyrofosforylas, syntetisk glykogen och amilo- (1,4 → 1,6) -glicosyltransferaser.
Glukos-1-fosfat, tillsammans med trifosfaturidin (UTP, en nukleosid av uridintrifosfat) och genom verkan av UDP-glykos-pyrofosforylas, bildar difosfat-glukos uridinkomplex (UDP GLC) (UDP GLC). Under processen hydrolyseras en pyrofosfatjon.
Sedan bildar det synteterade glykogenenzymet en glukosidisk bindning mellan C1 för UDP GLC -komplexet och C4 för en glykogen glukosterminalrester, och UDP UDP frigörs från UDP -aktiverat glukoskomplex. För att denna reaktion ska inträffa måste det finnas en befintlig glykogenmolekyl som kallas "primär glykogen".
Det primordiala glykogen syntetiseras på ett primingprotein, glykogenin, som har 37 kDa och glysila i en tyrosinrest med UDP GLC -komplexet. Därifrån är de länkade a-d-glukosavfall med 1 → 4 länkar och en liten kedja bildas på vilken syntesglykogen verkar.
När den initiala kedjan länkar minst 11 glukosrester överför gren eller amileenzym- (1,4 → 1,6) -glicosyltransferas en kedjebit av 6 eller 7 glukosavfall till den intilliggande kedjan i position 1 → 6, som fastställer en gren punkt. Glykogenmolekylen sålunda byggs växer med tillsatser av glukosenheter med glykosidlänkar 1 → 4 och fler förgreningar.
Degradering
Glykogennedbrytning kallas glukogenolys och motsvarar inte den omvända vägen för dess syntes. Hastigheten på denna rutt begränsas av hastigheten på reaktionen katalyserad av fosforylasglykogen.
Fosforyllasglykogen är ansvarig för splittring (fosforolys) av länkar 1 → 4 från glykogedkedjor, frisläppande glukos 1-fosfat. Den enzymatiska verkan börjar vid ändarna av de yttersta kedjorna och avlägsnas i följd tills 4 glukosrester finns kvar på varje sida av konsekvenserna.
Sedan lämnar ett annat enzym, a- (1 → 4) → α- (1 → 4) glukanöverföring, grenpunkten exponerad genom att överföra en trisackaridenhet från en gren till en annan. Detta tillåter amilo- (1 → 6) -glukosidas (unrampic enzym) hydrolys. Den kombinerade verkan av dessa enzymer slutar helt delas till glykogen.
Eftersom den initiala reaktionen av fosfomutas är reversibel kan 6-fosfatglukos bildas från glukosrester 1-fosfat delat från glykogen. I levern och njuren, men inte i muskeln, finns det ett enzym, glukos-6-fosfatas, som kan samlas till 6-fosfat glukos och förvandla det till fri glukos.
Kan tjäna dig: FotolysDefosforylerad glukos kan spridas till blod, och det är så leverglykogenolys återspeglas i en ökning av blodglukosvärden (glykemi).
Reglering av syntes och nedbrytning
Syntes
Denna process utövas på två grundläggande enzymer: syntesasglykogen och fosforylasglykogen, så att när en av dem är aktiverad är den andra i dess inaktiva tillstånd. Denna förordning förhindrar motsatta reaktioner av syntes och nedbrytning från att samtidigt inträffa.
Den aktiva formen och den inaktiva formen av båda enzymer är mycket annorlunda, och sammankopplingen av de aktiva och inaktiva formerna av fosforylas och syntetisk glykogen är föremål för strikt hormonell kontroll.
Adrenalin är ett hormon som frigörs från binjurarna, och glukagon är en annan som förekommer i den endokrina delen av bukspottkörteln. Endokrin bukspottkörtel producerar insulin och glukagon. Langerhans holmar α är de som syntetiserar glukagon.
Adrenalin och glukagon är två hormoner som frigörs när energi behövs som svar på minskningen av blodglukosnivåerna. Dessa hormoner stimulerar aktiveringen av fosforylasglykogen och hämmar syntesglykogen, vilket stimulerar glykogenolys och hämmar glykogenes.
Medan adrenalin utövar sin verkan på muskler och lever, verkar glukagon bara på levern. Dessa hormoner förenas med specifika membranala receptorer i den vita cellen, som aktiverar cyklasa adenilat.
Aktiveringen av cyklasadenylatet börjar ett enzymatiskt vattenfall som å ena sidan aktiverar ett AMPC -beroende proteinquinas som är inaktivt till syntetiskt glykogen och aktiverar glykogenfosforylas genom fosforylering (direkt och indirekt, respektive)).
Skelettmuskeln har en annan mekanism för aktivering av fosforylasglykogen genom kalcium, som frigörs som en följd av depolarisering av muskelmembranet i början av sammandragningen.
Av förnedring
Enzymatiska vattenfall som beskrivs ovan slutar ökande glukosnivåer och när de når en viss nivå aktiveras glykogenesen och glukogenolys hämmas, också hämmar den ytterligare frisättningen av adrenalin och glukagon.
Glykogenes aktiveras genom aktivering av fosfatasfosforylas, ett enzym som reglerar glykogensyntes av flera mekanismer, som innebär inaktivering av kinasfosforylas och fosforylas a, som är en syntesasglykogeninhibitor.
Insulin främjar inträde av glukos i muskelceller, vilket ökar 6-fosfatglukosnivåer, vilket stimulerar defosforylering och aktivering av syntesglykogen. Således börjar syntesen och nedbrytning av glykogen hämmas.
Funktioner
Muskelglykogen utgör en energireserv för muskeln som, precis som reservfetter, gör det möjligt för muskler att uppfylla sina funktioner. Som en glukoskälla används muskelglykogen under träning. Dessa reservationer ökar med fysisk träning.
I levern utgör glykogen också en viktig reservkälla för både organens funktioner och för glukosens bidrag till resten av kroppen.
Denna funktion av leverglykogen beror på att levern innehåller 6-fosfatasglukos, ett enzym som kan eliminera 6-fosfat glukosfosfatgruppen och förvandla den till fri glukos. Fri glukos, till skillnad från fosforylerad glukos, kan spridas genom hepatocytmembranet (leverceller).
Det kan tjäna dig: Sporulation: I växter, i svampar och i bakterierSå här kan levern ge glukos till cirkulation och upprätthålla stabila glukosnivåer, även under långvariga fasta förhållanden.
Denna funktion är av stor betydelse, eftersom hjärnan näras nästan uteslutande från blodglukos, så allvarlig hypoglykemi (mycket låga blodglukoskoncentrationer) kan orsaka kunskapsförlust.
Relaterade sjukdomar
Glykogenrelaterade sjukdomar får det generiska namnet på "glykogenlagringssjukdomar".
Dessa sjukdomar utgör en grupp av ärftliga patologier som kännetecknas av avsättningen i vävnaderna med onormala mängder eller typer av glykogen.
De flesta glykogenlagringssjukdomar orsakas av ett genetiskt naturunderskott av någon av de enzymer som är involverade i glykogenmetabolism.
De klassificeras i åtta typer, varav de flesta har sina egna namn och var och en av dem produceras av ett annat enzymatiskt underskott. Vissa är dödliga i mycket tidiga stadier av livet, medan andra åtföljs av muskelsvaghet och underskott under träning.
Enastående exempel
Några av de mest framträdande glykogenrelaterade sjukdomarna är följande:
- Von Gierkes sjukdom eller glykogenlagringssjukdom av typ I, produceras genom ett 6-fosfatasglukosunderskott i lever och njurar.
Det kännetecknas av onormal levertillväxt (hepatomegali) på grund av den överdrivna ackumuleringen av glykogen och hypoglykemi, eftersom levern inte kan ge glukos till cirkulation. Patienter med detta tillstånd har tillväxtförändringar.
- Pompe- eller typ II-sjukdom beror på ett a-underskott (1 → 4) -glukano 6-glykosyltransferor i lever-, hjärt- och skelettmusklerna. Denna sjukdom, som Andersen eller typ IV, är dödlig före de två åren av livet.
- McArdle eller typ V -sjukdom har ett muskelfosforylasunderskott och åtföljs av muskelsvaghet, minskad träningstolerans, onormal ackumulering av muskelglykogen och frånvaro av laktat under träning under träning.
Referenser
- Bhattacharya, K. (2015). Undersökning och hantering av glykogenlagringssjukdomar. Translationell pediatrik, 4(3), 240-248.
- Dagli, a., Sentner, C., & Weinstein, D. (2016). Glykogenlagringssjukdomstyp III. Genrecensioner, 1-16.
- Guyton, a., & Hall, J. (2006). Lärobok för medicinsk fysiologi (11: e upplagan.). Elsevier Inc.
- Mathews, C., Van Holde, K., & Ahern, K. (2000). Biokemi (3: e upplagan.). San Francisco, Kalifornien: Pearson.
- McKiernan, s. (2017). Patobiologi för leverens glykogenlagring. Curr pathobiol rep.
- Murray, r., Bender, D., Botham, K., Kennelly, s., Rodwell, V., & Weil, s. (2009). Harpers illustrerade biokemi (28: e upplagan.). McGraw-Hill Medical.
- Nelson, D. L., & Cox, M. M. (2009). Lehninger principer för biokemi. Omega -utgåvor (5: e upplagan.).
- Rawn, j. D. (1998). Biokemi. Burlington, Massachusetts: Neil Patterson Publishers.
- Tarnopolsky, m. TILL. (2018). Myopatier relaterade till glykogenmetabolismstörningar. Neuroterapeutik.
- « Argon historia, struktur, egenskaper, användningar
- Bijective Funktion Vad är, hur görs det, exempel, övningar »

