Bariumoxid (BAO) struktur, egenskaper, användningar, risker

- 4635
- 1461
- Johan Johansson
han bariumoxid Det är ett oorganiskt fast ämne som bildas av en bariumatom (BA) och en syre (O) atom. Dess kemiska formel är Bao. Det är ett vitt kristallint fast ämne och är hygroskopiskt, det vill säga den absorberar luftens fukt, men därmed reagerar den med detta.
Den snabba reaktionen av bariumoxid med vatten gör att den används i kemiska analyslaboratorier, det vill säga att eliminera vatten från organiska lösningsmedel, som är flytande föreningar som tjänar till att lösa upp andra ämnen.
 Solid bao bariumoxid. Lem [cc by-sa 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Källa: Wikimedia Commons.
Solid bao bariumoxid. Lem [cc by-sa 4.0 (https: // CreativeCommons.Org/licenser/BY-SA/4.0)]. Källa: Wikimedia Commons. Bao uppför sig som en stark bas, reagerar därför med många typer av syror. Reagera till exempel lätt med koldioxid2 av luften för att bilda bariumkarbonat Bacchus3.
Det tjänar i tillverkningen av polymerer för elkablar och som en hartsingrediens för att försegla tänder som har botats.
Bariumoxid (BAO) används också inom keramikindustrin, både för att täcka den med glasering och för att tillverka den. Det används också i cementblandningar för att öka komprimeringsmotståndet för slutprodukten.
[TOC]
Strukturera
Bao Baar -oxid bildas av en katjon BA2+ och en syreanjon eller2-.
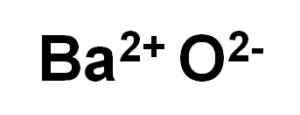 Bao bariumoxidjoner. Författare: Marilú Stea.
Bao bariumoxidjoner. Författare: Marilú Stea. I dess kristaller bildar Bao kubiska joniska nätverk (i form av en kub) av natriumkloridtypen.
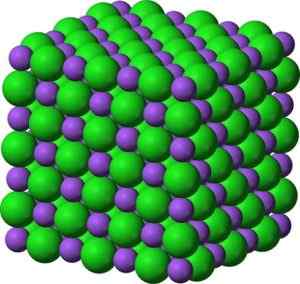 Bao bariumoxidformad kristallin struktur som liknar natriumklorid. Grön: Barium. Blå: syre. Benjah-Bmm27 (Talk · Bidrag) [Public Domain]. Källa: Wikimedia Commons.
Bao bariumoxidformad kristallin struktur som liknar natriumklorid. Grön: Barium. Blå: syre. Benjah-Bmm27 (Talk · Bidrag) [Public Domain]. Källa: Wikimedia Commons. Den elektroniska konfigurationen av bariumjonen är: [xe] 6s0 Tja, de två elektronerna i 6S -skiktet har tappat. Denna konfiguration är mycket stabil.
Nomenklatur
-Bariumoxid
-Bariummonoxid
Det kan tjäna dig: Test: Egenskaper, typer, exempel på användningsområdenFysikaliska egenskaper
Fysiskt tillstånd
Gulaktig vit kristallint fast.
Molekylvikt
153,33 g/mol
Smältpunkt
1923 ºC
Kokpunkt
Ungefär 2000 ºC.
Densitet
5,72 g/cm3
Löslighet
Lite vattenlösligt: 3,8 g/100 ml vid 20 ºC.
Kemiska egenskaper
Bario Bao -oxid reagerar snabbt2, vilket är den mest lösliga hydroxiden mellan alkalineteriska metallhydroxider.
Bao + h2O → BA (OH)2
Bao är en stark bas. Reagerar exotermiskt (det vill säga med värmeavskiljning) med alla typer av syror.
Med CO2 Bao reagerar för att bilda bariumkarbonat Bacchus3.
Bao + co2 → Bacchus3
Bao är hygroskopisk, för om det är tillåtet för miljön, förenas den gradvis till luftens fukt och bildar BA (OH)2 som kombineras med koldioxid2 av luften för att ge bariumkarbonat Bacchus3.
När Bao -bariummonoxiden värms upp i närvaro av luft, kombineras den med syre som bildar bariumperoxidbao2. Reaktionen är reversibel.
2 Bao + O2 ⇔ 2 bao2
I närvaro av vatten kan det reagera med aluminium på OR med FIFC Zn som bildar oxider eller hydroxider av dessa metaller och genererar vätgas h2.
Du kan initiera polymerisation av organiska föreningar som kan polymeriseras, såsom epoxider.
Risker
Det kan vara giftigt genom intag. Du bör inte kontakta huden. Det är irriterande ögon, hud och luftvägar. Det kan vara skadligt för nervsystemet. Det kan orsaka låga kaliumnivåer, vilket resulterar i hjärt- och muskelsjukdomar.
Erhållande
Bao bariumoxid kan erhållas genom att värma bario baco karbonat3 Med kol. Bao är bildad och kolmonoxidgas släpps.
Bacchus3 + C → Bao + 2 Co ↑
Ansökningar
Som torkmedel av organiska lösningsmedel
På grund av dess lätthet att reagera med vatten har Bao använts sedan mitten av förra seklet som torkmedel för bensin och grundläggande organiska lösningsmedel.
Det kan tjäna dig: CyanhyDric Acid: Molecular Structure, Egenskaper, användningarBAO är mycket aktivt torkar runt den, den tar fukt mycket snabbt, med utveckling av ganska värme, bildar bariumhydroxid BA (OH)2 vilket är stabilt upp till cirka 1000 ºC. Därför kan BAO användas vid höga temperaturer.
Den har också en hög vattenabsorptionskapacitet. För varje BAO -molekyl kan man ta upp ett vatten och BA (OH)2 Resultat kan också absorbera en viss mängd vatten.
Det är lämpligt för analytiska kemi laboratorier. Det är inte klibbigt.
Det kan användas i torkare, som är stora glasbehållare med lock där den torra inre atmosfären upprätthålls. Bao håller miniatmosfären av torkatorn torr.
 Distinters i ett laboratorium. Torkmedlet som Bao placeras längst ner på basen. Den ursprungliga uppladdaren var Rifleman 82 på engelska Wikipedia. [CC BY-SA 3.0 (http: // Creativecommons.Org/licenser/BY-SA/3.0/]]. Källa: Wikimedia Commons.
Distinters i ett laboratorium. Torkmedlet som Bao placeras längst ner på basen. Den ursprungliga uppladdaren var Rifleman 82 på engelska Wikipedia. [CC BY-SA 3.0 (http: // Creativecommons.Org/licenser/BY-SA/3.0/]]. Källa: Wikimedia Commons. Dessa torkare tjänar till att placera ämnen eller reagens och därmed förhindra dem från att absorbera vatten från miljön.
Det tjänar också till att torka grundgaser som ammoniak NH3.
I nedladdningslampor
Bao placeras i elektroderna i urladdningslamporna som ett elektronutsläppsmaterial.
Utsläppslampor bildas av ett glasrör, kvarts eller annat lämpligt material, innehåller en inert gas och i de flesta fall en metallånga. Metallisk ånga kan vara natrium eller kvicksilver.
 Kvicksilverlampa. Dmitry G [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikimedia Commons.
Kvicksilverlampa. Dmitry G [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikimedia Commons. Inuti röret uppstår elektrisk stöt eftersom den har en positiv och negativ elektrod.
BAO placeras i lampelektroder. Elektronerna släpps ut kollidera med metallångatomerna och överför energi.
Det kan tjäna dig: Cupric Oxide (CUO)När du passerar en elektrisk ström genom denna gas eller ånga finns det synligt ljus eller ultraviolett strålning (UV).
I keramisk tillverkning
BAO används i glaserade keramiska beläggningskompositioner.
 Belagd byggnadsfasad med glaserad keramik. Penny Mayes/glaserad fasad. Källa: Wikimedia Commons.
Belagd byggnadsfasad med glaserad keramik. Penny Mayes/glaserad fasad. Källa: Wikimedia Commons. Det har emellertid också testats som ett tillsatsmedel vid framställningen av HOB.
BAO förbättrar effektivt mekaniska egenskaper och kemisk resistens hos denna typ av keramik. Det har ett starkt inflytande på termiska egenskaper och sammansättningen av den kristallina fasen hos de erhållna materialen.
Vid beredning av cementblandningar
BAO har testats som en del av fosfoaluminatcement.
Denna typ av cement är användbar i marina miljöer, eftersom den inte har samma tendens att hydrera som andra typer av cement, så det lider inte av por eller expansion.
Fosfoalumineringscement måste emellertid stärkas i deras mekaniska prestanda för att kunna motstå marina strömmar och slag av flytande isbitar som finns i havet.
Tillägget av Bao till fosfoalumineringscementet modifierar mineralstrukturen för nämnda material, förbättrar porens struktur och ökar avsevärt tryckkraften för cementpasta.
Med andra ord förbättrar Bao kompressionsmotståndet för denna typ av cement.
 Blandning för betong. Bao bariumoxid är användbar för att förbättra vissa cementegenskaper. Thamizhpparithi Maari [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikimedia Commons.
Blandning för betong. Bao bariumoxid är användbar för att förbättra vissa cementegenskaper. Thamizhpparithi Maari [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenser/BY-SA/3.0)]. Källa: Wikimedia Commons. I flera applikationer
Det används som en ingrediens för att ge opacitet i tandhartser för fyllning av hål i tänderna, utförda av tandläkare.
Det används också som ett kärnbildningsmedel för framställning av polyvinylidenfluoridpolymerer som används för att isolera elkablar.
Referenser
- Partka, J. et al. (2016). Effekt av tillsats av BAO på sintring av glaskeramiska material från SIO2-Till2ANTINGEN3-Na2OKEJ2O-cao/mgo-system. J Therm Anal Calim (2016) 125: 1095. Länk återhämtat sig.Kandare.com.
- Zhang, s. et al. (2019). Effekt av BAO på mineralstruktur och hydratisering av fosfoaluminatcement. J Therm Anal Calim (2019) 136: 2319. Länk återhämtat sig.Kandare.com.
- ELLER.S. National Library of Medicine. (2019). Oxidbarium. Återhämtat sig från pubchem.Ncbi.Nlm.Nih.Gov.
- Smith, n.TILL. (2003). Belysning. Princip. I Electrical Engineers referensbok (sextonde upplagan). Återhämtat sig från Scientedirect.com.
- Ebnejjad, s. (2003). Fluoropolymerskum. PVDF -skumning. I smältprocesserbar fluoroplast. Återhämtat sig från Scientedirect.com.
- Booth, h.S. och McIntyre, L.H. (1930). Bariumoxid som en desicant. Ind. Göra. Kem. Anal. Ed. 1930, 2, 1, 12-15. Återhämtat sig från pubar.ACS.org.
- « Natriumcyanid (NACN) struktur, egenskaper, risker, användningar
- De 15 bästa livsmedel för att öka skinkorna (naturliga) »

